Clear Sky Science · zh
与小鼠心肌缺血再灌注损伤相关的异常可变剪接及RNA结合蛋白调控因子的综合分析
为什么恢复血流仍会伤害心脏
当有人发生心肌梗死时,医生会尽快疏通阻塞的动脉以恢复血流。然而,这一挽救生命的步骤也可能在延迟阶段引发一波损伤,称为再灌注损伤。本研究在小鼠心脏细胞中深入探查血流恢复时微小的RNA信息如何被切割和编辑,以及这些变化如何可能加重或缓解损伤。理解这一隐蔽的调控层或能为心肌梗死后的保护措施开辟新路径。
心细胞内的隐性信息
每个细胞都使用RNA作为遗传信息的工作拷贝。在这些RNA信息被用来合成蛋白质之前,它们可以以不同方式被切割和重连,这一过程称为可变剪接。这意味着单个基因可以产生多种具有不同功能的蛋白质版本。作者探讨了在标准的冠状动脉受控闭塞与再通模型(模拟心梗及其治疗)中,小鼠心脏的这一编辑过程如何改变。他们重新分析了一个现有的RNA测序数据集,该数据集比较了受损小鼠心组织与假手术对照组的差异。
损伤后广泛的RNA编辑转变
研究团队发现,再灌注损伤伴随着全基因组范围内RNA编辑模式的显著变化。他们检测到数百个剪接事件在健康心脏与受损心脏之间的使用频率存在差异,尤其集中在RNA片段的起始端。许多受影响的基因属于重要的细胞信号通路,这些通路决定心肌细胞是生长、回收组分还是自我毁灭。特别是mTOR和MAPK通路中的基因——这些通路参与细胞代谢、应激反应和炎症的调控——在其RNA的切割与组装方式上呈现出强烈变化。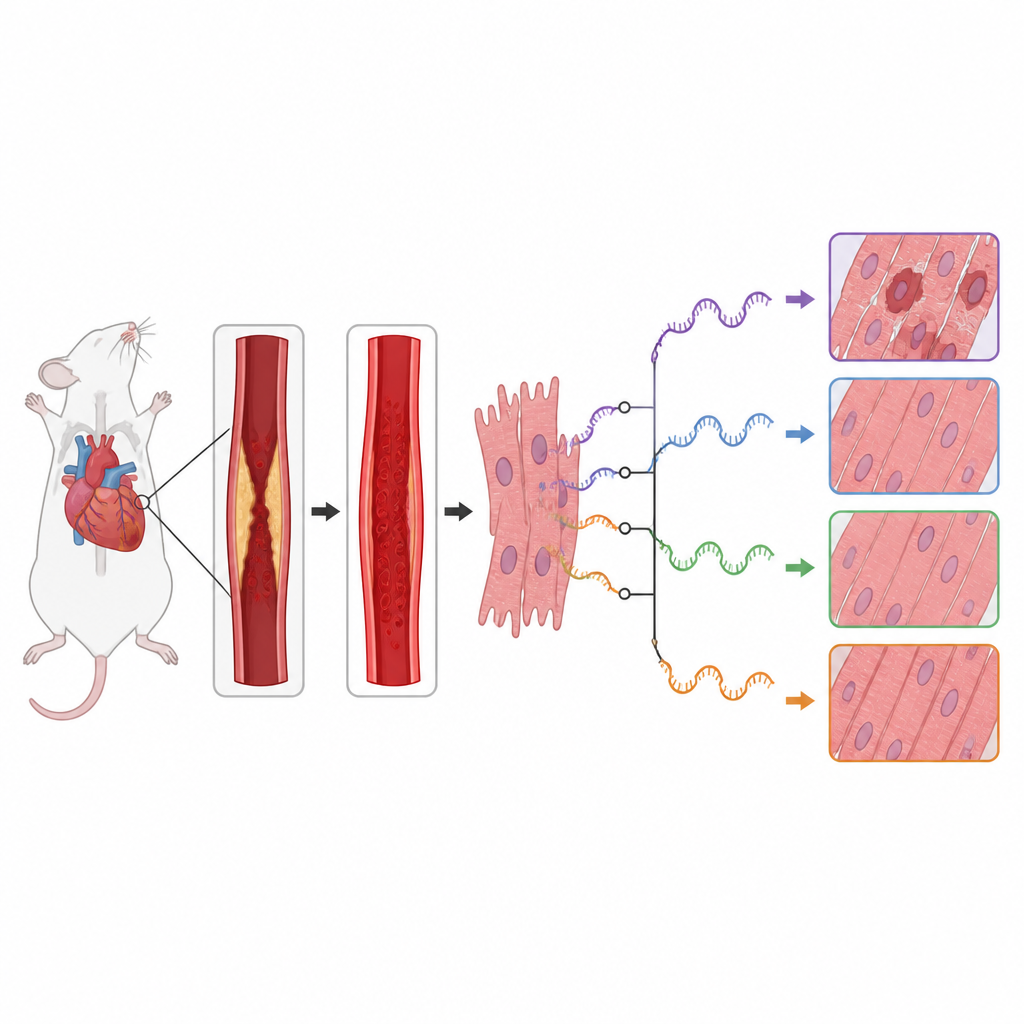
引导RNA切割的蛋白质
RNA结合蛋白如同交通指挥,决定每条RNA在哪儿被切割和拼接。通过比较受损与对照心脏的基因表达,研究者鉴定出一百多种在损伤后水平发生变化的此类蛋白。许多蛋白与血管生长和低氧应答相关,这两者对心脏恢复至关重要。其中一个蛋白LMNA格外引人注目,其水平与一个名为Atp6v1h基因的特定RNA的编辑程度密切相关,该基因参与调控与mTOR信号相关的细胞泵。该RNA的剪接形式在受损心脏中更为常见,暗示LMNA可能在再灌注应激期间帮助微调能量感知。
聚焦关键基因并在动物中验证
作者重点列举了若干其编辑RNA形式可能使心肌细胞偏向生存或受损的基因。例如,缺氧应答因子Eif4e2、与炎症相关的调控因子Traf6、胰岛素受体Insr以及应激敏感调节子Nr4a1在损伤后都产生了更常见的RNA变体。另一些基因,如Map4k4,则显示出特定剪接形式的使用减少。为检验这些RNA变化在计算分析之外是否真实存在,团队构建了自己的小鼠再灌注损伤模型。他们确认了许多预测的基因变体和RNA结合蛋白在RNA和蛋白水平上都发生了同方向的变化,从而强化了这些特征为受损心脏真实现象的证据。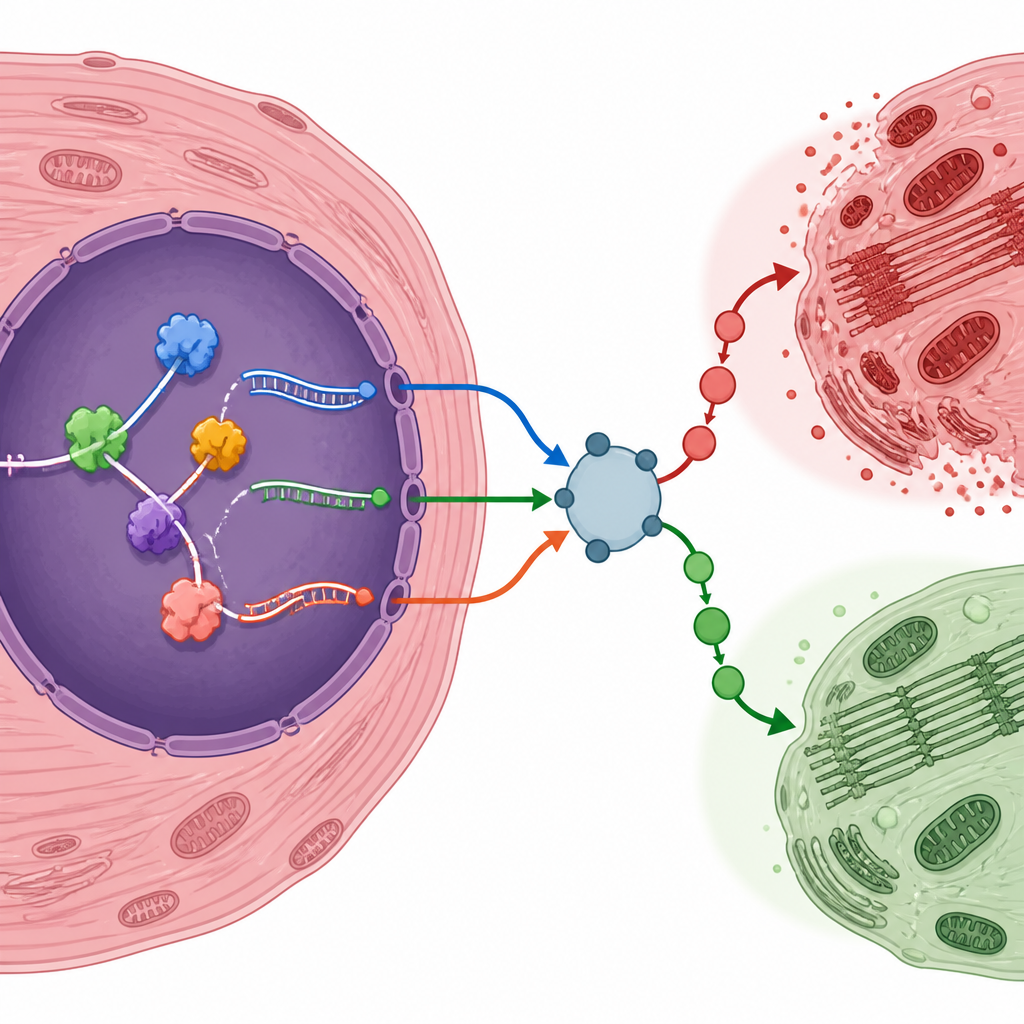
对未来心脏治疗的意义
简言之,这项工作表明,血流恢复后,细胞迅速通过以新的方式重新剪接RNA来重编其内部信息,这一过程由一组调控蛋白引导。这些被编辑的信息微调了决定细胞应激、清理与炎症的主要决策通路。尽管该研究在小鼠中进行,尚未证明因果关系,但它绘制出一张候选RNA开关及其调控网络图,这些开关可能决定心梗后最终的永久性损伤程度。未来,温和调整RNA结合蛋白或特定剪接模式的疗法,可能成为当前治疗的补充,为在恢复血供时更精确地保护心脏提供可能。
引用: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
关键词: 心肌缺血再灌注损伤, 可变剪接, RNA结合蛋白, mTOR通路, MAPK信号传导