Clear Sky Science · tr
Fare sonrası miyokard iskemik reperfüzyon hasarıyla ilişkili anormal alternatif spleyis ve RNA-bağlayıcı protein düzenleyicilerinin kapsamlı analizi (fare modeli)
Kalbin yeniden çalıştırılması neden yine zarar verebilir
Bir kişinin kalp krizi geçirdiğinde, doktorlar tıkalı arterleri açıp kan akışını yeniden sağlamaya çalışır. Ancak bu hayat kurtarıcı müdahale, reperfüzyon hasarı adı verilen gecikmiş bir zarar dalgasına da yol açabilir. Farelerde yapılan bu çalışma, kan akışı geri geldiğinde kalp hücreleri içindeki küçük RNA iletilerinin nasıl kesilip düzenlendiğini ve bu değişikliklerin hasarı nasıl kötüleştirebileceğini veya hafifletebileceğini derinlemesine inceliyor. Bu gizli kontrol katmanını anlamak, kalbi kalp krizi sonrası korumaya yönelik yeni yollar açabilir.
Kalp hücreleri içindeki gizli iletiler
Her hücre genetik bilginin çalışan kopyası olarak RNA kullanır. Bu RNA iletileri protein yapmak için kullanılmadan önce alternatif spleys olarak bilinen farklı şekillerde kesilip yeniden birleştirilebilir. Bu, tek bir genin birbirinden farklı etkileri olan birkaç protein versiyonu üretebileceği anlamına gelir. Yazarlar, bu düzenleme sürecinin, standart bir kalp krizi ve tedavisi modeli olan koroner bir arterin kontrollü olarak tıkanması ve yeniden açılmasına maruz kalan fare kalplerinde nasıl değiştiğini sordular. Yaralanmış fare dokusunu sahte operasyona tabi tutulmuş kontrollere karşı karşılaştıran mevcut bir RNA dizileme veri setini yeniden analiz ettiler.
Hasar sonrası RNA düzenlemesinde geniş kaymalar
Araştırma ekibi, reperfüzyon hasarının genom çapında RNA düzenleme desenlerinde kapsamlı kaymalarla eşlik ettiğini buldu. Sağlıklı ve hasarlı kalpler arasında kullanımı farklı olan yüzlerce spleys olayı tespit ettiler; özellikle RNA segmentlerinin başlangıç uçlarındaki değişiklikler göze çarpıyordu. Etkilenen birçok gen, kalp kası hücrelerinin büyüyüp büyümeyeceğine, bileşenlerini geri dönüştürüp geri dönüştürmeyeceğine ya da kendi kendini imha edip etmeyeceğine karar veren önemli hücre sinyal yollarına aitti. Özellikle hücre metabolizması, stres yanıtları ve inflamasyonu kontrol etmeye yardımcı olan mTOR ve MAPK yollarındaki genler, RNA’larının nasıl kesilip birleştirildiğinde güçlü değişiklikler gösterdi. 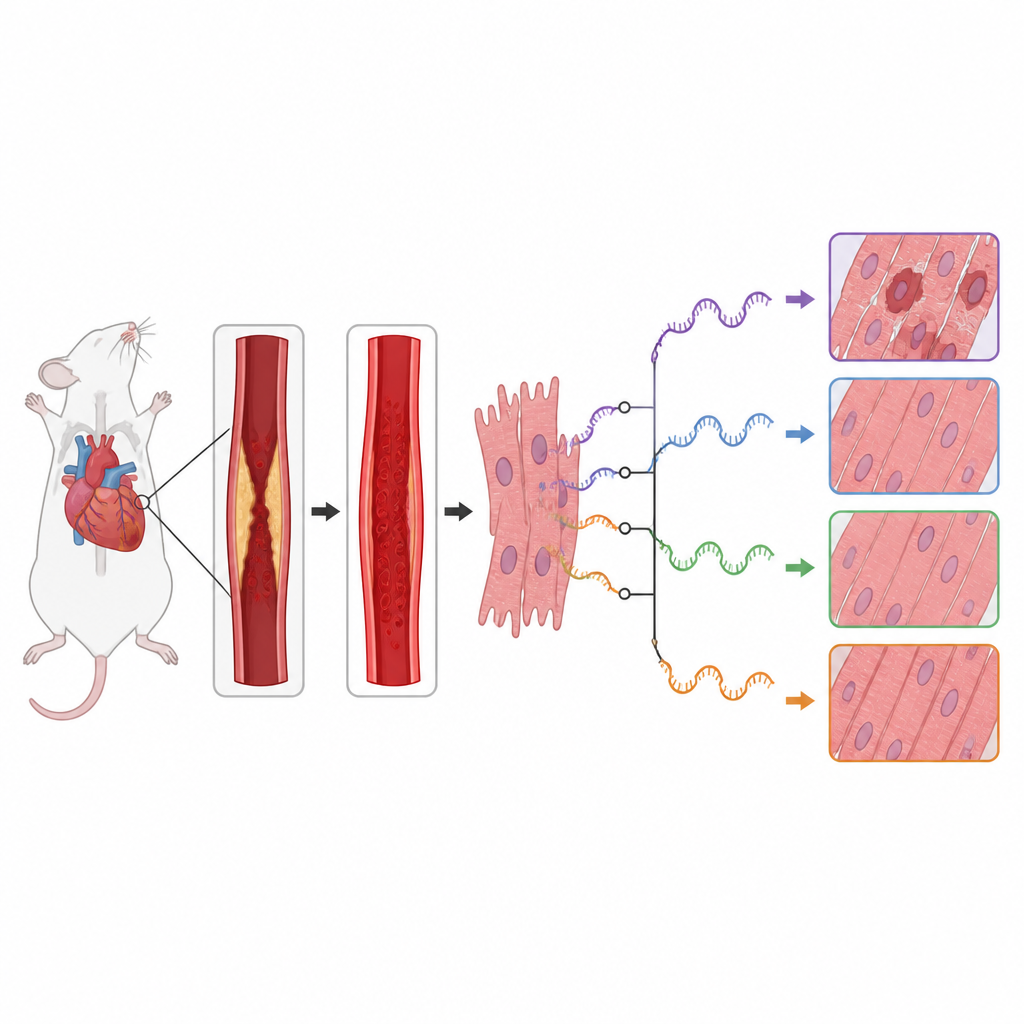
RNA kesimini yönlendiren proteinler
RNA bağlayıcı proteinler, her RNA’nın nereden kesilip dikileceğine karar veren trafik denetçileri gibi davranır. Yaralanmış ve kontrol kalplerdeki gen aktivitesini karşılaştırarak, araştırmacılar yaralanma sonrası düzeyi değişen yüzün üzerinde böyle protein belirledi. Birçoğu kan damarlarının büyümesi ve düşük oksijene yanıtlarla ilişkiliydi; bunlar kalbin toparlanmasında merkezi süreçlerdir. LMNA adlı bir protein öne çıktı çünkü düzeyi, mTOR sinyalleşmesiyle ilişkili hücresel bir pompayı düzenlemeye yardımcı olan Atp6v1h geninin belirli bir RNA’nın düzenlenmesiyle yakından ilişki gösteriyordu. Bu RNA’nın splice edilmiş formu hasarlı kalplerde daha yaygındı; bu da LMNA’nın reperfüzyon stresinde enerji algılamayı ince ayarlamaya yardımcı olabileceğini düşündürüyor.
Ana genlere odaklanma ve hayvanda doğrulama
Yazarlar, düzenlenmiş RNA formları kalp hücrelerini hayatta kalma veya hasara eğilimli hale getirebilecek birkaç geni öne çıkardı. Örneğin, hipoksiye yanıt veren bir faktör olan Eif4e2, inflamasyonla ilişkili düzenleyici Traf6, insulin reseptörü Insr ve stres duyarlı düzenleyici Nr4a1, yaralanma sonrası daha sık görülen RNA varyantları üretti. Map4k4 gibi diğerleri ise belirli splice formlarının kullanımında azalma gösterdi. Bu RNA değişimlerinin yalnızca bilgisayar analizleri ötesinde gerçek olup olmadığını test etmek için ekip kendi fare reperfüzyon hasarı modelini oluşturdu. Birçok öngörülen gen varyantının ve RNA bağlayıcı proteinin hem RNA hem de protein düzeylerinde aynı yönde değiştiğini doğruladılar; bu da bunların yaralı kalbin gerçek özellikleri olduğu görüşünü güçlendiriyor. 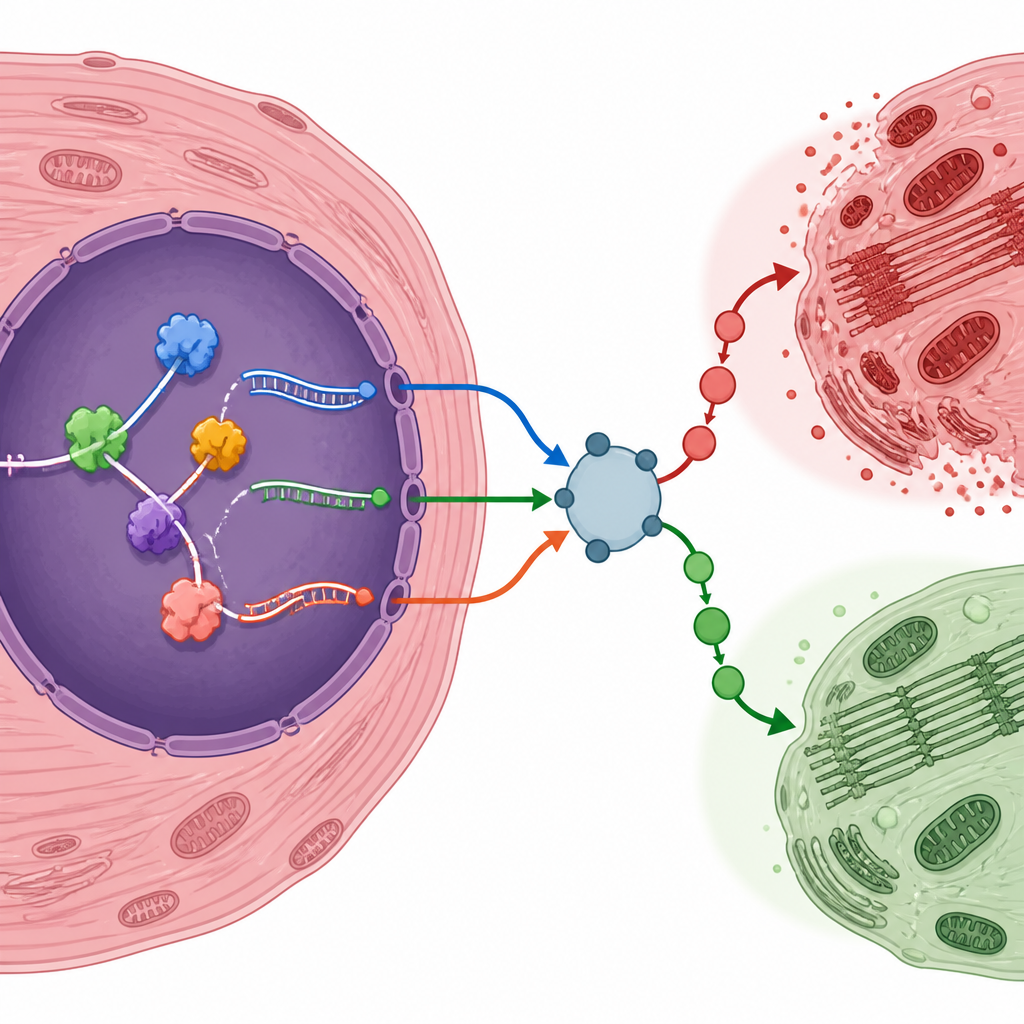
Geleceğin kalp bakımına etkileri
Açıkça söylemek gerekirse, bu çalışma kan akışı kalbe geri döndüğünde hücrelerin iç iletilerini yeni yollarla hızla yeniden yapılandırdığını; bu sürecin RNA’nın farklı şekillerde yeniden kesilmesiyle ve bir dizi düzenleyici protein tarafından yönlendirildiğini gösteriyor. Bu düzenlenmiş iletiler, hücre stresini, temizlik süreçlerini ve inflamasyonu yöneten önemli karar alma yollarını değiştiriyor. Çalışma farelerde yapıldığı ve henüz neden-sonuç kanıtı sunmadığı halde, kalp krizi sonrası ne kadar kalıcı hasar oluştuğunu şekillendirebilecek aday RNA anahtarları ve bunların denetleyicilerinin bir ağını haritalıyor. Zamanla, RNA bağlayıcı proteinleri veya belirli splice desenlerini hassas biçimde ayarlayan terapiler, mevcut tedavilere tamamlayıcı olarak kan akışı yeniden sağlandığında kalbi korumaya daha hedefe yönelik bir yol sunabilir.
Atıf: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Anahtar kelimeler: miyokard iskemi reperfüzyon hasarı, alternatif spleys, RNA bağlayıcı proteinler, mTOR yolu, MAPK sinyalleşmesi