Clear Sky Science · it
Analisi completa dello splicing alternativo aberrante e dei regolatori delle proteine leganti l'RNA associati al danno da ischemia-riperfusione miocardica nei topi
Perché la riapertura del cuore può comunque danneggiare
Quando una persona ha un infarto, i medici si affrettano a riaprire l'arteria bloccata e ripristinare il flusso sanguigno. Tuttavia questo passo salvavita può anche danneggiare il cuore in un'onda ritardata chiamata danno da riperfusione. Questo studio sui topi esplora in profondità nelle cellule cardiache come i minuscoli messaggi RNA vengono tagliati e modificati quando il flusso sanguigno ritorna, e come tali cambiamenti possano aggravare o attenuare il danno. Capire questo livello nascosto di controllo potrebbe aprire nuove strade per proteggere il cuore dopo un infarto.
Messaggi nascosti all'interno delle cellule cardiache
Ogni cellula usa l'RNA come copia operativa dell'informazione genetica. Prima che questi messaggi RNA vengano usati per produrre proteine, possono essere tagliati e ricongiunti in modi diversi, un processo noto come splicing alternativo. Questo significa che un singolo gene può generare diverse versioni proteiche con effetti distinti. Gli autori si sono chiesti come questo processo di editing cambi nei cuori di topo sottoposti a un'occlusione controllata e alla riapertura di una arteria coronaria chiave, un modello standard di infarto seguito da trattamento. Hanno rianalizzato un dataset esistente di sequenziamento dell'RNA che metteva a confronto il tessuto cardiaco di topi danneggiati con controlli sham operati.
Ampie variazioni nello splicing dell'RNA dopo il danno
Il gruppo ha scoperto che il danno da riperfusione è stato accompagnato da ampie variazioni nei modelli di splicing dell'RNA in tutto il genoma. Hanno rilevato centinaia di eventi di splicing il cui uso differiva tra cuori sani e danneggiati, soprattutto all'estremità iniziale dei segmenti di RNA. Molti dei geni interessati appartenevano a importanti vie di segnalazione cellulare che decidono se le cellule muscolari cardiache crescono, riciclano i propri componenti o vanno incontro ad autodistruzione. In particolare, i geni delle vie mTOR e MAPK, che contribuiscono a controllare il metabolismo cellulare, le risposte allo stress e l'infiammazione, hanno mostrato forti cambiamenti nel modo in cui il loro RNA veniva tagliato e assemblato. 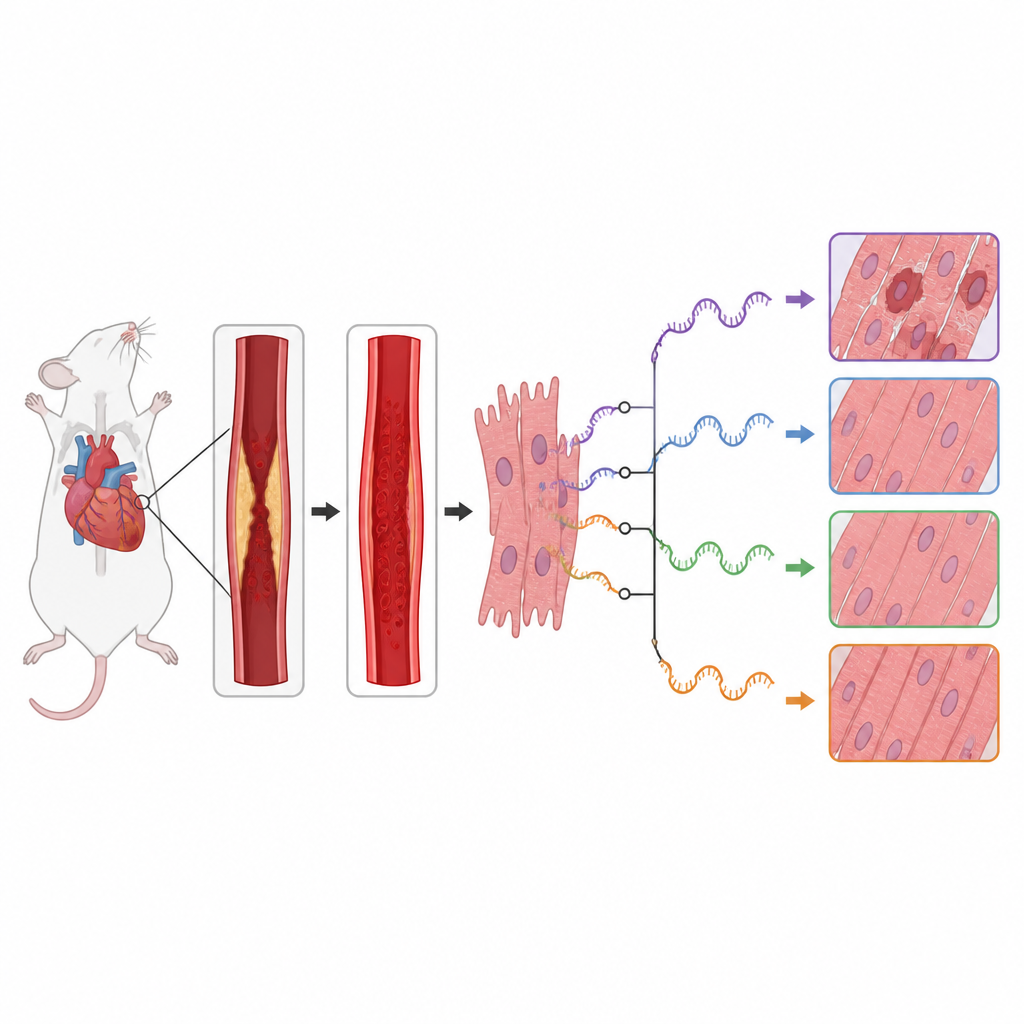
Proteine che indirizzano il taglio dell'RNA
Le proteine leganti l'RNA agiscono come controllori del traffico che decidono dove ogni RNA viene affettato e ricucito. Confrontando l'attività genica nei cuori danneggiati e di controllo, i ricercatori hanno identificato più di cento di queste proteine i cui livelli sono cambiati dopo il danno. Molte erano collegate alla crescita dei vasi sanguigni e alle risposte all'ipossia, due processi centrali per il recupero cardiaco. Una proteina, LMNA, si è distinta perché i suoi livelli seguivano da vicino lo splicing di un RNA specifico di un gene chiamato Atp6v1h, che aiuta a regolare una pompa cellulare legata alla segnalazione mTOR. La forma splicata di questo RNA era più comune nei cuori danneggiati, suggerendo che LMNA potrebbe contribuire a tarare la rilevazione energetica durante lo stress della riperfusione.
Zoom sui geni chiave e conferme negli animali
Gli autori hanno evidenziato diversi geni le cui forme di RNA editate possono inclinare le cellule cardiache verso la sopravvivenza o il danno. Per esempio, un fattore responsivo all'ipossia chiamato Eif4e2, un regolatore legato all'infiammazione Traf6, il recettore dell'insulina Insr e un regolatore sensibile allo stress Nr4a1 hanno tutti prodotto varianti di RNA più frequenti dopo il danno. Altri, come Map4k4, hanno mostrato una ridotta utilizzazione di particolari forme di splicing. Per verificare se questi spostamenti nell'RNA fossero reali oltre l'analisi computazionale, il gruppo ha creato il proprio modello murino di danno da riperfusione. Hanno confermato che molte delle varianti geniche previste e delle proteine leganti l'RNA cambiavano nella stessa direzione sia a livello di RNA sia a livello proteico, rafforzando l'ipotesi che si tratti di caratteristiche genuine del cuore lesionato. 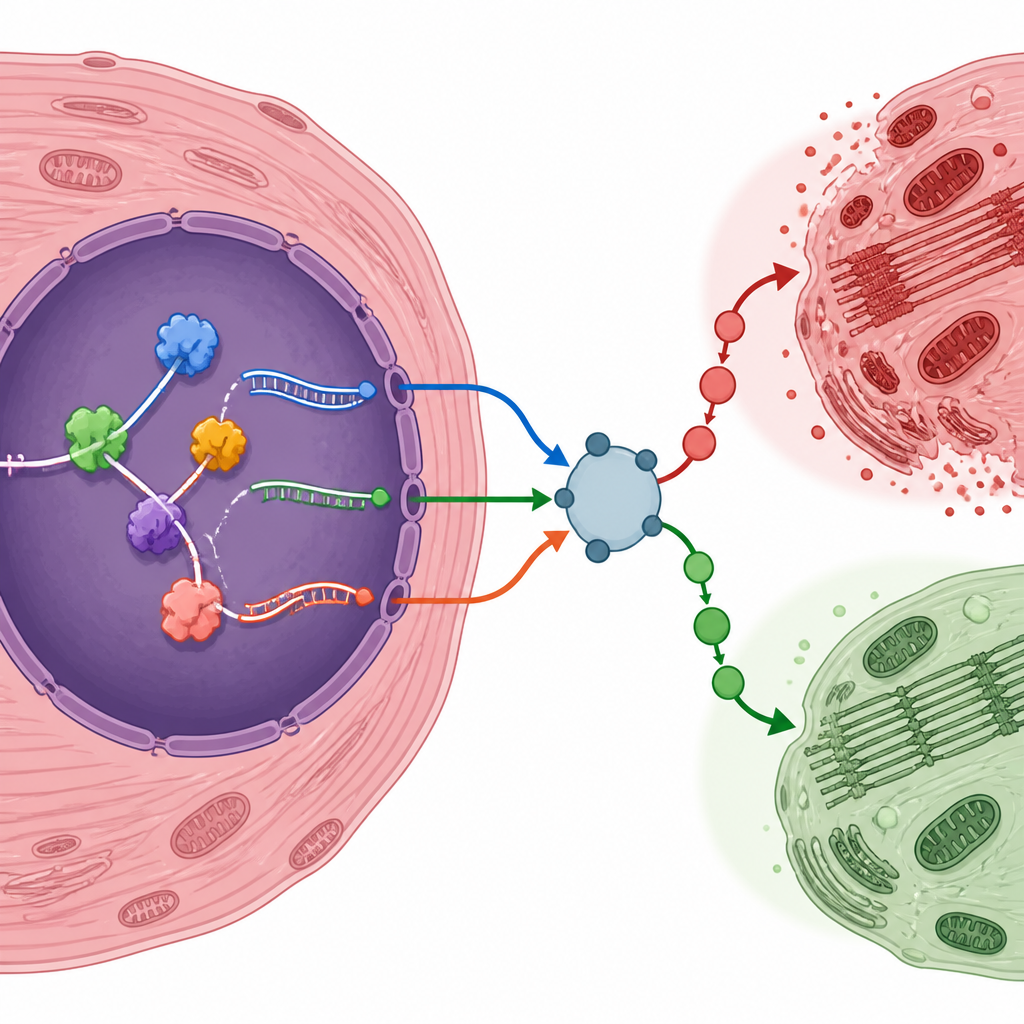
Cosa significa per la cura futura del cuore
In termini semplici, questo lavoro mostra che dopo il ripristino del flusso sanguigno, le cellule cardiache riorganizzano rapidamente i loro messaggi interni ricutendo l'RNA in modi nuovi, guidate da un insieme di proteine regolatrici. Questi messaggi editati modulano importanti vie decisionali che governano lo stress cellulare, la pulizia dei componenti e l'infiammazione. Sebbene lo studio sia stato condotto sui topi e non dimostri ancora causa ed effetto, mappa una rete di potenziali interruttori di RNA e dei loro controllori che potrebbero determinare quanto danno permanente segue a un infarto. Col tempo, terapie che modulano con delicatezza le proteine leganti l'RNA o specifici schemi di splicing potrebbero affiancare i trattamenti attuali, offrendo modi più precisi per proteggere il cuore quando viene ripristinata la sua fornitura di sangue.
Citazione: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Parole chiave: danno da ischemia-riperfusione miocardica, splicing alternativo, proteine leganti l'RNA, via mTOR, segnalizzazione MAPK