Clear Sky Science · sv
Omfattande analys av avvikande alternativ splitsning och regulatorer av RNA-bindande proteiner kopplade till myokardial ischemi-reperfusionsskada hos möss
Varför återställande av hjärtats blodflöde fortfarande kan skada hjärtat
När någon drabbas av en hjärtinfarkt skyndar läkare för att öppna den blockerade artären och återställa blodflödet. Men denna livräddande åtgärd kan också skada hjärtat i en fördröjd våg av skada som kallas reperfusionsskada. Denna studie i möss undersöker på cellnivå hur små RNA-meddelanden skärs och redigeras när blodflödet återkommer, och hur dessa förändringar kan förvärra eller lindra skadan. Att förstå detta dolda kontrollager kan öppna nya vägar för att skydda hjärtat efter en infarkt.
Dolda meddelanden inuti hjärtceller
Varje cell använder RNA som en arbetskopia av den genetiska informationen. Innan dessa RNA-meddelanden används för att bygga proteiner kan de skäras och sammanfogas på olika sätt, en process som kallas alternativ splitsning. Det innebär att en enda gen kan ge upphov till flera proteinkonfigurationer med skilda effekter. Författarna frågade hur denna redigeringsprocess förändras i mushjärtan som utsattes för en kontrollerad blockering och återöppning av en huvudkoronarartär, en standardmodell för hjärtinfarkt följt av behandling. De gjorde en nyanalys av en befintlig RNA-sekvenseringsuppsättning som jämförde hjärtvävnad från skadade möss med skenopererade kontrollgrupper.
Breda skiften i RNA-redigering efter skada
Teamet fann att reperfusionsskada åtföljdes av omfattande förändringar i RNA-redigeringsmönster över hela genomet. De upptäckte hundratals splitsningsevenemang vars användning skilde sig mellan friska och skadade hjärtan, särskilt vid RNA-segmentens startände. Många av de påverkade generna tillhörde viktiga cellsignalvägar som avgör om hjärtmuskelceller växer, återvinner sina komponenter eller genomgår självdestruktion. Särskilt gener i mTOR- och MAPK-vägarna, som hjälper till att styra cellers metabolism, stressvar och inflammation, visade starka förändringar i hur deras RNA skars och monterades. 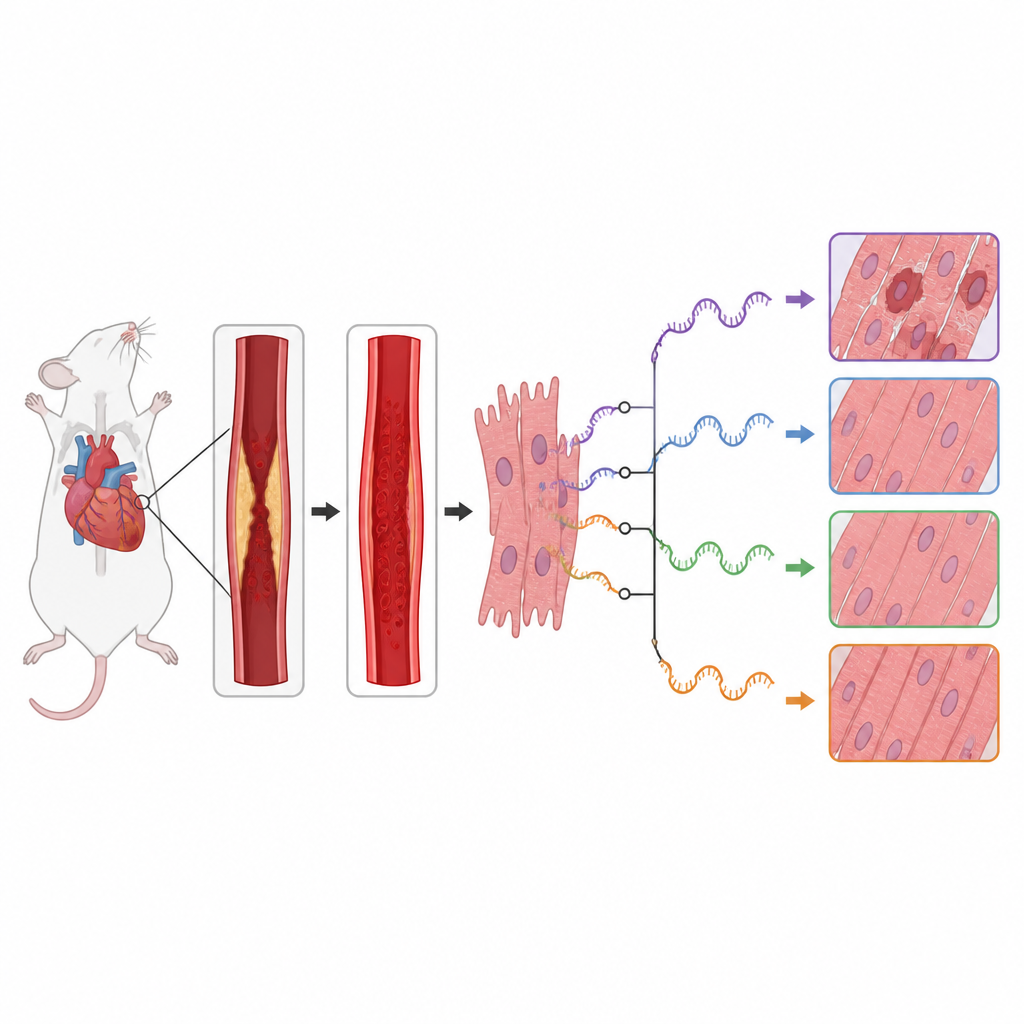
Proteiner som styr RNA-skarvning
RNA-bindande proteiner fungerar som trafikregulatorer som bestämmer var varje RNA ska skäras och sys ihop. Genom att jämföra genaktivitet i skadade och kontrollhjärtan identifierade forskarna fler än hundra sådana proteiner vars nivåer förändrades efter skada. Många var kopplade till blodkärlsbildning och svar på låg syrehalt, två processer som är centrala för hjärtats återhämtning. Ett protein, LMNA, stack ut eftersom dess nivåer tydligt följde redigeringen av ett specifikt RNA från genen Atp6v1h, som hjälper till att reglera en cellulär pump kopplad till mTOR-signalering. Den splitsade formen av detta RNA var vanligare i skadade hjärtan, vilket tyder på att LMNA kan bidra till att finjustera energisensorn under stressen av reperfusion.
Fördjupning på nyckelgener och bekräftelse i djur
Författarna lyfte fram flera gener vars redigerade RNA-former kan skjuta hjärtceller mot överlevnad eller skada. Till exempel producerade en hypoxiresponsiv faktor kallad Eif4e2, en inflammationsrelaterad regulator Traf6, insulinreceptorn Insr och en stresskänslig regulator Nr4a1 alla RNA-varianter som var vanligare efter skada. Andra, såsom Map4k4, visade minskad användning av vissa splitsformer. För att testa om dessa RNA-förskjutningar var verkliga utöver datoranalysen skapade teamet sin egen musmodell för reperfusionsskada. De bekräftade att många av de förutspådda genvarianterna och RNA-bindande proteinerna förändrades i samma riktning både på RNA- och proteinnivå, vilket stärker argumentet att detta är genuina egenskaper hos det skadade hjärtat. 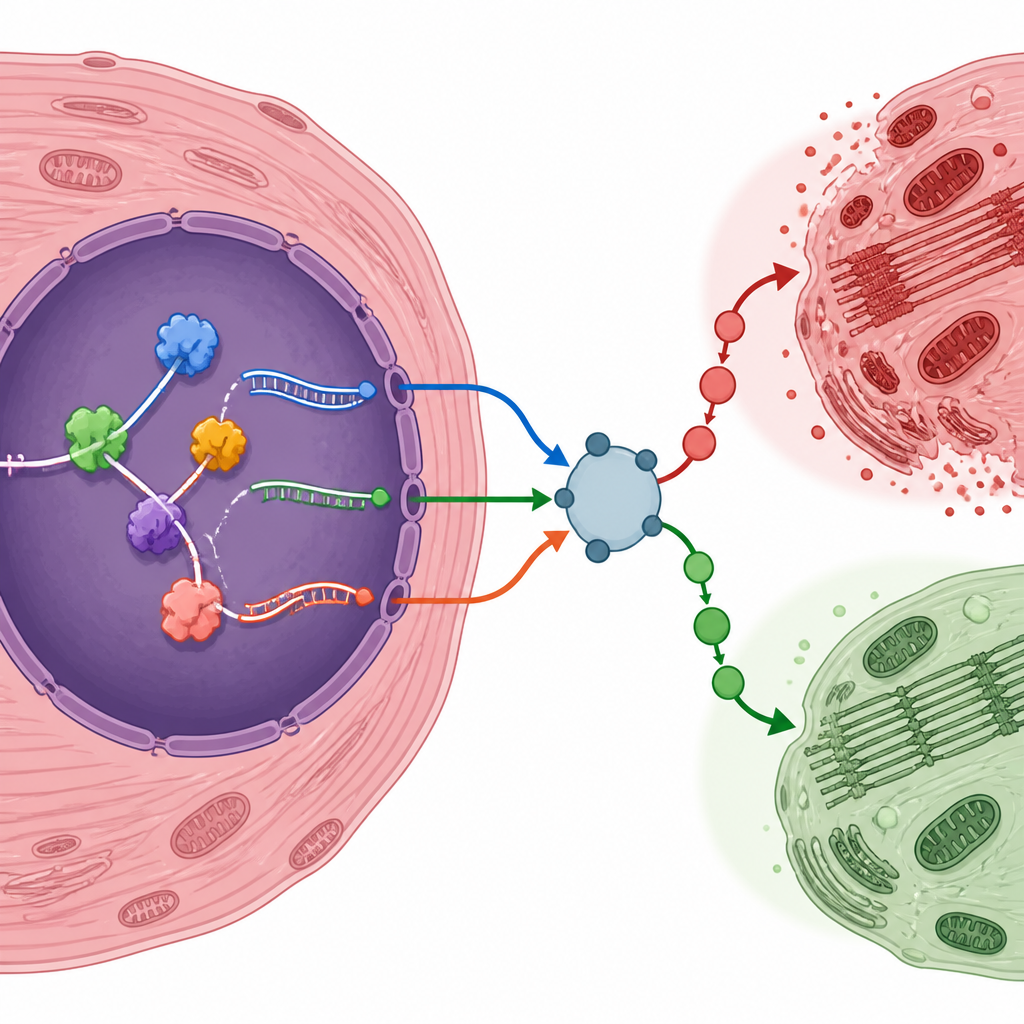
Vad detta betyder för framtida hjärtvård
Enkelt uttryckt visar detta arbete att efter att blodflödet återvänder till hjärtat rewirar cellerna snabbt sina interna meddelanden genom att skära om RNA på nya sätt, vägledda av en uppsättning regulatoriska proteiner. Dessa redigerade meddelanden finjusterar stora beslutsvägar som styr cellernas stressrespons, städning och inflammation. Även om studien är gjord i möss och ännu inte bevisar orsakssamband, kartlägger den ett nätverk av potentiella RNA-brytningar och deras styrande faktorer som kan avgöra hur mycket bestående skada som följer en hjärtinfarkt. Med tiden skulle behandlingar som varsamt justerar RNA-bindande proteiner eller specifika splitsmönster kunna komplettera nuvarande terapier och erbjuda ett mer precist sätt att skydda hjärtat när blodtillförseln återställs.
Citering: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Nyckelord: myokardial ischemi-reperfusionsskada, alternativ splitsning, RNA-bindande proteiner, mTOR-vägen, MAPK-signalering