Clear Sky Science · fr
Analyse complète des épissages alternatifs aberrants et des régulateurs protéines liant l'ARN associés à la lésion de reperfusion myocardique chez la souris
Pourquoi la réouverture du cœur peut encore l'endommager
Lorsqu'une personne fait une crise cardiaque, les médecins s'efforcent de rouvrir rapidement l'artère bouchée et de rétablir le flux sanguin. Pourtant, cette étape salvatrice peut aussi blesser le cœur dans une vague retardée de dommages appelée lésion de reperfusion. Cette étude chez la souris examine en profondeur les cellules cardiaques comment de petits messages ARN sont découpés et modifiés quand le flux sanguin revient, et comment ces changements peuvent aggraver ou atténuer les lésions. Comprendre ce niveau de contrôle caché pourrait ouvrir de nouvelles voies pour protéger le cœur après une crise cardiaque.
Des messages cachés à l'intérieur des cellules cardiaques
Chaque cellule utilise l'ARN comme copie de travail de l'information génétique. Avant d'être utilisés pour fabriquer des protéines, ces messages ARN peuvent être découpés et recollés de différentes façons, un processus connu sous le nom d'épissage alternatif. Cela signifie qu'un seul gène peut donner plusieurs versions protéiques aux effets distincts. Les auteurs se sont demandé comment ce processus d'édition changeait dans les cœurs de souris exposés à une occlusion contrôlée puis à la réouverture d'une artère coronaire majeure, un modèle standard d'infarctus suivi d'un traitement. Ils ont réanalysé un jeu de données de séquençage ARN existant comparant les tissus cardiaques de souris lésées et de témoins opérés fictivement.
Vastes changements d'édition de l'ARN après la lésion
L'équipe a constaté que la lésion de reperfusion s'accompagnait de changements étendus des schémas d'édition de l'ARN à l'échelle du génome. Ils ont détecté des centaines d'événements d'épissage dont l'utilisation différait entre les cœurs sains et lésés, en particulier à l'extrémité initiale des segments d'ARN. Beaucoup des gènes affectés appartenaient à des voies de signalisation cellulaires importantes qui déterminent si les cellules du muscle cardiaque croissent, recyclent leurs composants ou s'autodétruisent. En particulier, des gènes des voies mTOR et MAPK, qui contribuent au contrôle du métabolisme cellulaire, des réponses au stress et de l'inflammation, montraient de fortes modifications dans la manière dont leur ARN était découpé et assemblé. 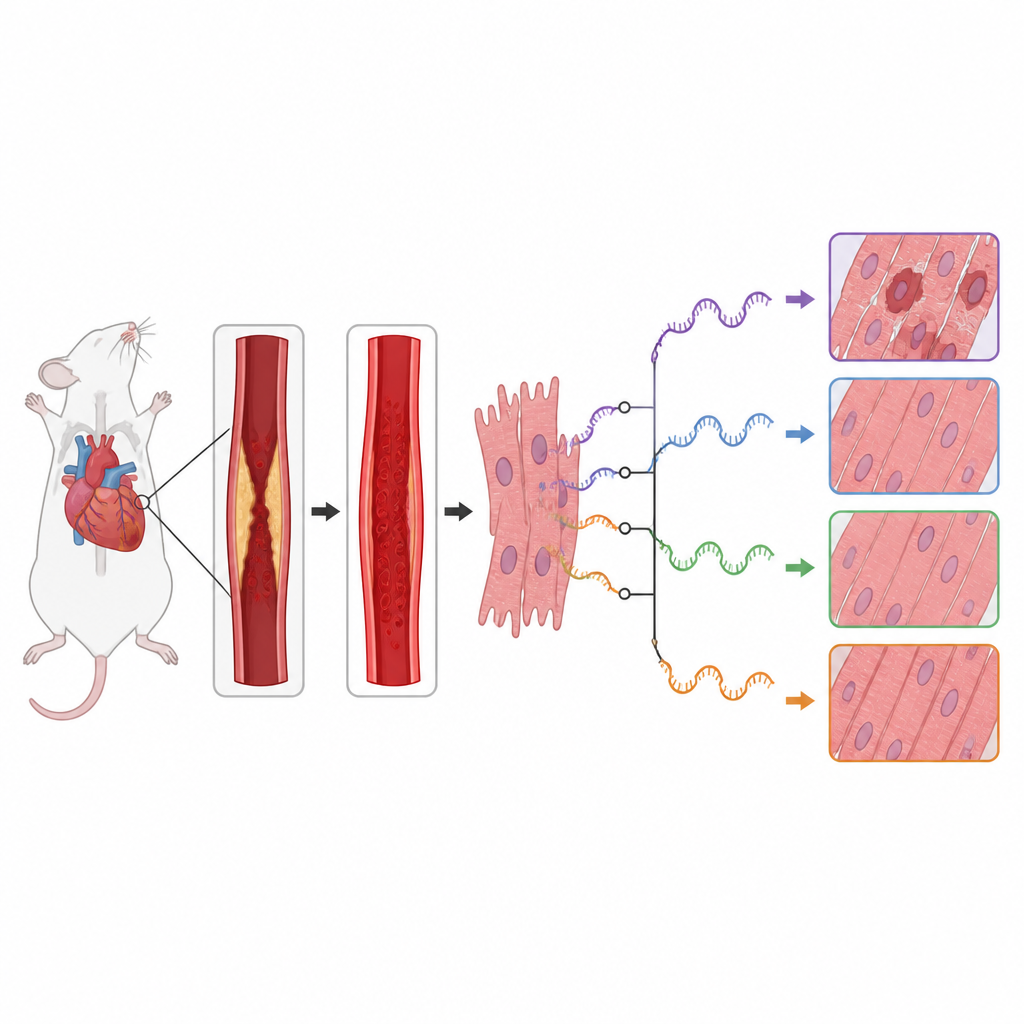
Des protéines qui orientent le découpage de l'ARN
Les protéines liant l'ARN agissent comme des contrôleurs de circulation qui décident où chaque ARN est découpé et rabouté. En comparant l'activité génique dans les cœurs lésés et témoins, les chercheurs ont identifié plus d'une centaine de ces protéines dont les niveaux changeaient après la lésion. Beaucoup étaient liées à la croissance des vaisseaux sanguins et aux réponses à l'hypoxie, deux processus centraux pour la récupération cardiaque. Une protéine, LMNA, s'est distinguée car ses niveaux suivaient de près l'édition d'un ARN spécifique d'un gène appelé Atp6v1h, qui participe à la régulation d'une pompe cellulaire liée à la signalisation mTOR. La forme épissée de cet ARN était plus fréquente dans les cœurs lésés, suggérant que LMNA pourrait aider à ajuster la détection de l'énergie pendant le stress de la reperfusion.
Zoom sur des gènes clés et validation in vivo
Les auteurs ont mis en évidence plusieurs gènes dont les formes ARN éditées pourraient orienter les cellules cardiaques vers la survie ou la lésion. Par exemple, un facteur réactif à l'hypoxie appelé Eif4e2, un régulateur lié à l'inflammation Traf6, le récepteur de l'insuline Insr, et un régulateur sensible au stress Nr4a1 produisaient tous des variantes d'ARN plus fréquentes après la lésion. D'autres, comme Map4k4, montraient une diminution de l'utilisation de formes d'épissage particulières. Pour vérifier que ces changements d'ARN existaient au-delà de l'analyse informatique, l'équipe a créé son propre modèle murin de lésion de reperfusion. Ils ont confirmé que de nombreuses variantes géniques prédites et protéines liant l'ARN changeaient dans le même sens aux niveaux ARN et protéique, renforçant l'idée qu'il s'agit de caractéristiques réelles du cœur lésé. 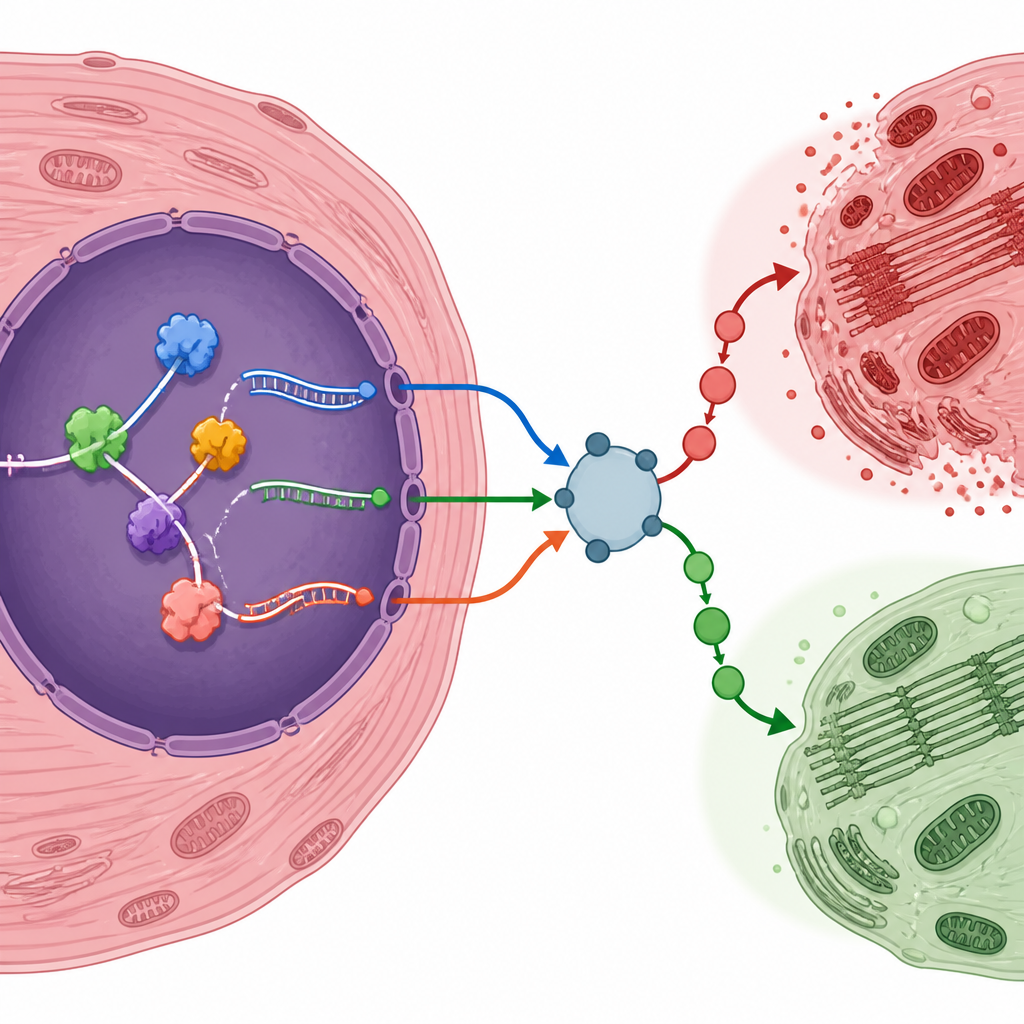
Ce que cela signifie pour les soins cardiaques futurs
En termes simples, ce travail montre qu'après le rétablissement du flux sanguin, les cellules réorganisent rapidement leurs messages internes en recoupant l'ARN de nouvelles manières, guidées par un ensemble de protéines régulatrices. Ces messages édités modulent des voies décisionnelles majeures qui gouvernent le stress cellulaire, le nettoyage et l'inflammation. Bien que l'étude ait été réalisée chez la souris et ne démontre pas encore la causalité, elle cartographie un réseau de commutateurs ARN candidats et de leurs contrôleurs susceptibles d'influencer l'étendue des lésions permanentes après un infarctus. À terme, des thérapies visant à ajuster en douceur les protéines liant l'ARN ou des schémas d'épissage spécifiques pourraient compléter les traitements actuels, offrant une manière plus précise de protéger le cœur lorsque son apport sanguin est rétabli.
Citation: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Mots-clés: lésion de reperfusion myocardique, épissage alternatif, protéines liant l'ARN, voie mTOR, signalisation MAPK