Clear Sky Science · pl
Kompleksowa analiza zaburzonego alternatywnego składania RNA i regulatorów białek wiążących RNA związanych z niedokrwienno-reperfuzjnym uszkodzeniem mięśnia sercowego u myszy
Dlaczego przywrócenie przepływu krwi może nadal szkodzić sercu
Gdy ktoś ma zawał serca, lekarze pośpiesznie udrażniają zablokowaną tętnicę i przywracają przepływ krwi. Ten ratujący życie zabieg może jednak wywołać opóźnioną falę uszkodzeń zwaną reperfuzjnym uszkodzeniem serca. W tym badaniu na myszach przyjrzano się dogłębnie komórkom serca, jak drobne komunikaty RNA są cięte i edytowane po powrocie przepływu krwi oraz jak te zmiany mogą nasilać lub łagodzić szkody. Zrozumienie tej ukrytej warstwy kontroli może otworzyć nowe drogi ochrony serca po zawale.
Ukryte wiadomości w komórkach serca
Każda komórka używa RNA jako roboczej kopii informacji genetycznej. Zanim te wiadomości RNA zostaną użyte do produkcji białek, mogą być cięte i składane na różne sposoby, proces znany jako alternatywne składanie. Oznacza to, że jeden gen może dawać kilka wersji białka o odmiennych funkcjach. Autorzy zapytali, jak ten proces edycji zmienia się w sercach myszy poddanych kontrolowanemu zablokowaniu i ponownemu udrożnieniu kluczowej tętnicy wieńcowej — standardowego modelu zawału z leczeniem. Ponownie przeanalizowali istniejący zestaw danych z sekwencjonowania RNA porównujący tkankę serca od myszy z urazem i od operowanych bez urazu (sham).
Szerokie przesunięcia w edycji RNA po urazie
Zespół stwierdził, że reperfuzjne uszkodzenie wiązało się z szerokimi zmianami wzorców edycji RNA w całym genomie. Wykryto setki zdarzeń składania, których użycie różniło się między zdrowymi a uszkodzonymi sercami, szczególnie na końcu początkowym segmentów RNA. Wiele dotkniętych genów należało do istotnych szlaków sygnalizacyjnych komórek, które decydują o tym, czy kardiomiocyty rosną, prowadzą recykling własnych składników lub przechodzą samozniszczenie. W szczególności geny w szlakach mTOR i MAPK, które pomagają kontrolować metabolizm komórek, reakcje na stres i zapalenie, wykazały silne zmiany w sposobie cięcia i składania ich RNA. 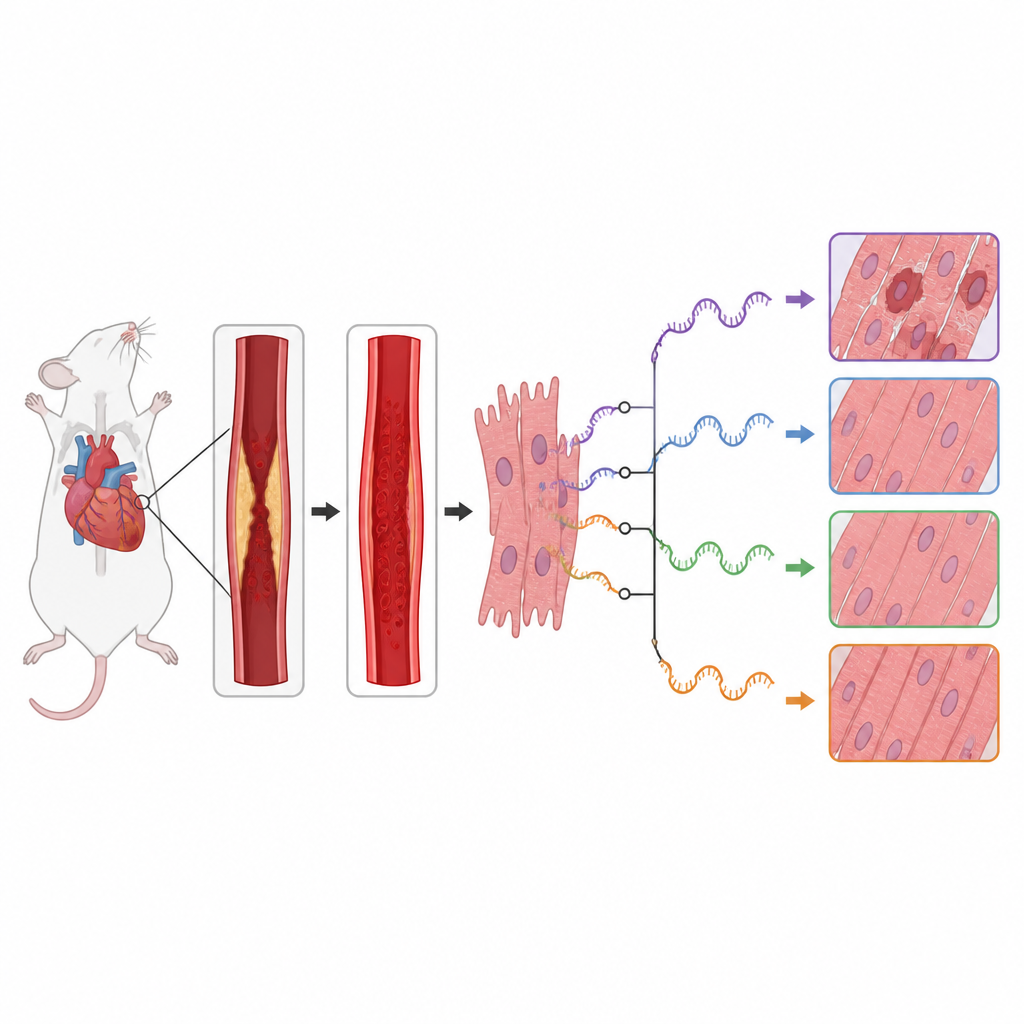
Białka kierujące cięciem RNA
Białka wiążące RNA działają jak kontrolerzy ruchu, którzy decydują, gdzie każde RNA jest przecinane i składane. Porównując aktywność genów w sercach z urazem i kontrolnych, badacze zidentyfikowali ponad sto takich białek, których poziomy zmieniły się po urazie. Wiele z nich było powiązanych z rozwojem naczyń krwionośnych i reakcjami na niedotlenienie — dwoma procesami kluczowymi dla regeneracji serca. Jedno białko, LMNA, wyróżniało się, ponieważ jego poziomy ściśle korelowały z edycją konkretnego RNA z genu Atp6v1h, który pomaga regulować pompkę komórkową związaną z sygnalizacją mTOR. Forma tego RNA powstała przez składanie była częstsza w sercach po urazie, co sugeruje, że LMNA może pomagać w precyzyjnym dostrajaniu wykrywania energii podczas stresu reperfuzji.
Skupienie na kluczowych genach i potwierdzenie in vivo
Autorzy wyróżnili kilka genów, których edytowane formy RNA mogą przechylić losy kardiomiocytów w stronę przeżycia lub uszkodzenia. Na przykład czynnik odpowiadający za odpowiedź na niedotlenienie Eif4e2, regulator związany z zapaleniem Traf6, receptor insuliny Insr oraz regulator wrażliwy na stres Nr4a1 wytwarzały warianty RNA częściej występujące po urazie. Inne, takie jak Map4k4, wykazywały zmniejszone użycie określonych form składania. Aby sprawdzić, czy te przesunięcia RNA są rzeczywiste poza analizą komputerową, zespół stworzył własny model reperfuzyjnego urazu u myszy. Potwierdzili, że wiele przewidywanych wariantów genów i białek wiążących RNA zmieniło się w tym samym kierunku zarówno na poziomie RNA, jak i białka, co wzmacnia argument, że są to autentyczne cechy uszkodzonego serca. 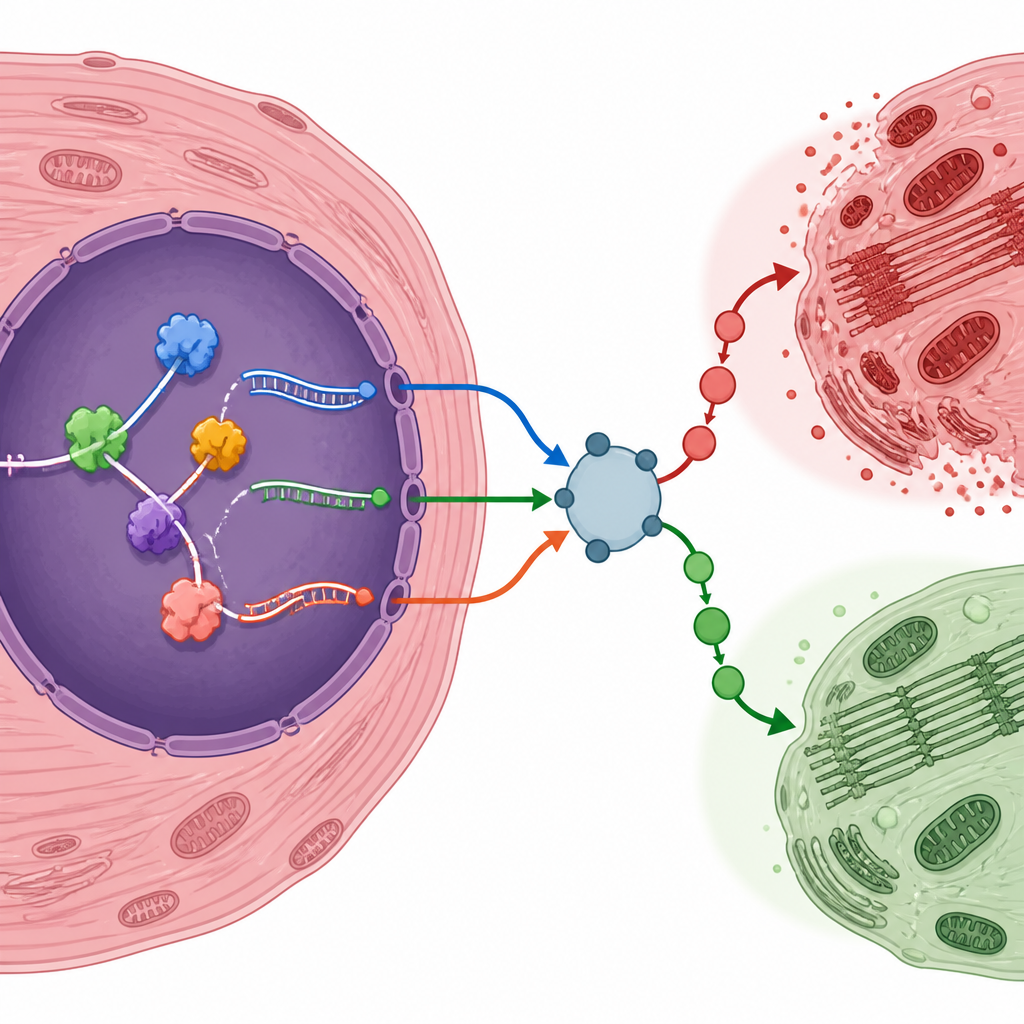
Co to oznacza dla przyszłej opieki nad sercem
Mówiąc prosto, ta praca pokazuje, że po przywróceniu przepływu krwi komórki serca szybko przełączają swoje wewnętrzne komunikaty przez ponowne cięcie RNA w nowe sposoby, prowadzone przez zestaw regulatorowych białek. Te edytowane komunikaty modyfikują główne ścieżki decyzyjne rządzące stresem komórkowym, oczyszczaniem i stanem zapalnym. Choć badanie przeprowadzono na myszach i nie dowodzi jeszcze związku przyczynowo-skutkowego, mapuje sieć kandydackich przełączników RNA i ich kontrolerów, które mogą kształtować zakres trwałego uszkodzenia po zawale. Z czasem terapie delikatnie modulujące białka wiążące RNA lub specyficzne wzorce składania mogłyby uzupełniać obecne leczenie, oferując precyzyjniejszy sposób osłony serca po przywróceniu jego ukrwienia.
Cytowanie: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Słowa kluczowe: niedokrwienno-reperfuzjne uszkodzenie mięśnia sercowego, alternatywne składanie, białka wiążące RNA, szlak mTOR, sygnalizacja MAPK