Clear Sky Science · ru
Комплексный анализ нарушенного альтернативного сплайсинга и регуляторов белков, связывающих РНК, связанных с ишемически‑реперфузионным повреждением миокарда у мышей
Почему восстановление кровотока может повредить сердце
Когда у человека происходит сердечный приступ, врачи спешат восстановить проходимость закупоренной артерии и вернуть кровоток. Однако этот жизненно важный шаг может вызвать отложенную волну повреждений — реперфузионное повреждение. В этом исследовании на мышах подробно изучают, что происходит внутри клеток сердца с небольшими РНК‑сообщениями при возвращении кровотока, и как эти изменения могут усугублять или смягчать ущерб. Понимание этого скрытого уровня контроля может открыть новые пути защиты сердца после инфаркта.
Скрытые сообщения внутри клеток сердца
Каждая клетка использует РНК как рабочую копию генетической информации. Прежде чем эти РНК‑сообщения будут использованы для синтеза белков, их можно разрезать и соединить по‑разному — процесс, известный как альтернативный сплайсинг. Это означает, что один ген может порождать несколько вариантов белка с разными функциями. Авторы спросили, как этот процесс редактирования меняется в мышином сердце при контролируемой блокаде и восстановлении важной коронарной артерии — стандартной модели инфаркта с последующим лечением. Они переанализировали существующий набор данных РНК‑секвенирования, сравнивая ткани сердца у повреждённых мышей и у контрольных животных с ложной операцией.
Широкие сдвиги в редактировании РНК после повреждения
Исследователи обнаружили, что реперфузионное повреждение сопровождается масштабными изменениями в схемах сплайсинга по всему геному. Они выявили сотни событий сплайсинга, использование которых отличалось между здоровыми и повреждёнными сердцами, особенно на начальном (5') конце транскриптов. Многие поражённые гены относятся к важным сигнальным путям, которые решают, будут ли кардиомиоциты расти, утилизировать компоненты или инициировать клеточную гибель. В частности, гены путей mTOR и MAPK, регулирующие метаболизм клетки, реакции на стресс и воспаление, продемонстрировали сильные изменения в способах разрезания и сборки их РНК. 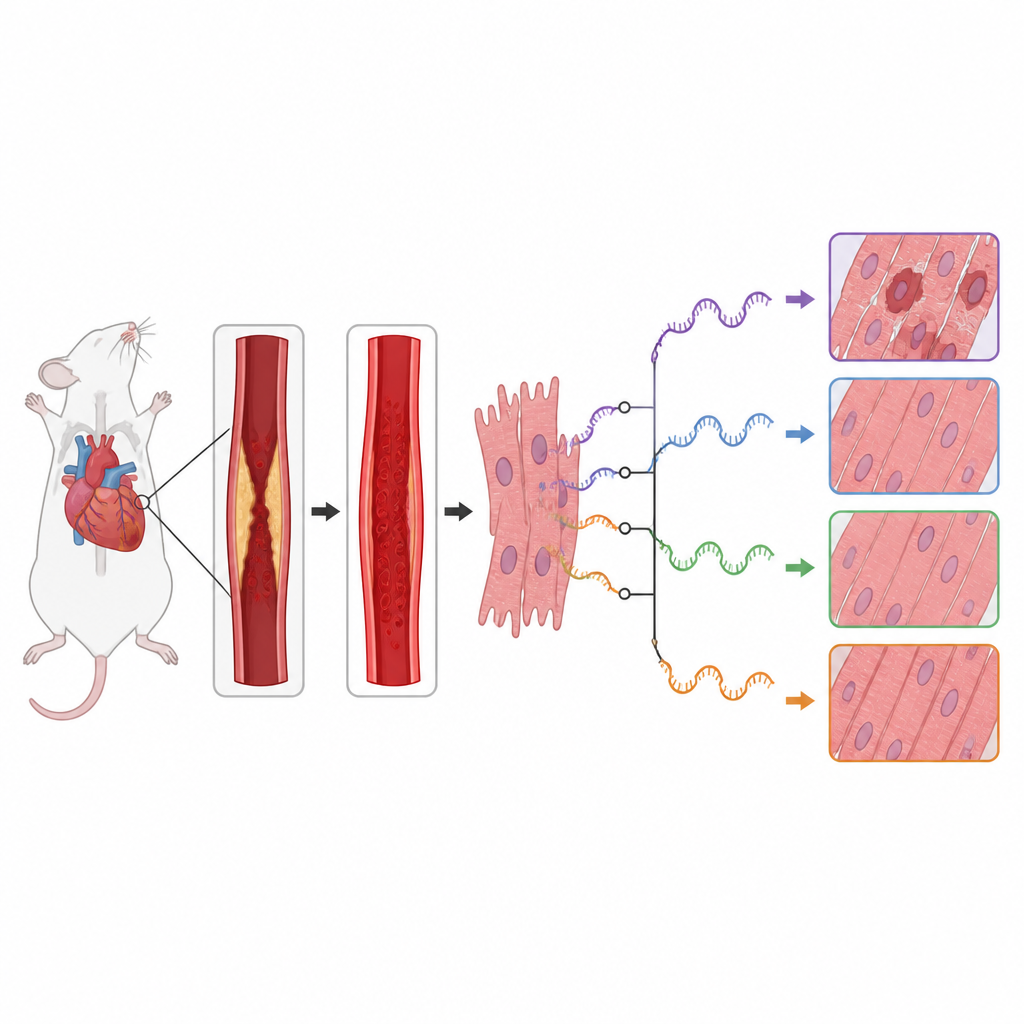
Белки, направляющие разрезание РНК
Белки, связывающие РНК, действуют как регуляторы‑«светофоры», определяя, где именно РНК будет разрезана и сшита. Сравнив экспрессию генов в повреждённых и контрольных сердцах, исследователи выделили более сотни таких белков, уровни которых менялись после травмы. Многие из них связаны с ростом сосудов и ответами на гипоксию — двумя процессами, центральными для восстановления сердца. Один белок, LMNA, выделялся тем, что его уровни тесно коррелировали с редактированием конкретной РНК от гена Atp6v1h, участвующего в регуляции клеточного насоса, связанного с mTOR‑сигналингом. Сплайс‑вариант этой РНК был более распространён в повреждённых сердцах, что наводит на мысль, что LMNA может участвовать в точной настройке энергоощущения во время стресса реперфузии.
Фокус на ключевых генах и подтверждение в животных
Авторы выделили несколько генов, чьи отредактированные РНК‑варианты могут смещать баланс кардиомиоцитов в сторону выживания или повреждения. Например, фактор, реагирующий на гипоксию Eif4e2, регулятор воспаления Traf6, инсулиновый рецептор Insr и стресс‑чувствительный регулятор Nr4a1 — все они давали РНК‑варианты, чаще встречающиеся после повреждения. Другие, такие как Map4k4, демонстрировали снижение использования определённых сплайс‑форм. Чтобы проверить, реальны ли эти сдвиги за пределами вычислительного анализа, команда создала собственную модель реперфузионного повреждения у мышей. Они подтвердили, что многие предсказанные варианты генов и белки, связывающие РНК, менялись в том же направлении как на уровне РНК, так и на уровне белка, что укрепляет аргумент в пользу того, что это подлинные признаки повреждённого сердца. 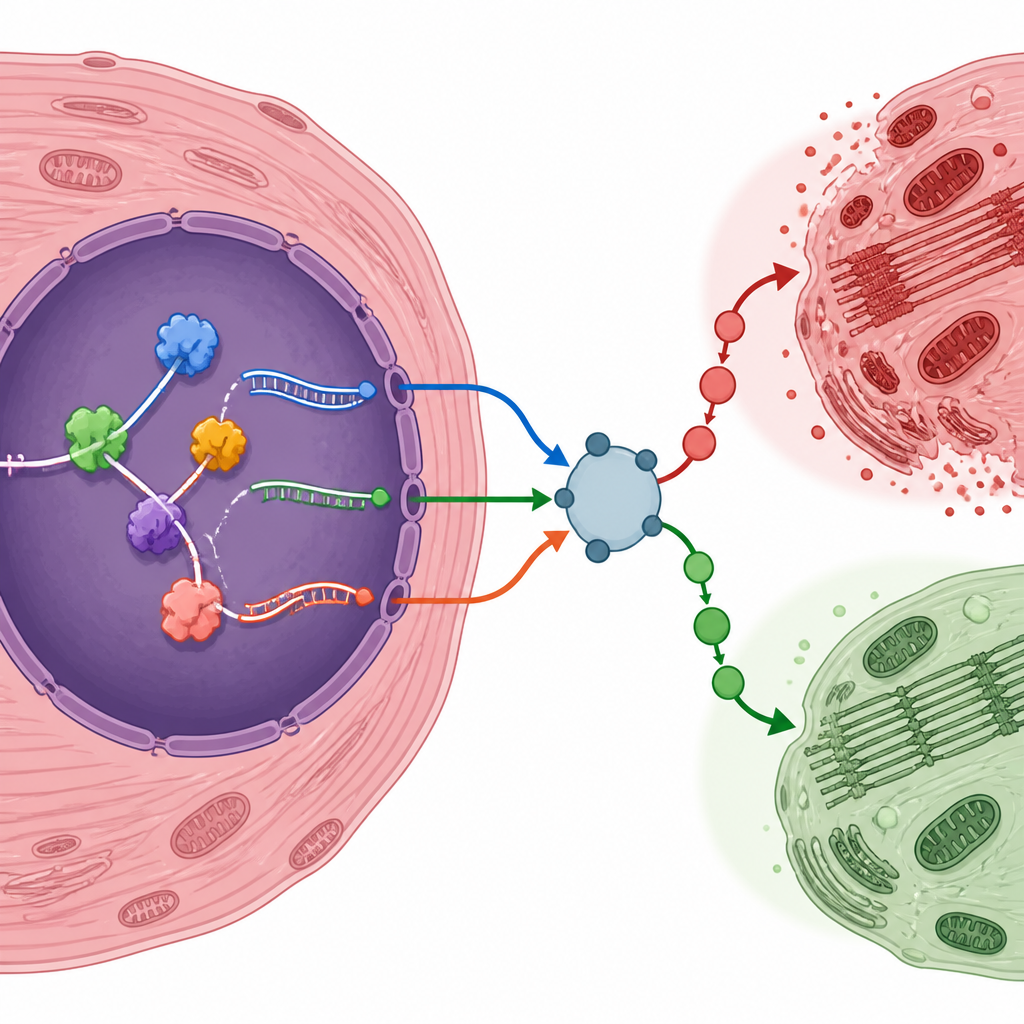
Что это значит для будущей помощи сердцу
Проще говоря, работа показывает, что после восстановления кровотока клетки сердца быстро перестраивают свои внутренние сообщения, перережая РНК новыми способами под руководством набора регуляторных белков. Эти отредактированные сообщения модифицируют крупные «решающие» пути, управляющие клеточным стрессом, механизмами утилизации и воспалением. Хотя исследование проведено на мышах и пока не доказывает причинно‑следственной связи, оно картирует сеть кандидатов — РНК‑переключателей и их контролёров — которые могут определять степень необратимого ущерба после инфаркта. Со временем терапии, мягко корректирующие активность белков, связывающих РНК, или конкретные схемы сплайсинга, могли бы дополнить существующие методы и предложить более точный способ защиты сердца при восстановлении его кровоснабжения.
Цитирование: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Ключевые слова: ишемически‑реперфузионное повреждение миокарда, альтернативный сплайсинг, белки, связывающие РНК, путь mTOR, MAPK‑сигнальный путь