Clear Sky Science · nl
Uitgebreide analyse van afwijkend alternatief splicen en RNA-bindende eiwitten geassocieerd met myocardiale ischemie-reperfusie schade bij muizen
Waarom het opnieuw op gang brengen van de bloedtoevoer nog steeds schadelijk kan zijn voor het hart
Wanneer iemand een hartaanval krijgt, haasten artsen zich om de geblokkeerde arterie te openen en de bloedstroom te herstellen. Toch kan deze levensreddende ingreep in een vertraagde golf van schade ook het hart verwonden, zogenaamde reperfusieschade. Deze studie bij muizen kijkt diep in hartcellen naar hoe kleine RNA-berichten worden geknipt en bewerkt wanneer de bloedstroom terugkeert, en hoe die veranderingen de schade mogelijk kunnen verergeren of verminderen. Begrijpen van deze verborgen controlelaag kan nieuwe wegen openen om het hart na een hartaanval te beschermen.
Verborgen boodschappen in hartcellen
Elke cel gebruikt RNA als een werkkopie van de genetische informatie. Voordat deze RNA-berichten worden gebruikt om eiwitten te maken, kunnen ze op verschillende manieren worden geknipt en opnieuw samengevoegd, een proces dat alternatief splicen wordt genoemd. Dat betekent dat één gen meerdere eiwitversies kan opleveren met verschillende effecten. De auteurs vroegen zich af hoe dit bewerkingsproces verandert in muizenharten die werden blootgesteld aan een gecontroleerde blokkade en heropening van een belangrijke kransslagader, een standaardmodel van een hartaanval gevolgd door behandeling. Zij heranalyseerden een bestaand RNA-sequencing dataset waarin hartweefsel van beschadigde muizen werd vergeleken met sham-geopereerde controles.
Grote verschuivingen in RNA-bewerking na schade
Het team vond dat reperfusieschade gepaard ging met ingrijpende verschuivingen in RNA-bewerkingspatronen over het hele genoom. Ze detecteerden honderden splicing-gebeurtenissen waarvan het gebruik verschilde tussen gezonde en beschadigde harten, vooral aan het begin van RNA-segmenten. Veel van de getroffen genen behoorden tot belangrijke cellulaire signaalroutes die bepalen of hartspiercellen groeien, hun componenten recyclen of zelf-destructie inzetten. In het bijzonder toonden genen in de mTOR- en MAPK-routes, die helpen bij het beheersen van celmetabolisme, stressreacties en ontsteking, sterke veranderingen in hoe hun RNA werd geknipt en samengesteld. 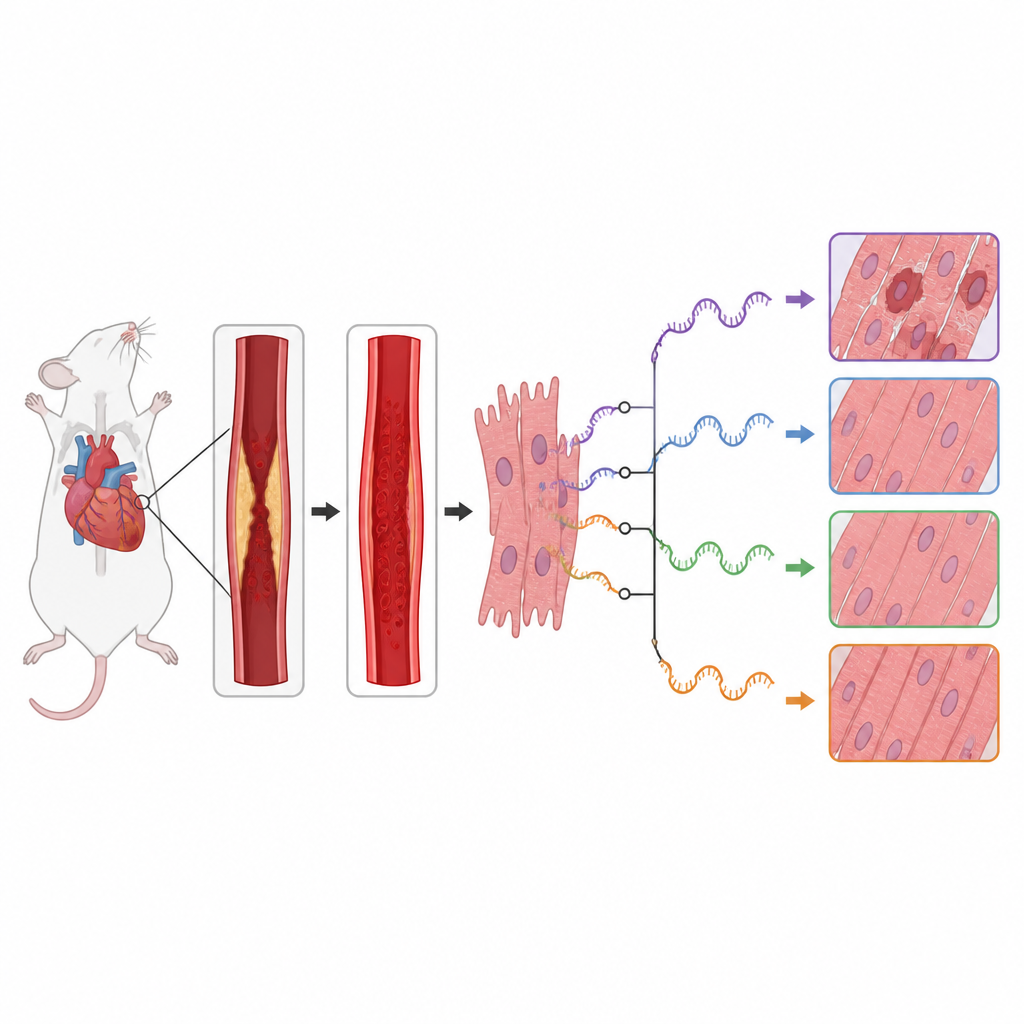
Proteïnen die het RNA-knippen sturen
RNA-bindende eiwitten fungeren als verkeersleiders die beslissen waar elk RNA wordt doorgesneden en vastgenaaid. Door genexpressie in beschadigde en controle-harten te vergelijken, identificeerden de onderzoekers meer dan honderd zulke eiwitten waarvan de niveaus na schade veranderden. Velen waren gekoppeld aan vaatgroei en reacties op zuurstoftekort, twee processen die centraal staan in hartherstel. Eén eiwit, LMNA, sprong eruit omdat zijn niveaus nauw overeenkwamen met de bewerking van een specifiek RNA van een gen genaamd Atp6v1h, dat helpt een cellulair pompje te regelen dat verbonden is met mTOR-signaalgeving. De gesplicede vorm van dit RNA kwam vaker voor in beschadigde harten, wat suggereert dat LMNA mogelijk helpt de energiewaarneming fijn af te stemmen tijdens de stress van reperfusie.
Inzoomen op sleutelgenen en bevestigen in dieren
De auteurs belichtten meerdere genen waarvan de bewerkte RNA-vormen hartcellen mogelijk in de richting van overleving of schade duwen. Bijvoorbeeld een hypoxie-responsief factor genaamd Eif4e2, een ontstekingsgerelateerde regulator Traf6, de insuline-receptor Insr en een stressgevoelige regulator Nr4a1 produceerden alle RNA-varianten die vaker voorkwamen na schade. Anderen, zoals Map4k4, vertoonden een verminderd gebruik van specifieke splice-vormen. Om te testen of deze RNA-verschuivingen verder reikten dan computeranalyse, creëerde het team hun eigen muismodel van reperfusieschade. Zij bevestigden dat veel van de voorspelde genvarianten en RNA-bindende eiwitten in dezelfde richting veranderden op zowel RNA- als proteïneniveau, wat de stelling versterkt dat dit echte kenmerken zijn van het beschadigde hart. 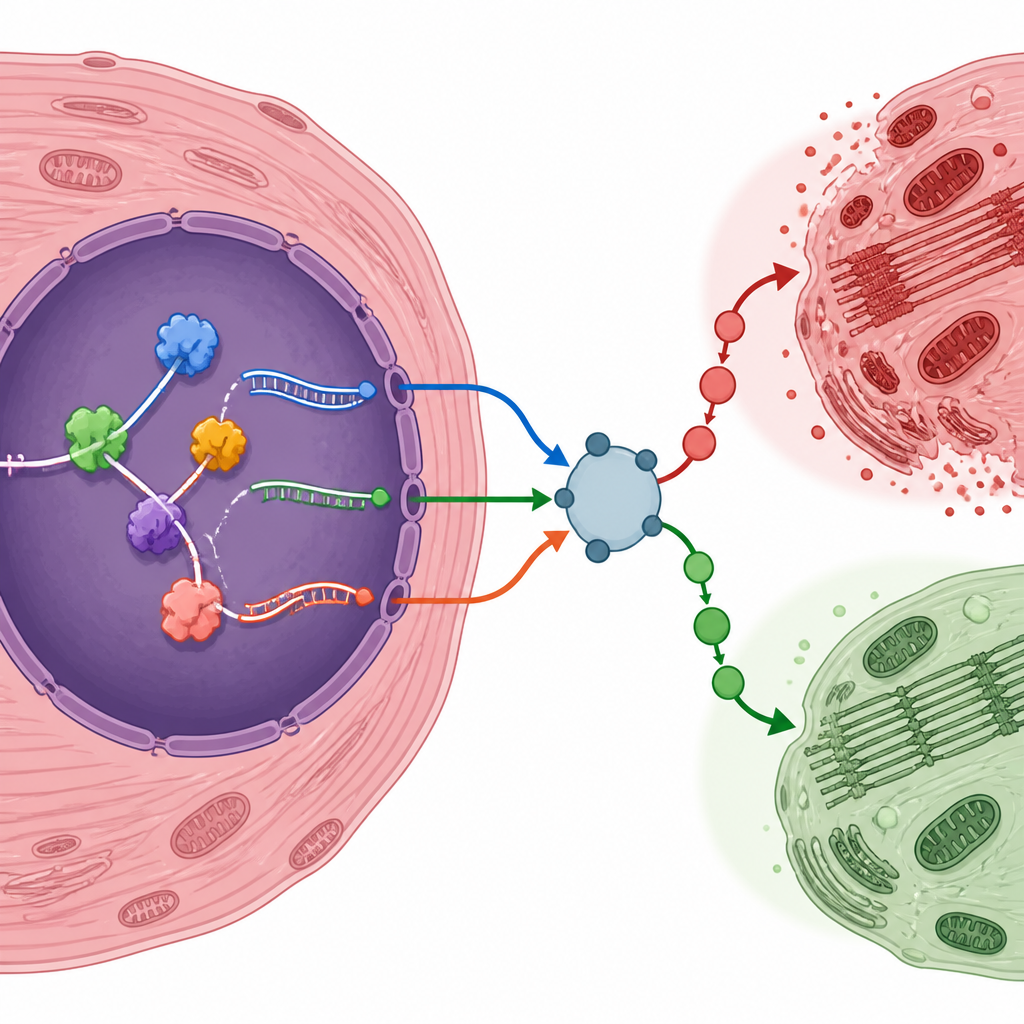
Wat dit betekent voor toekomstige hartzorg
Kort gezegd toont dit werk aan dat cellen, nadat de bloedstroom naar het hart is hersteld, snel hun interne boodschappen opnieuw bedraden door RNA op nieuwe manieren te knippen, gestuurd door een set regulatorische eiwitten. Deze bewerkte boodschappen verfijnen grote besluitvormingsroutes die celstress, opruiming en ontsteking beheersen. Hoewel de studie in muizen is uitgevoerd en nog geen oorzaak-gevolgrelaties bewijst, brengt zij een netwerk in kaart van kandidaat-RNA-schakelaars en hun regisseurs die kunnen bepalen hoeveel blijvende schade volgt op een hartaanval. Op termijn zouden therapieën die RNA-bindende eiwitten of specifieke splice-patronen voorzichtig aanpassen, bestaande behandelingen kunnen aanvullen en een preciezere manier bieden om het hart te beschermen wanneer de bloedtoevoer is hersteld.
Bronvermelding: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Trefwoorden: myocardiale ischemie reperfusie schade, alternatief splicen, RNA-bindende eiwitten, mTOR-route, MAPK-signaleringsroute