Clear Sky Science · es
Análisis exhaustivo del splicing alternativo aberrante y los reguladores de proteínas que unen ARN asociados con la lesión por isquemia-reperfusión miocárdica en ratones
Por qué reiniciar el corazón puede seguir dañándolo
Cuando alguien sufre un infarto, los médicos se apresuran a reabrir la arteria obstruida y restaurar el flujo sanguíneo. Sin embargo, este paso que salva vidas también puede lesionar el corazón en una oleada retrasada de daño llamada lesión por reperfusión. Este estudio en ratones examina en profundidad las células cardíacas para ver cómo se cortan y editan los pequeños mensajes de ARN cuando el flujo sanguíneo regresa, y cómo esos cambios podrían empeorar o mitigar el daño. Entender esta capa oculta de control podría abrir nuevas vías para proteger el corazón tras un infarto.
Mensajes ocultos dentro de las células cardíacas
Cada célula utiliza ARN como una copia de trabajo de la información genética. Antes de que estos mensajes de ARN se usen para fabricar proteínas, pueden cortarse y reunirse de distintas maneras, un proceso conocido como splicing alternativo. Eso significa que un solo gen puede dar lugar a varias versiones de proteína con efectos distintos. Los autores preguntaron cómo cambia este proceso de edición en corazones de ratón expuestos a una obstrucción controlada y reapertura de una arteria coronaria clave, un modelo estándar de infarto seguido de tratamiento. Volvieron a analizar un conjunto de datos de secuenciación de ARN existente que comparaba tejido cardíaco de ratones lesionados con controles operados sin lesión.
Grandes cambios en la edición del ARN tras la lesión
El equipo encontró que la lesión por reperfusión iba acompañada de cambios generalizados en los patrones de splicing del ARN a lo largo del genoma. Detectaron cientos de eventos de empalme cuyo uso difería entre corazones sanos y lesionados, especialmente en el extremo inicial de los segmentos de ARN. Muchos de los genes afectados pertenecían a rutas de señalización celular importantes que deciden si las células del músculo cardíaco crecen, reciclan sus componentes o se autodestruyen. En particular, genes de las vías mTOR y MAPK, que ayudan a controlar el metabolismo celular, las respuestas al estrés y la inflamación, mostraron cambios marcados en cómo se cortaba y ensamblaba su ARN. 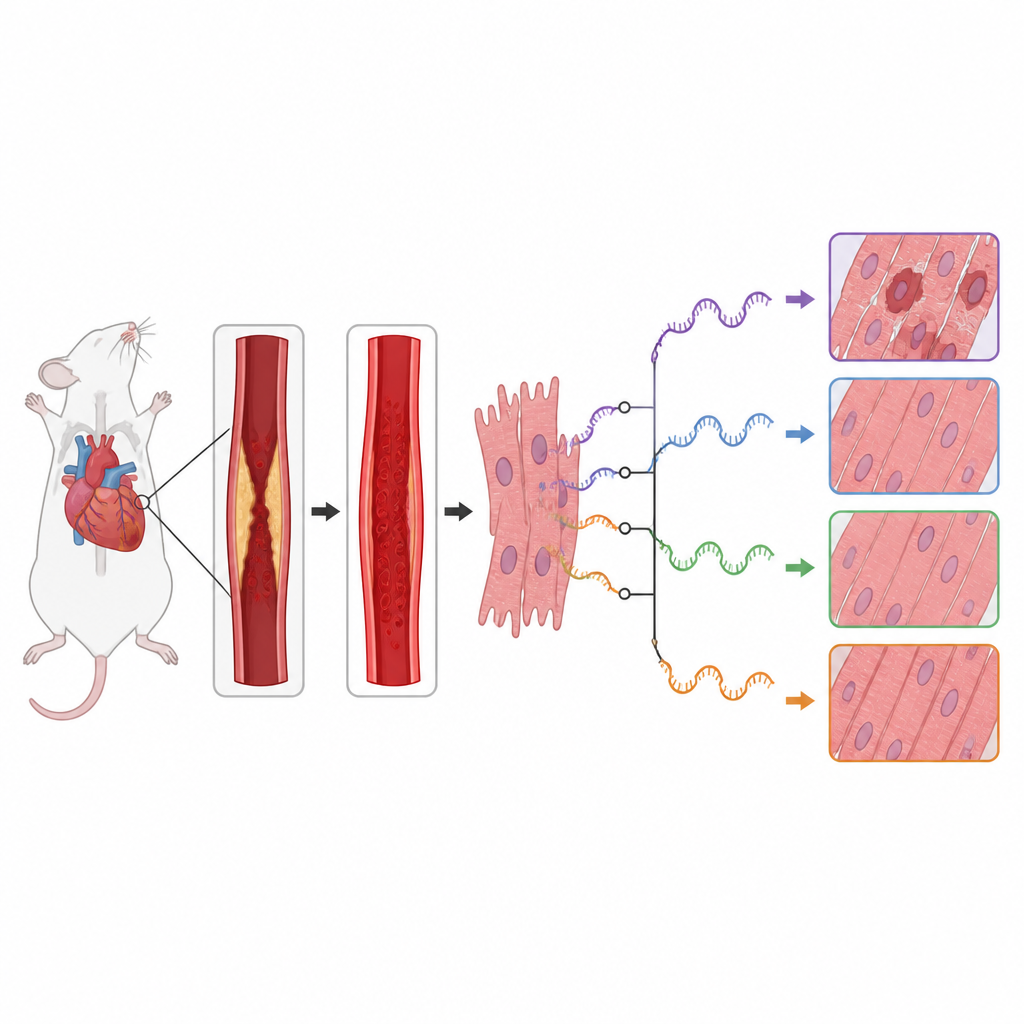
Proteínas que dirigen el corte del ARN
Las proteínas que unen ARN actúan como controladores de tráfico que deciden dónde se corta y se cose cada ARN. Al comparar la actividad génica en corazones lesionados y controles, los investigadores identificaron más de un centenar de estas proteínas cuyos niveles cambiaron tras la lesión. Muchas estaban vinculadas al crecimiento de vasos sanguíneos y a respuestas a la baja oxigenación, dos procesos centrales para la recuperación cardíaca. Una proteína, LMNA, destacó porque sus niveles seguían de cerca la edición de un ARN específico de un gen llamado Atp6v1h, que ayuda a regular una bomba celular ligada a la señalización mTOR. La forma empalmada de este ARN fue más común en corazones lesionados, lo que sugiere que LMNA podría ayudar a ajustar la detección de energía durante el estrés de la reperfusión.
Acercándose a genes clave y confirmando en animales
Los autores destacaron varios genes cuyas formas de ARN editadas podrían inclinar a las células cardíacas hacia la supervivencia o el daño. Por ejemplo, un factor sensible a la hipoxia llamado Eif4e2, un regulador relacionado con la inflamación Traf6, el receptor de insulina Insr y un regulador sensible al estrés Nr4a1 produjeron variantes de ARN más frecuentes tras la lesión. Otros, como Map4k4, mostraron un uso reducido de formas de empalme particulares. Para comprobar si estos cambios en el ARN eran reales más allá del análisis computacional, el equipo creó su propio modelo de ratón de lesión por reperfusión. Confirmaron que muchas de las variantes génicas y proteínas que unen ARN predichas cambiaron en la misma dirección tanto a nivel de ARN como de proteína, lo que refuerza la idea de que son rasgos genuinos del corazón lesionado. 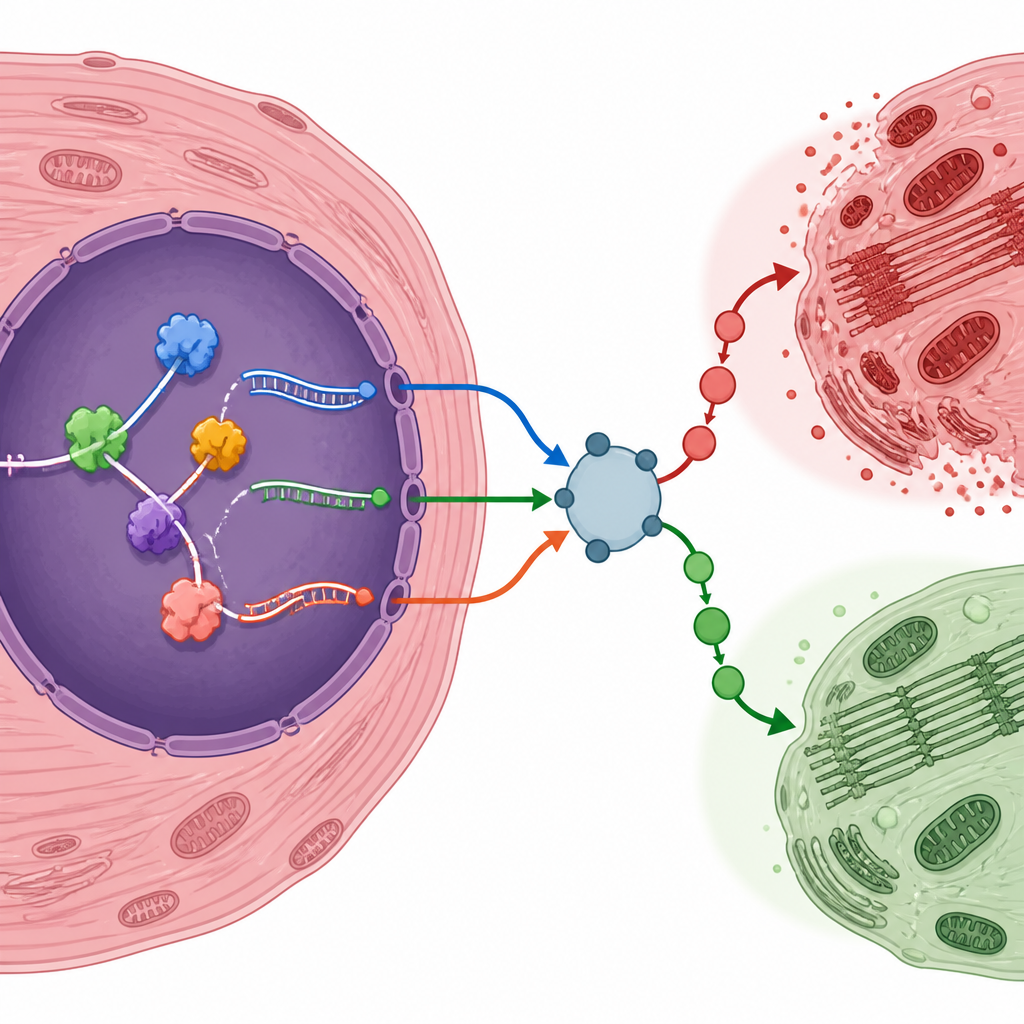
Qué significa esto para la atención cardíaca futura
En términos sencillos, este trabajo muestra que tras la restauración del flujo sanguíneo, las células reconfiguran rápidamente sus mensajes internos cortando el ARN de nuevas maneras, guiadas por un conjunto de proteínas regulatorias. Estos mensajes editados modulan vías decisorias principales que gobiernan el estrés celular, la limpieza y la inflamación. Aunque el estudio se realizó en ratones y aún no demuestra causalidad, traza una red de interruptores de ARN candidatos y sus controladores que podrían determinar cuánto daño permanente sigue a un infarto. Con el tiempo, terapias que ajusten suavemente las proteínas que unen ARN o patrones de empalme específicos podrían complementar los tratamientos actuales, ofreciendo una forma más precisa de proteger el corazón cuando se restaura su suministro sanguíneo.
Cita: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Palabras clave: lesión por isquemia-reperfusión miocárdica, splicing alternativo, proteínas que unen ARN, ruta mTOR, señalización MAPK