Clear Sky Science · he
ניתוח מקיף של שינויים חריגים בספלייסינג חלופי ומווסתי חלבוני קשירת RNA המקושרים לפגיעה איסכמית-רפיקשורפי של הלב בעכברים
למה החזרת זרימת הדם עלולה עדיין לפגוע בלב
כאשר מישהו עובר התקף לב, הרופאים ממהרים לפתוח את העורק החסום ולהשיב את זרימת הדם. עם זאת, צעד מציל חיים זה יכול גם לפגוע בלב בגל עיכוב של נזק הקרוי פגיעה רפיקשורפית. המחקר בעכברים מביט עמוק לתוך תאי הלב על האופן שבו הודעות RNA זעירות נחתכות ומעובדות כשזרימת הדם חוזרת, וכיצד שינויים אלה עשויים להחריף או להפחית את הנזק. הבנת שכבת הבקרה הנסתרת הזו עשויה לפתוח נתיבים חדשים להגנה על הלב אחרי התקף.
הודעות חסרות-מראה בתוך תאי הלב
כל תא משתמש ב‑RNA כעותק פעיל של המידע הגנטי. לפני שהודעות RNA אלה מנוצלות לייצור חלבונים, הן יכולות להיחתך ולהתחבר מחדש בדרכים שונות, תהליך המכונה ספלייסינג חלופי. משמעות הדבר היא שגן יחיד יכול להניב מספר גרסאות חלבון בעלות השפעות שונות. המחברים בדקו כיצד תהליך העריכה הזה משתנה בלבי עכברים שנחשפו לחסימה מבוקרת ולפתיחה מחודשת של עורק כלילי חשוב — מודל סטנדרטי להתקף לב ואחריו טיפול. הם ערכו ניתוח מחודש של מאגר נתוני רצף RNA קיים שהשווה רקמות לב מעכברים פגועים לעכברים בעשייה מדומה (שאם).
שינויים רחבי היקף בעריכת RNA לאחר הפגיעה
הצוות גילה כי פגיעה רפיקשורפית לוותה בשינויים נרחבים בדפוסי עריכת ה‑RNA ברחבי הגנום. הם זיהו מאות אירועי ספלייסינג שהשימוש בהם השתנה בין לבות בריאות ופגועות, במיוחד בקצוות ההתחלתיים של מקטעי ה‑RNA. רבים מהגנים המושפעים השתייכו למסלולי איתות תאיים חשובים שמחליטים אם תאי שריר הלב יגדלו, ימחזרו מרכיבים פנימיים או ייכנסו למות מתוכנן. בפרט, גנים במסלולי mTOR ו‑MAPK, המסייעים לשלוט במטבוליזם התא, בתגובת סטרס ובדלקת, הראו שינויים חזקים באופן שבו ה‑RNA שלהם נחתך והרכבו. 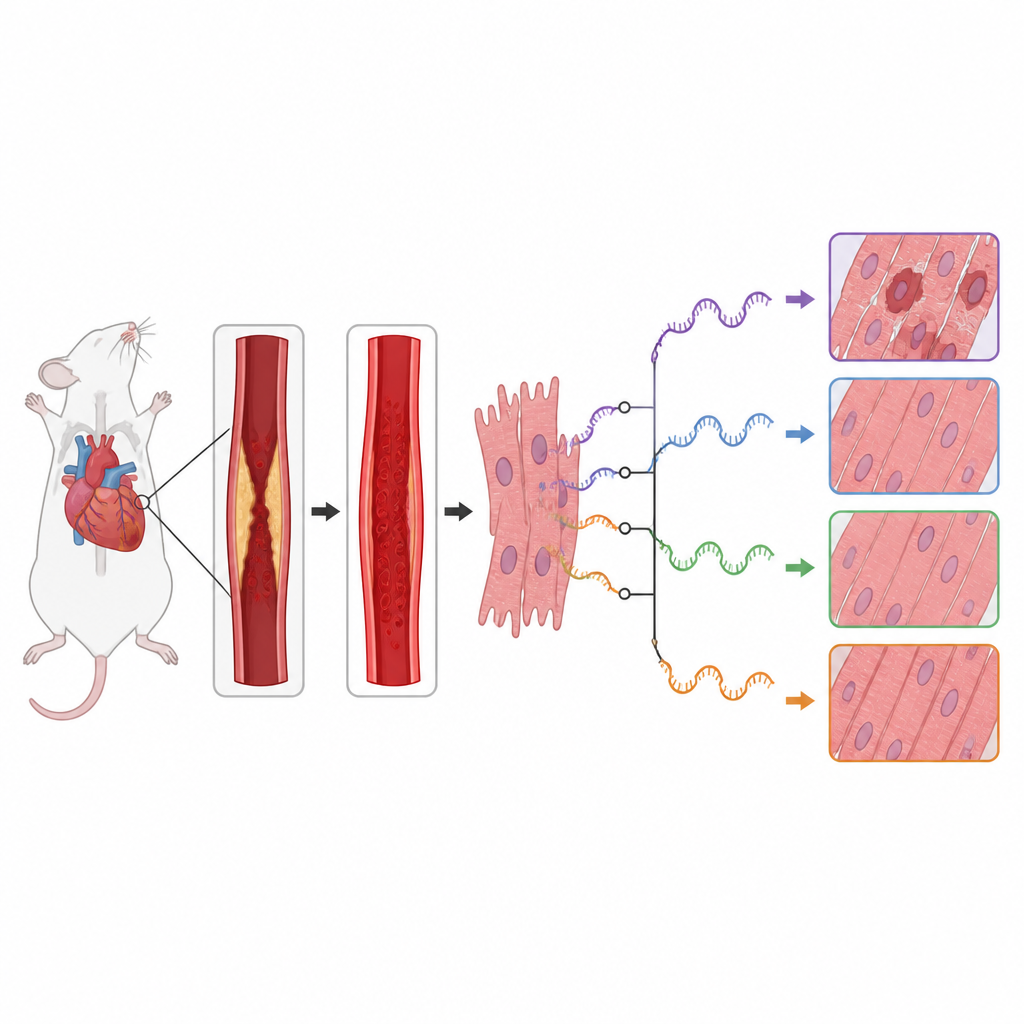
חלבונים המכוונים את חיתוך ה‑RNA
חלבוני קשירת RNA פועלים כבוררי תנועה שמחליטים היכן כל RNA ייחתך ויתפרק. בהשוואת פעילות הגנים בלב פגוע ובבקרות, החוקרים זיהו יותר ממאה חלבונים כאלה שרמותיהם השתנו לאחר הפגיעה. רבים מהם נקשרו לגידול כלי דם ולתגובות לחוסר חמצן — שני תהליכים מרכזיים בהחלמת הלב. חלבון אחד, LMNA, בלט כי רמותיו עקבו באופן הדוק אחר עריכת RNA מסוים של הגן Atp6v1h, העוזר לווסת משאבה תאית הקשורה לאיתות mTOR. הצורה המסולסת של ה‑RNA הזו היתה שכיחה יותר בלבבות פגועים, מה שמרמז ש‑LMNA עשוי לסייע בכיוונון חישת האנרגיה בזמן המתח של הרפיקשור.
התמקדות בגנים מרכזיים ואימות בחיות
המחברים הדגישו מספר גנים שאצלם צורות RNA ערוכות עשויות להטות את תאי הלב לכיוון הישרדות או נזק. למשל, גורם מגיב להיפוקסיה בשם Eif4e2, רגולטור הקשור לדלקת Traf6, קולט אינסולין Insr, ורגולטור רגיש סטרס Nr4a1 — כולם ייצרו וריאנטים של RNA שהתגלו בתדירות גבוהה יותר לאחר הפגיעה. אחרים, כגון Map4k4, הראו ירידה בשימוש בצורות ספלייס מסוימות. כדי לבדוק האם השינויים האלה ברמת ה‑RNA הם אמיתיים מעבר לניתוח הממוחשב, הצוות יצר מודל עכברים משלו של פגיעה רפיקשורפית. הם אישרו שרבים מהווריאנטים החזויים של גנים וחלבוני קשירת ה‑RNA השתנו באותו הכיוון הן ברמת ה‑RNA והן ברמת החלבון, מחזק את הטענה שאלו מאפיינים אמיתיים של הלב הפגוע. 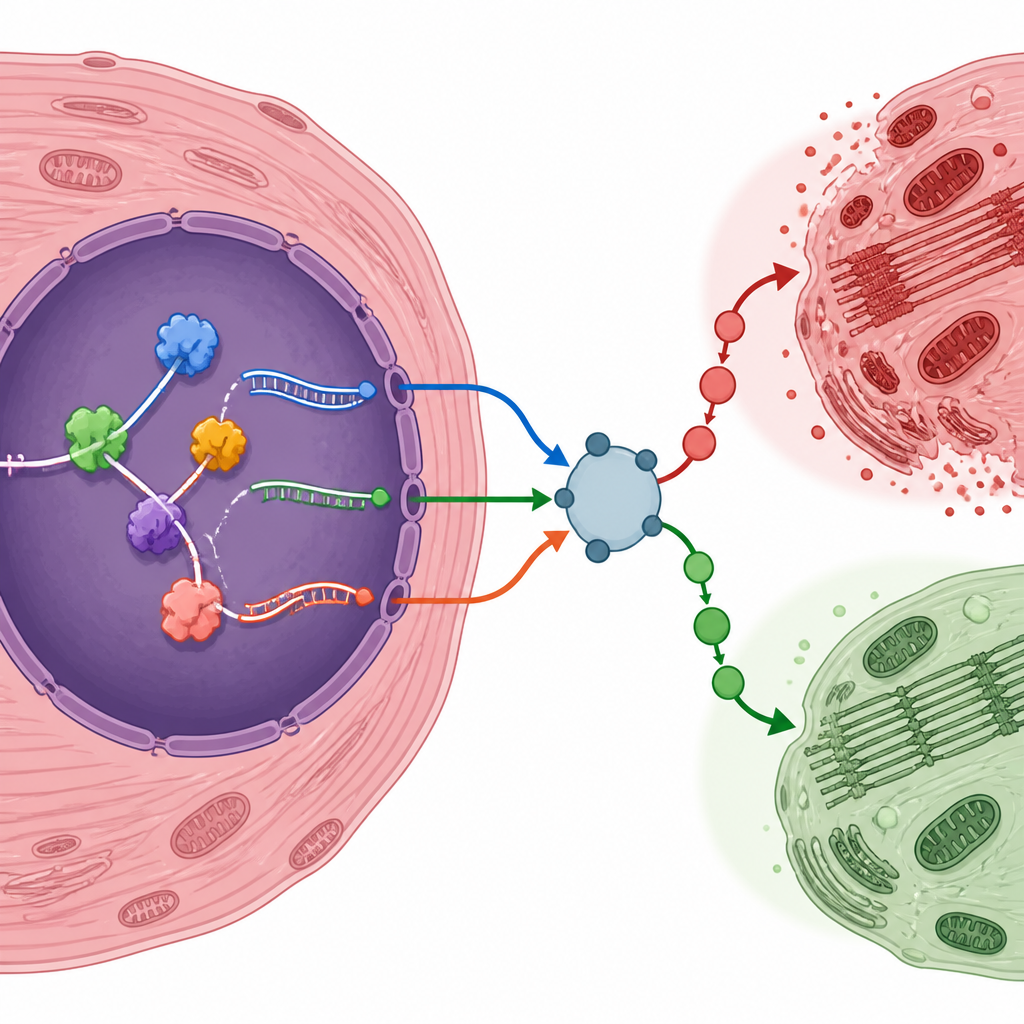
מה המשמעות לטיפול בלב בעתיד
במלים פשוטות, העבודה הזאת מראה שאחרי שחזרת זרימת הדם ללב, התאים מחליפים במהירות את הודעותיהם הפנימיות על‑ידי חיתוך מחדש של RNA בדרכים חדשות, בהנחיית סט של חלבוני בקרה. הודעות ערוכות אלה מתאמות מסלולי קבלת החלטות מרכזיים שמווסתים סטרס תאי, ניקוי והתהליכים הדלקתיים. אמנם המחקר נערך בעכברים ואין בו הוכחה עקבית לסיבתיות, אך הוא ממפה רשת של מתגי RNA מועמדים ושל שולטיהם שעשויים לעצב את כמות הנזק הקבוע אחרי התקף לב. עם הזמן, טיפולים שיכוונו בעדינות חלבוני קשירת RNA או תבניות ספלייס ספציפיות יכולים להשלים טיפולים קיימים ולהציע דרך מדויקת יותר להגן על הלב כשאספקת הדם לו משוחזרת.
ציטוט: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
מילות מפתח: פגיעה איסכמית-רפיקשורפי של שריר הלב, ספלייסינג חלופי, חלבוני קשירת RNA, מסלול mTOR, אותות MAPK