Clear Sky Science · ar
تحليل شامل لتشتت التوصيل البديل الشاذ ومنظمات بروتينات ربط الحمض النووي الريبي المرتبطة بإصابة نقص التروية مع إعادة التروية القلبية لدى الفئران
لماذا قد يؤذي إرجاع عمل القلب القلب نفسه
عند حدوث نوبة قلبية، يسارع الأطباء إلى إعادة فتح الشريان المسدود واستعادة تدفق الدم. ومع ذلك، قد تتسبب هذه الخطوة المنقذة للحياة أيضاً في تلف متأخر للقلب يُعرف باسم إصابة إعادة التروية. تبحث هذه الدراسة في الفئران بعمق داخل خلايا القلب عن كيفية قص وتحرير رسائل الحمض النووي الريبي الصغيرة عند عودة تدفق الدم، وكيف يمكن أن تفاقم هذه التغييرات التلف أو تخفف منه. فهم هذا المستوى المخفي من التحكم قد يفتح طرقاً جديدة لحماية القلب بعد النوبة القلبية.
رسائل مخفية داخل خلايا القلب
تستخدم كل خلية الحمض النووي الريبي كنسخة عملية للمعلومة الوراثية. قبل أن تُستخدم هذه الرسائل لصنع البروتينات، يمكن قصّها وإعادة ربطها بطرق مختلفة، وهي عملية تعرف بالتوصيل البديل. وهذا يعني أن جيناً واحداً يمكن أن يولّد عدة نسخ بروتينية ذات تأثيرات مميزة. تساءل المؤلفون كيف يتغير هذا التحرير في قلوب الفئران التي تعرّضت إلى انسداد وختمه ثم إعادة فتح لشريان تاجي رئيسي، وهو نموذج قياسي للنوبة القلبية تليها معالجة. أعادوا تحليل مجموعة بيانات تسلسل الحمض النووي الريبي الموجودة التي قارنت نسيج القلب من فئران مصابة مع ضوابط خضعت لعملية وهمية.
تحولات واسعة في تحرير الحمض النووي الريبي بعد الإصابة
وجد الفريق أن إصابة إعادة التروية صاحبتها تحولات واسعة في أنماط تحرير الحمض النووي الريبي عبر الجينوم. رصدوا مئات أحداث التوصيل التي اختلفت استخدامها بين القلوب السليمة والمصابة، خصوصاً في الطرف البادئ لمقاطع الحمض النووي الريبي. كان العديد من الجينات المتأثرة ينتمي إلى مسارات إشارية خلوية مهمة تقرر إن كانت خلايا عضلة القلب تنمو أو تعيد تدوير مكوناتها أو تنخر. على وجه الخصوص، أظهرت الجينات في مساري mTOR وMAPK، اللذين يساعدان في التحكم في الأيض الخلوي واستجابات الضغط والالتهاب، تغييرات قوية في كيفية قصّ وتجميع رسائلها الحمضية. 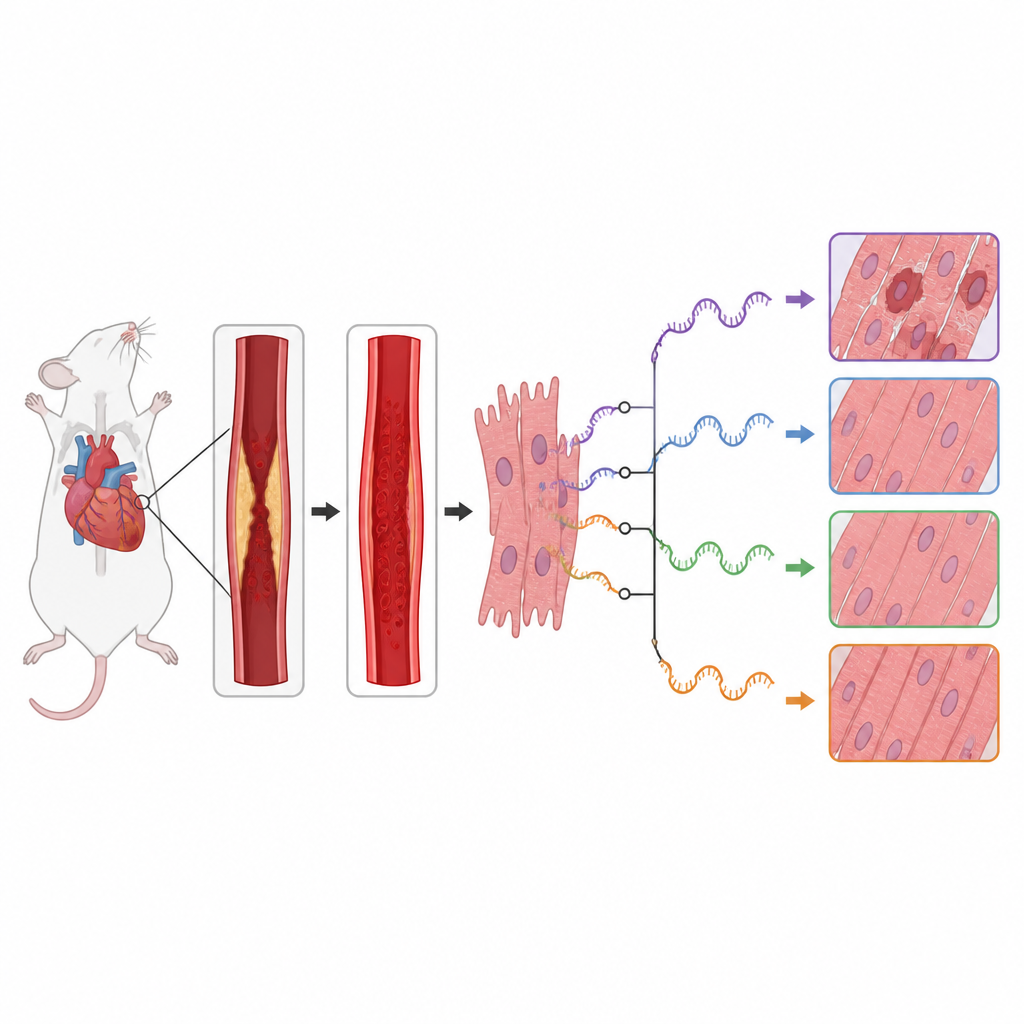
البروتينات التي توجه قصّ الحمض النووي الريبي
تعمل بروتينات ربط الحمض النووي الريبي كمرشدين يحددون أين يُقصّ ويُلحَق كل حمض نووي ريبي. بمقارنة نشاط الجينات في القلوب المصابة والضابطة، حدد الباحثون أكثر من مئة من هذه البروتينات التي تغيرت مستوياتها بعد الإصابة. ارتبط العديد منها بنمو الأوعية الدموية والاستجابات لنقص الأكسجة، وهما عمليتان محوريّتان في تعافي القلب. برز بروتين واحد، LMNA، لأن مستوياته تزامنت عن قرب مع تحرير حمض نووي ريبي محدد من جين يسمى Atp6v1h، الذي يساعد في تنظيم مضخة خلوية مرتبطة بإشارة mTOR. كان الشكل الموصّل من هذا الحمض النووي الريبي أكثر شيوعاً في القلوب المصابة، مما يلمح إلى أن LMNA قد يساعد في ضبط استشعار الطاقة أثناء إجهاد إعادة التروية.
التركيز على جينات رئيسية وتأكيدها في الحيوان
سلّط المؤلفون الضوء على عدة جينات قد تميل بصيغها المعدّلة من الحمض النووي الريبي خلايا القلب نحو البقاء أو التلف. على سبيل المثال، عامل الاستجابة لنقص الأكسجة Eif4e2، والمُنظِّم المرتبط بالالتهاب Traf6، ومستقبل الإنسولين Insr، والمنظم الحساس للإجهاد Nr4a1 كل إنتاجوا متغيرات حمض نووي ريبية كانت أكثر تكراراً بعد الإصابة. أما آخرون، مثل Map4k4، فظهر لديهم انخفاض في استخدام أشكال توصيل معينة. لاختبار ما إذا كانت هذه التحولات الحامضية حقيقية تتجاوز التحليل الحاسوبي، أنشأ الفريق نموذجهم الخاص من إصابة إعادة التروية لدى الفأر. أكدوا أن العديد من المتغيرات الجينية المتوقعة وبروتينات ربط الحمض النووي الريبي تغيرت في نفس الاتجاه على مستوى الحمض النووي الريبي والبروتين، مما يعزز الحجة بأن هذه سمات حقيقية للقلب المصاب. 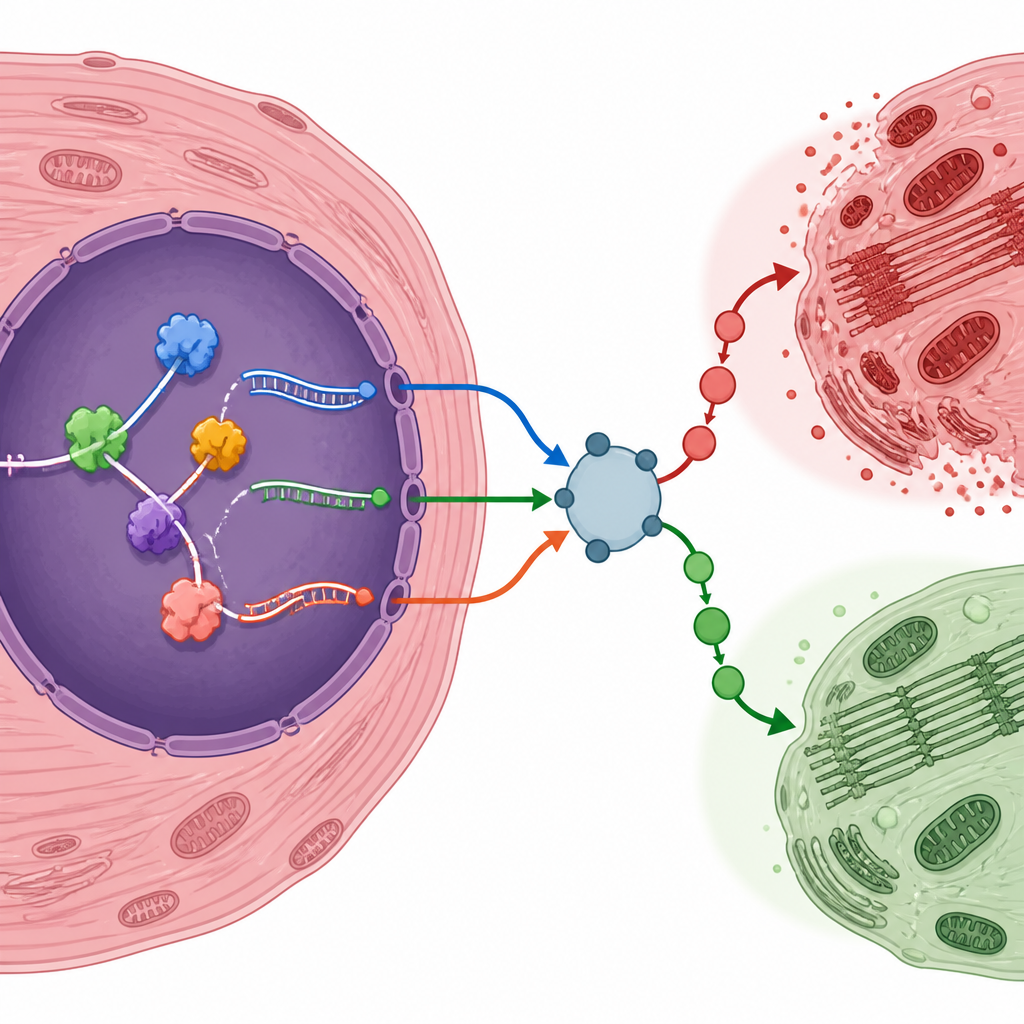
ماذا يعني هذا لرعاية القلب في المستقبل
بعبارة بسيطة، تُظهر هذه الدراسة أنه بعد عودة تدفق الدم إلى القلب، تعيد الخلايا بسرعة توصيل رسائلها الداخلية عبر قصّ الحمض النووي الريبي بطرق جديدة، موجهة من قبل مجموعة من البروتينات المنظمة. تقوم هذه الرسائل المعدّلة بضبط مسارات اتخاذ القرار الرئيسية التي تتحكم في إجهاد الخلايا والتنظيف والالتهاب. رغم أن الدراسة أُجريت على الفئران ولم تثبت بعد السببية، فإنها ترسم شبكة من مفاتيح التوصيل الحمضية المحتملة ومتحكميها التي قد تشكّل مدى الضرر الدائم بعد النوبة القلبية. مع الوقت، قد تكمل العلاجات التي تعدل بلطف بروتينات ربط الحمض النووي الريبي أو أنماط التوصيل المحددة العلاجات الحالية، مقدّمةً طريقة أدق لحماية القلب عندما يُستعاد تزويده بالدم.
الاستشهاد: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
الكلمات المفتاحية: إصابة نقص التروية مع إعادة التروية القلبية, التوصيل البديل, بروتينات ربط الحمض النووي الريبي, مسار mTOR, إشارة MAPK