Clear Sky Science · pt
Análise abrangente do splicing alternativo aberrante e reguladores de proteínas de ligação ao RNA associados à lesão por isquemia-reperfusão miocárdica em camundongos
Por que reiniciar o coração ainda pode prejudicá-lo
Quando alguém tem um infarto, os médicos correm para reabrir a artéria bloqueada e restaurar o fluxo sanguíneo. Ainda assim, esse passo que salva vidas também pode ferir o coração em uma onda atrasada de dano chamada lesão por reperfusão. Este estudo em camundongos investiga profundamente dentro das células cardíacas como pequenas mensagens de RNA são cortadas e editadas quando o fluxo sanguíneo retorna, e como essas mudanças podem agravar ou aliviar o dano. Compreender essa camada oculta de controle pode abrir novos caminhos para proteger o coração após um ataque cardíaco.
Mensagens ocultas dentro das células cardíacas
Cada célula usa RNA como uma cópia de trabalho da informação genética. Antes que essas mensagens de RNA sejam usadas para produzir proteínas, elas podem ser cortadas e religadas de maneiras diferentes, um processo conhecido como splicing alternativo. Isso significa que um único gene pode gerar várias versões de proteína com efeitos distintos. Os autores perguntaram como esse processo de edição muda em corações de camundongos expostos a uma oclusão controlada e à reperfusão de uma artéria coronária principal, um modelo padrão de infarto seguido por tratamento. Eles reanalisaram um conjunto de dados de sequenciamento de RNA já existente que comparou tecido cardíaco de camundongos lesionados com controles submetidos a cirurgia simulada.
Grandes mudanças no splicing de RNA após a lesão
A equipe encontrou que a lesão por reperfusão veio acompanhada de mudanças abrangentes nos padrões de edição do RNA ao longo do genoma. Detectaram centenas de eventos de splicing cujo uso diferiu entre corações saudáveis e lesionados, especialmente na extremidade inicial dos segmentos de RNA. Muitos dos genes afetados pertenciam a vias de sinalização celular importantes que decidem se os miócitos crescem, reciclam seus componentes ou se autodestroem. Em particular, genes das vias mTOR e MAPK, que ajudam a controlar o metabolismo celular, respostas ao estresse e inflamação, exibiram alterações significativas em como seus RNAs eram cortados e montados. 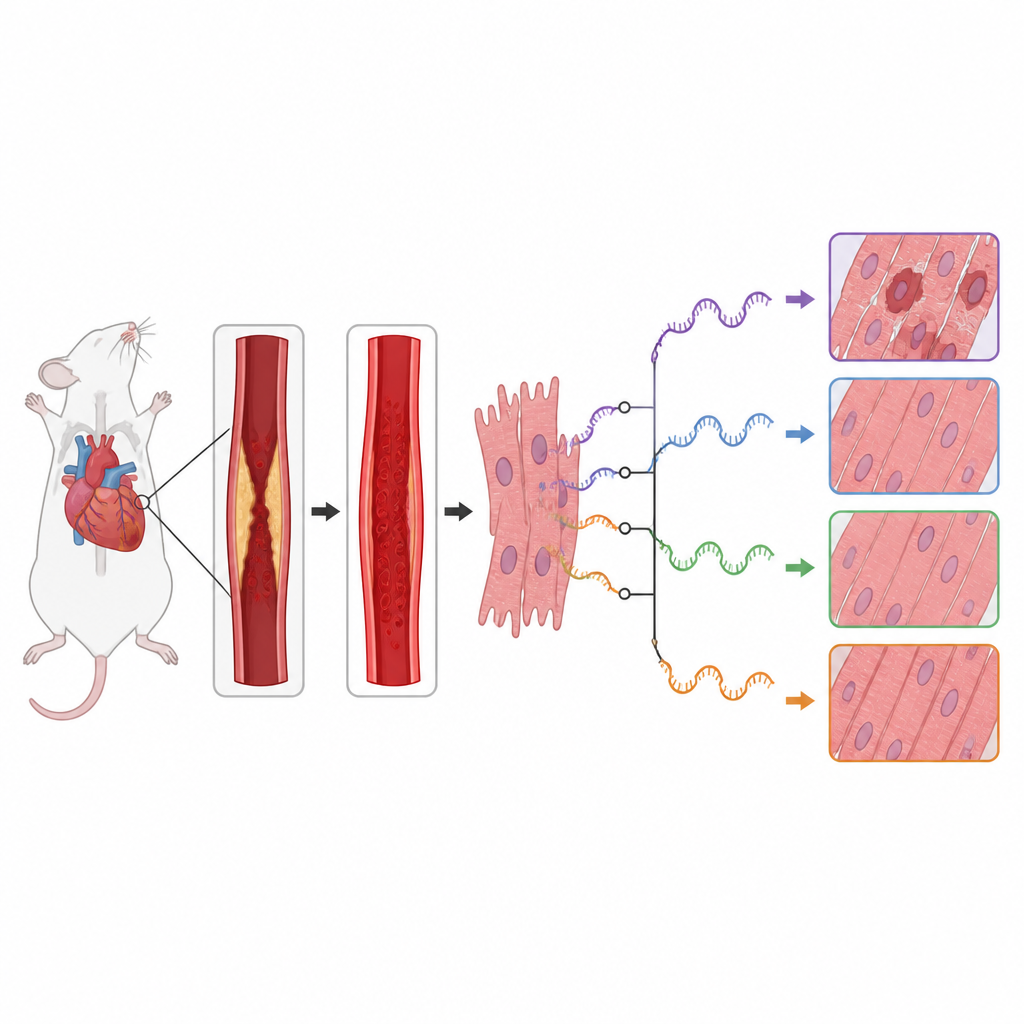
Proteínas que orientam o corte do RNA
Proteínas de ligação ao RNA atuam como controladores de tráfego que determinam onde cada RNA é fatiado e costurado. Ao comparar a atividade gênica em corações lesionados e controles, os pesquisadores identificaram mais de cem dessas proteínas cujos níveis mudaram após a lesão. Muitas estavam vinculadas ao crescimento de vasos sanguíneos e às respostas à baixa oxigenação, dois processos centrais para a recuperação cardíaca. Uma proteína, LMNA, destacou-se porque seus níveis acompanharam de perto a edição de um RNA específico do gene Atp6v1h, que ajuda a regular uma bomba celular ligada à sinalização mTOR. A forma splicada desse RNA foi mais comum em corações lesionados, sugerindo que LMNA pode ajudar a ajustar a detecção de energia durante o estresse da reperfusão.
Aproximando-se de genes-chave e confirmando em animais
Os autores destacaram vários genes cujas formas de RNA editadas podem inclinar as células cardíacas em direção à sobrevivência ou ao dano. Por exemplo, um fator responsivo à hipóxia chamado Eif4e2, um regulador ligado à inflamação Traf6, o receptor de insulina Insr e um regulador sensível ao estresse Nr4a1 produziram variantes de RNA mais frequentes após a lesão. Outros, como Map4k4, mostraram uso reduzido de formas de splicing específicas. Para testar se essas mudanças de RNA eram reais além da análise computacional, a equipe criou seu próprio modelo de reperfusão em camundongos. Confirmaram que muitas das variantes gênicas previstas e proteínas de ligação ao RNA mudaram na mesma direção tanto nos níveis de RNA quanto de proteína, fortalecendo a evidência de que essas são características genuínas do coração lesionado. 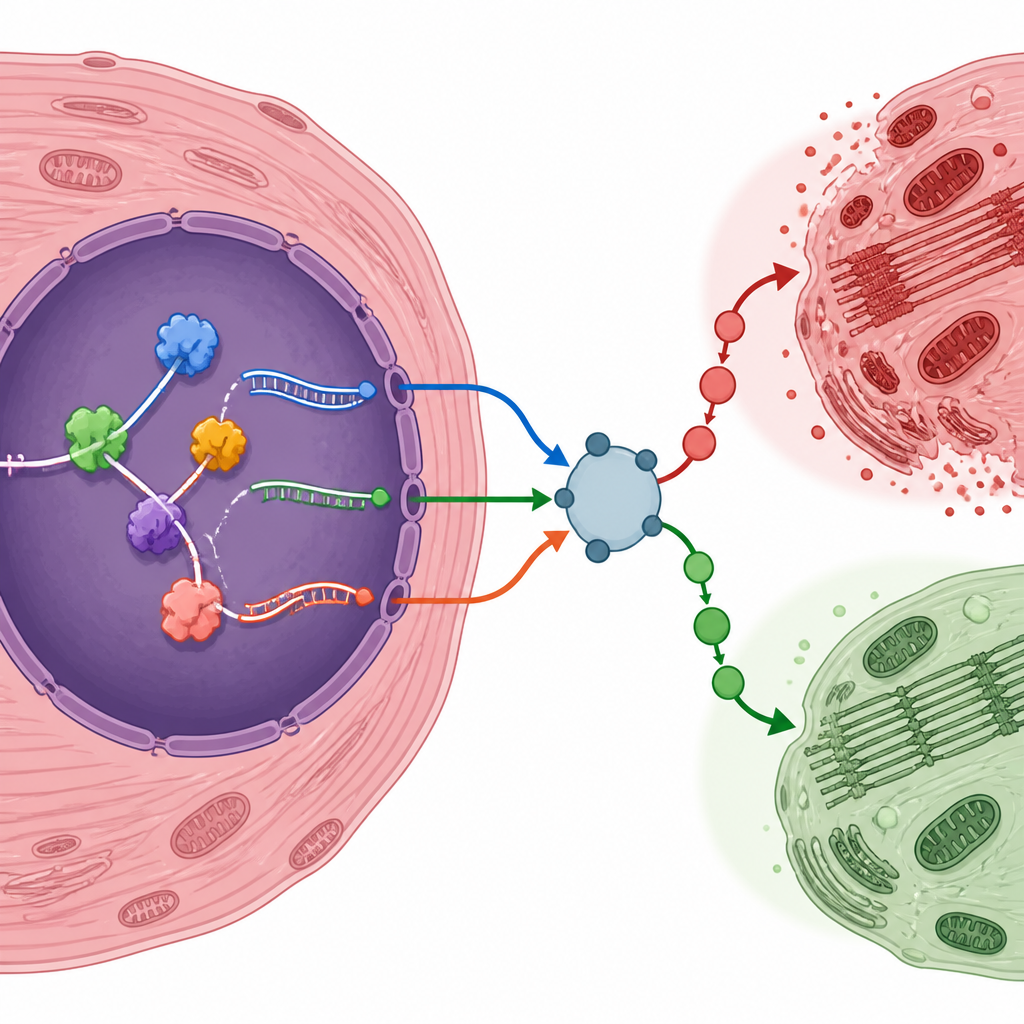
O que isso significa para os cuidados cardíacos futuros
Em termos simples, este trabalho mostra que, após o retorno do fluxo sanguíneo ao coração, as células reconfiguram rapidamente suas mensagens internas recortando o RNA de novas maneiras, guiadas por um conjunto de proteínas reguladoras. Essas mensagens editadas ajustam grandes vias decisórias que governam estresse celular, limpeza e inflamação. Embora o estudo tenha sido realizado em camundongos e ainda não prove causalidade, ele mapeia uma rede de interruptores de RNA candidatos e seus controladores que podem moldar quanto dano permanente segue um infarto. Com o tempo, terapias que ajustem com precisão proteínas de ligação ao RNA ou padrões específicos de splicing poderiam complementar os tratamentos atuais, oferecendo uma forma mais precisa de proteger o coração quando seu suprimento sanguíneo é restabelecido.
Citação: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Palavras-chave: lesão por isquemia-reperfusão miocárdica, splicing alternativo, proteínas de ligação ao RNA, via mTOR, sinalização MAPK