Clear Sky Science · de
Umfassende Analyse abweichender alternativer Spleißvorgänge und regulatorischer RNA-bindender Proteine im Zusammenhang mit myokardialer Ischämie-Reperfusionsverletzung bei Mäusen
Warum das Wiederherstellen des Blutflusses dem Herzen schaden kann
Wenn jemand einen Herzinfarkt hat, bemühen sich Ärztinnen und Ärzte, die blockierte Arterie rasch wieder zu eröffnen und die Durchblutung wiederherzustellen. Doch dieser lebensrettende Schritt kann in einer verzögerten Schadenswelle, der sogenannten Reperfusionsverletzung, zusätzliches Herzgewebe schädigen. Diese Studie an Mäusen blickt tief in Herzmuskelzellen hinein, um zu untersuchen, wie kleine RNA-Botschaften beim Wiederaufkommen des Blutflusses geschnitten und bearbeitet werden und wie diese Veränderungen den Schaden verschlimmern oder lindern könnten. Das Verständnis dieser verborgenen Kontrollschicht könnte neue Wege eröffnen, das Herz nach einem Infarkt zu schützen.
Verborgene Botschaften in Herzmuskelzellen
Jede Zelle nutzt RNA als Arbeitskopie der genetischen Information. Bevor diese RNA-Botschaften zur Proteinproduktion genutzt werden, können sie auf unterschiedliche Weise geschnitten und wieder zusammengesetzt werden — ein Prozess, der als alternatives Spleißen bekannt ist. Das bedeutet, dass ein einzelnes Gen mehrere Proteinvarianten mit unterschiedlichen Wirkungen hervorbringen kann. Die Autoren fragten, wie sich dieser Bearbeitungsprozess in den Herzen von Mäusen verändert, die einem kontrollierten Verschluss und der erneuten Öffnung einer wichtigen Koronararterie ausgesetzt wurden — ein gängiges Modell für Herzinfarkt gefolgt von Behandlung. Sie analysierten ein vorhandenes RNA-Sequenzierungs-Datenset neu, das Herzgewebe von verletzten Mäusen mit sham-operierten Kontrollen verglich.
Weitreichende Verschiebungen im RNA-Spleißen nach Verletzung
Das Team fand heraus, dass die Reperfusionsverletzung von weitreichenden Veränderungen der RNA-Bearbeitungsmuster über das gesamte Genom begleitet war. Sie detektierten Hunderte von Spleißereignissen, deren Nutzung zwischen gesunden und verletzten Herzen unterschiedlich war, insbesondere am 5'-Ende der RNA-Abschnitte. Viele der betroffenen Gene gehörten zu wichtigen Zellsignalwegen, die darüber entscheiden, ob Herzmuskelzellen wachsen, ihre Bestandteile recyceln oder sich selbst zerstören. Besonders betroffen waren Gene der mTOR- und MAPK-Wege, die den Zellstoffwechsel, Stressreaktionen und Entzündungen steuern; bei ihnen zeigten sich ausgeprägte Veränderungen in der Art, wie ihre RNA geschnitten und zusammengesetzt wurde. 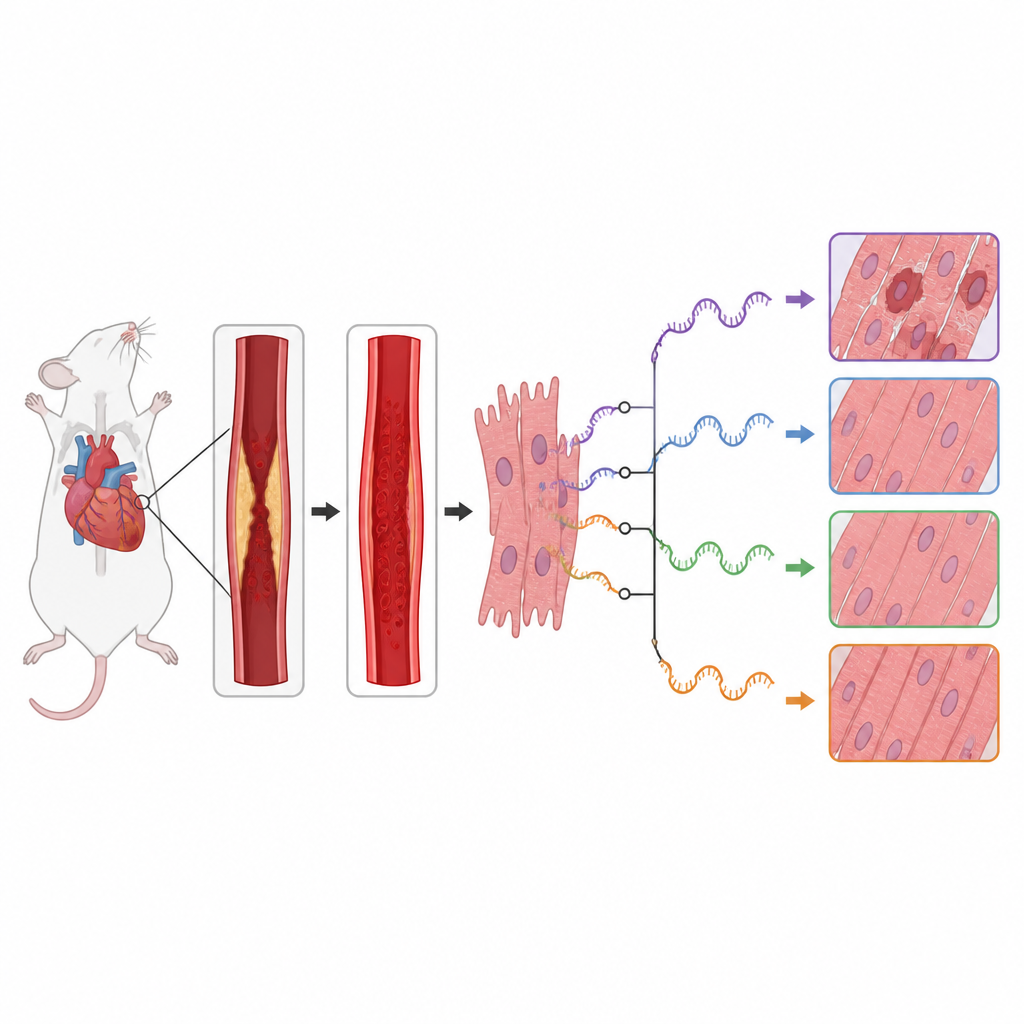
Proteine, die das RNA-Spleißen steuern
RNA-bindende Proteine fungieren als Verkehrsleiter, die entscheiden, wo jede RNA geschnitten und zusammengesetzt wird. Durch den Vergleich der Genaktivität in verletzten und Kontrollherzen identifizierten die Forschenden mehr als hundert solche Proteine, deren Mengen sich nach der Verletzung veränderten. Viele waren mit Gefäßwachstum und Reaktionen auf Sauerstoffmangel verknüpft — zwei Prozesse, die für die Erholung des Herzens zentral sind. Ein Protein, LMNA, fiel besonders auf, weil seine Mengen eng mit der Bearbeitung einer spezifischen RNA eines Gens namens Atp6v1h korrelierten, das eine zelluläre Pumpe reguliert, die mit der mTOR-Signalgebung verbunden ist. Die gespleißte Form dieser RNA war in verletzten Herzen häufiger, was darauf hindeutet, dass LMNA die Energieerkennung unter dem Stress der Reperfusion feinjustieren könnte.
Fokussierung auf Schlüsselgene und Bestätigung im Tiermodell
Die Autoren hoben mehrere Gene hervor, deren gespleißte RNA-Formen Herzmuskelzellen eher in Richtung Überleben oder Schädigung lenken könnten. Beispielsweise produzierten ein hypoxie-reaktiver Faktor namens Eif4e2, ein entzündungsbezogener Regulator Traf6, der Insulinrezeptor Insr und ein stresssensitiver Regulator Nr4a1 nach der Verletzung häufiger vorkommende RNA-Varianten. Andere, wie Map4k4, zeigten eine verringerte Verwendung bestimmter Spleißformen. Um zu prüfen, ob diese RNA-Verschiebungen über die Computeranalyse hinaus real sind, erzeugte das Team ein eigenes Mausmodell der Reperfusionsverletzung. Sie bestätigten, dass viele der vorhergesagten Genvarianten und RNA-bindenden Proteine in dieselbe Richtung sowohl auf RNA- als auch auf Proteinebene verändert waren, was die Annahme stützt, dass es sich um echte Merkmale des verletzten Herzens handelt. 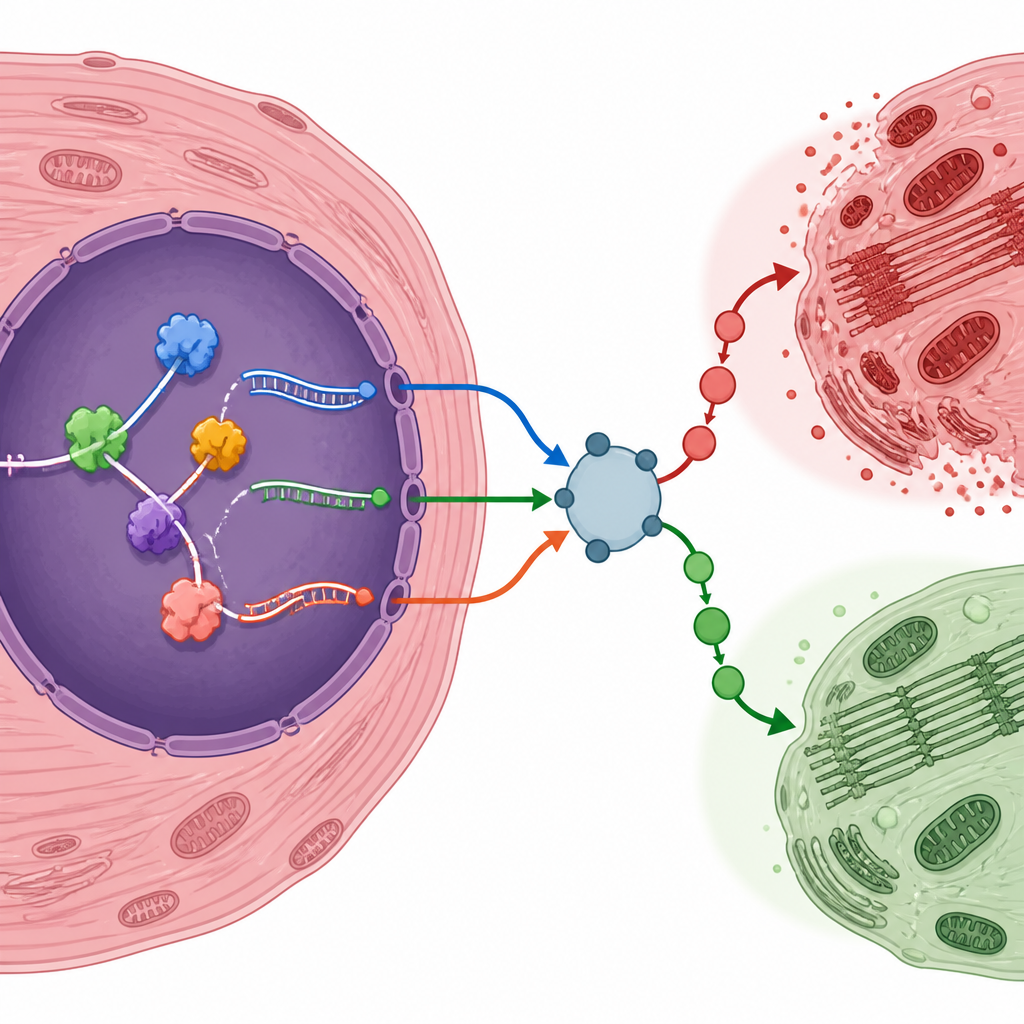
Was das für die künftige Herzmedizin bedeutet
Einfach gesagt zeigt diese Arbeit, dass sich Zellen nach Wiederherstellung des Blutflusses rasch durch erneutes Schneiden von RNA intern neu verdrahten, gesteuert von einer Reihe regulatorischer Proteine. Diese bearbeiteten Botschaften verändern wichtige Entscheidungswege, die Zellstress, Aufräumprozesse und Entzündung steuern. Obwohl die Studie an Mäusen durchgeführt wurde und noch keine direkte Ursache-Wirkungs-Beziehung beweist, kartiert sie ein Netzwerk potenzieller RNA-Schalter und ihrer Regulatoren, das bestimmen könnte, wie viel bleibender Schaden einem Herzinfarkt folgt. In Zukunft könnten Therapien, die RNA-bindende Proteine oder spezifische Spleißmuster gezielt anpassen, die aktuellen Behandlungen ergänzen und eine präzisere Möglichkeit bieten, das Herz beim Wiederherstellen der Blutversorgung zu schützen.
Zitation: Zhou, D., Tan, Y., Jiang, B. et al. Comprehensive analysis of aberrant alternative splicing and RNA binding proteins regulators associated with myocardial ischemia reperfusion injury in mice. Sci Rep 16, 15156 (2026). https://doi.org/10.1038/s41598-026-45174-0
Schlüsselwörter: myokardiale Ischämie-Reperfusionsverletzung, alternatives Spleißen, RNA-bindende Proteine, mTOR-Signalweg, MAPK-Signalgebung