Clear Sky Science · zh
hnRNP A2/B1 截短体对 G-四链体单链 DNA 的分子识别与诱导二聚化
细胞如何识别病毒 DNA
病毒会在我们的细胞内留下其遗传物质的痕迹,机体必须迅速识别这些痕迹以发起防御。该研究探讨了一种丰度较高的细胞蛋白 hnRNP A2/B1 如何帮助感知许多病毒中常见的不寻常 DNA 构象。通过理解该蛋白在结合此类 DNA 时如何改变其构象,研究人员希望为新的抗病毒和抗癌策略奠定基础。
位于细胞核中的构象感知蛋白
hnRNP A2/B1 最为人所知的是作为管理 RNA(遗传信息工作拷贝)的辅助蛋白。它主要位于细胞核中,参与从 RNA 剪接到控制其稳定性的一系列关键任务。然而,近期工作表明该蛋白还有第二种功能:它可以作为侵入病毒外来 DNA 的传感器。当病毒 DNA 进入细胞核时,hnRNP A2/B1 参与激活先天免疫信号,触发抗病毒分子干扰素的产生。
解析一种易聚集的蛋白
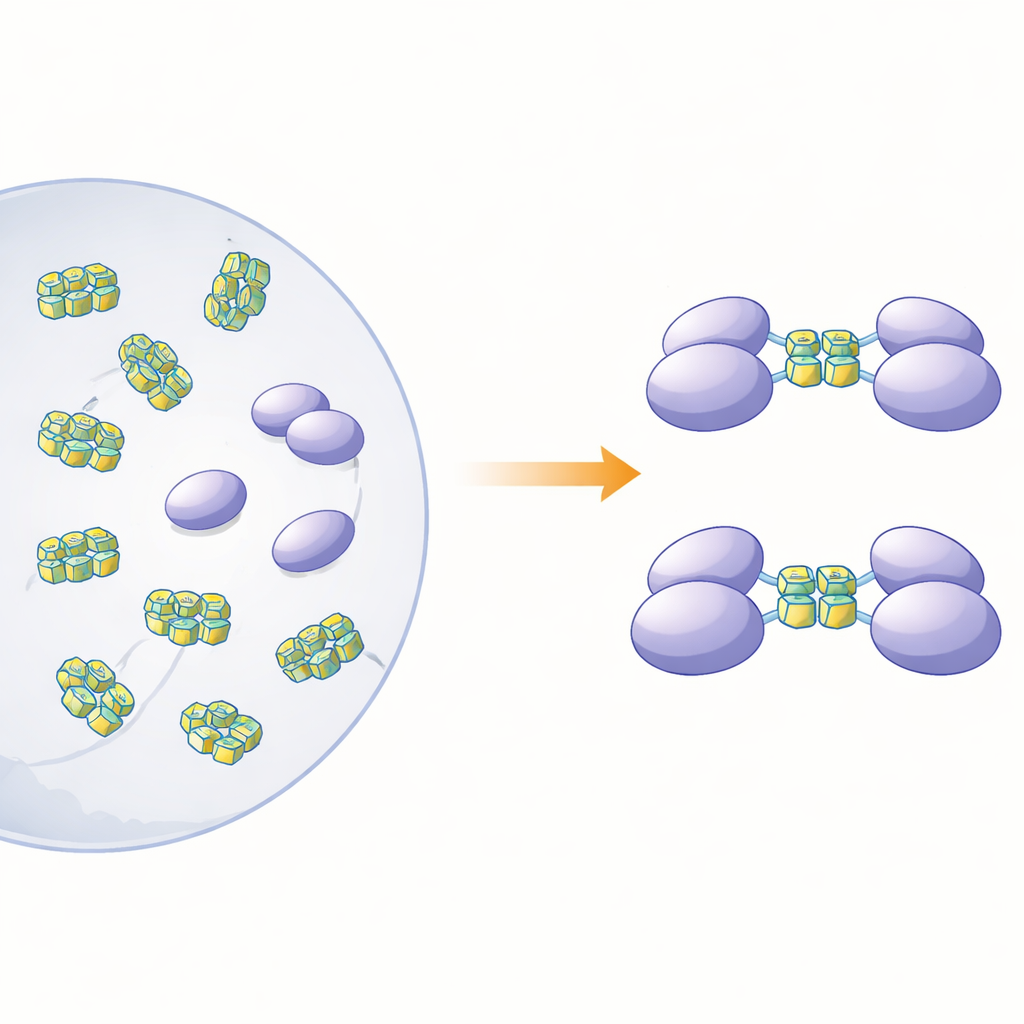
为澄清该蛋白的物理形态与其感知功能之间的关系,作者在细菌中制备了全长 hnRNP A2/B1 及若干截短版本。对溶液中全长蛋白的观察显示,它并不以整齐、独立的颗粒存在,而是形成大的、不规则的团块——“可溶的无定形聚集体”,这些聚集体不稳定且易进一步沉淀。相比之下,缺失蛋白尾端不同片段的三个截短版本在溶液中保持为整洁的单分子(单体)。基于计算的结构预测表明,hnRNP A2/B1 约四分之三由松散的无序区构成,尤其集中在两端。这些柔性区域似乎促进了聚集,并解释了为何难以获得该蛋白用于高分辨率结构研究的晶体。
类似病毒的 DNA 促使蛋白配对
研究人员接着询问哪些类型的 DNA 会被这些单体片段结合,以及这种结合会如何改变蛋白的状态。他们聚焦于可折叠形成 G-四链体 的单链 DNA 片段——由富含鸟嘌呤的序列组成、将链折成紧密 U 形的紧凑堆叠结构。这类构象散布在许多病毒基因组和与癌症相关的基因中。通过量热法和凝胶结合测试,团队表明一段跨越所谓 RRM 与 RGG 区域(残基 15–250)的片段能强烈结合单链 DNA,但不与对应的双链形式结合。基于尺寸分离和超速离心的实验揭示了一个显著效应:当该片段遇到由 12 或 22 个碱基形成的 G-四链体 DNA 时,两个蛋白片段副本会结合形成二聚体,而非四链体 DNA 则不会触发这种配对。
窥视一个柔性的界面
由于实验晶体学尝试反复失败,团队转向计算建模以可视化蛋白片段可能如何抓握 G-四链体。使用现代预测工具构建的模型表明,hnRNP A2/B1 更加刚性的中心结构域包裹着堆叠的 DNA 结构,而周围的无序片段保持可动。对接模拟突出了来自若干结构域的一组特定氨基酸,它们可能与 G-四链体形成氢键,从而稳定一个二聚复合体,在该复合体中两分子蛋白共享同一段 DNA。值得注意的是,这些相互作用残基与 hnRNP A2/B1 的近亲所使用的残基不同,暗示该蛋白已进化出一种独特的识别 G-四链体 DNA 的方式。
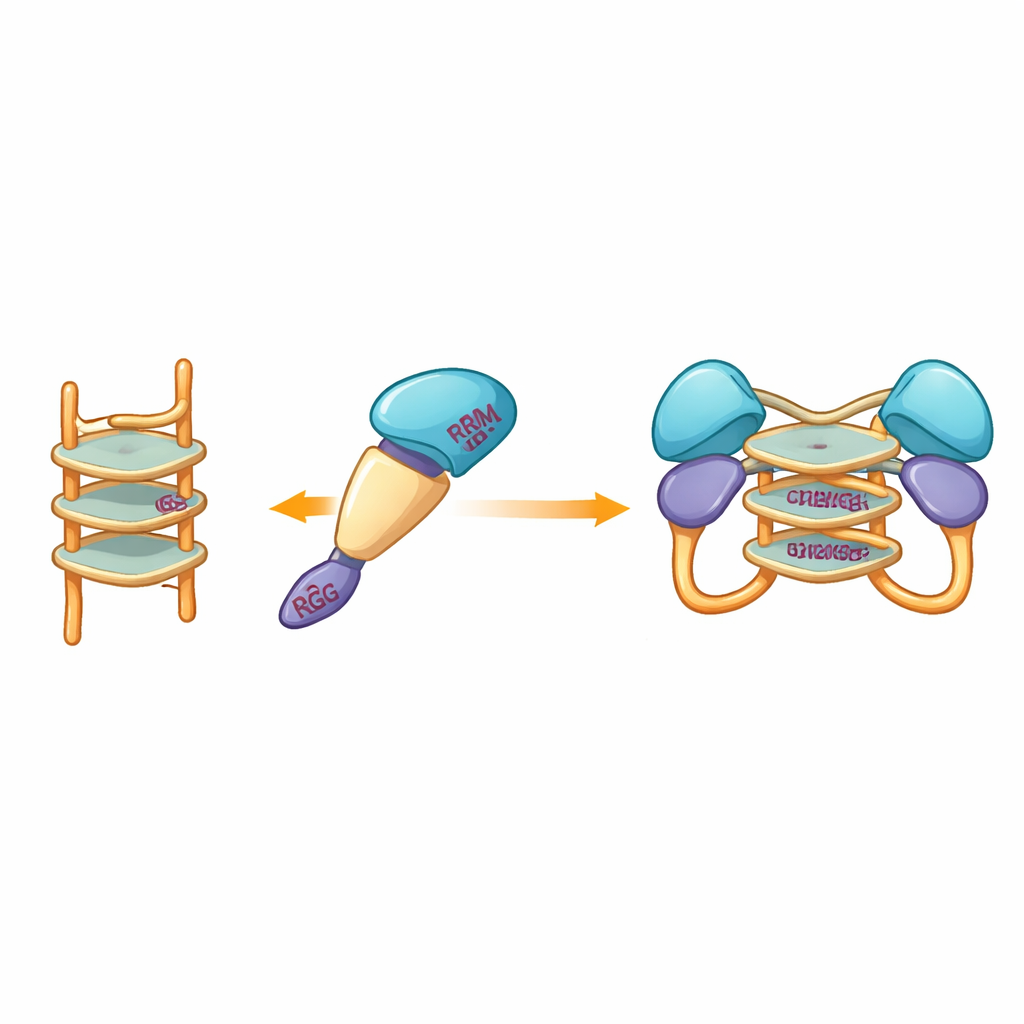
从蛋白配对到抗病毒防御
综合来看,研究结果显示尽管全长 hnRNP A2/B1 倾向于聚集成不稳定的团块,经过精细截短的版本则表现为有序的单分子,并在遇到 G-四链体 DNA 时配对。由许多病毒基因组中丰富的富含鸟嘌呤的单链序列特异性驱动的这种受控二聚形成,提示了该蛋白感知侵入 DNA 并帮助启动抗病毒信号通路的一个合理物理步骤。尽管这些结果来源于体外试验,仍需在活细胞和感染模型中得到确认,但它们为蛋白组装变化如何与细胞针对病毒的早期预警系统相关联提供了更清晰的、具体的图景——并为设计可调节这一反应的小分子以用于未来治疗提供了路线图。
引用: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
关键词: hnRNP A2/B1, G-四链体 DNA, DNA 感知, 抗病毒免疫, 蛋白质二聚化