Clear Sky Science · de
Molekulare Erkennung und induzierte Dimerisierung von hnRNP A2/B1-Trunkierungen durch einzelsträngige G‑Quadruplex‑DNA
Wie Zellen virale DNA erkennen
Viren hinterlassen Spuren ihres genetischen Materials in unseren Zellen, und der Körper muss diese Spuren rasch erkennen, um eine Abwehrreaktion auszulösen. Diese Studie untersucht, wie ein häufig vorkommendes zelluläres Protein, hnRNP A2/B1, ungewöhnliche DNA‑Formen erkennen könnte, die in vielen Viren verbreitet sind. Indem Forscher verstehen, wie sich die Gestalt dieses Proteins beim Binden an solche DNA verändert, erhoffen sie sich Grundlagen für neue antivirale und anticancer Strategien.
Ein formwahrnehmendes Protein im Zellkern
HnRNP A2/B1 ist vor allem als Hilfsprotein zur Verwaltung von RNA bekannt, der arbeitsfähigen Kopie genetischer Information. Es kommt hauptsächlich im Zellkern vor und ist an zahlreichen wichtigen Aufgaben beteiligt, vom Spleißen von RNA‑Botschaften bis zur Kontrolle ihrer Stabilität. Neuere Arbeiten haben jedoch ein zweites Wirken dieses Proteins gezeigt: Es kann als Sensor für fremde DNA von eindringenden Viren fungieren. Wenn virale DNA in den Zellkern gelangt, wirkt hnRNP A2/B1 an der Aktivierung angeborener Immunreaktionen mit, die die Produktion antiviraler Moleküle namens Interferone anstoßen.
Entwirrung eines aggregierten Proteins
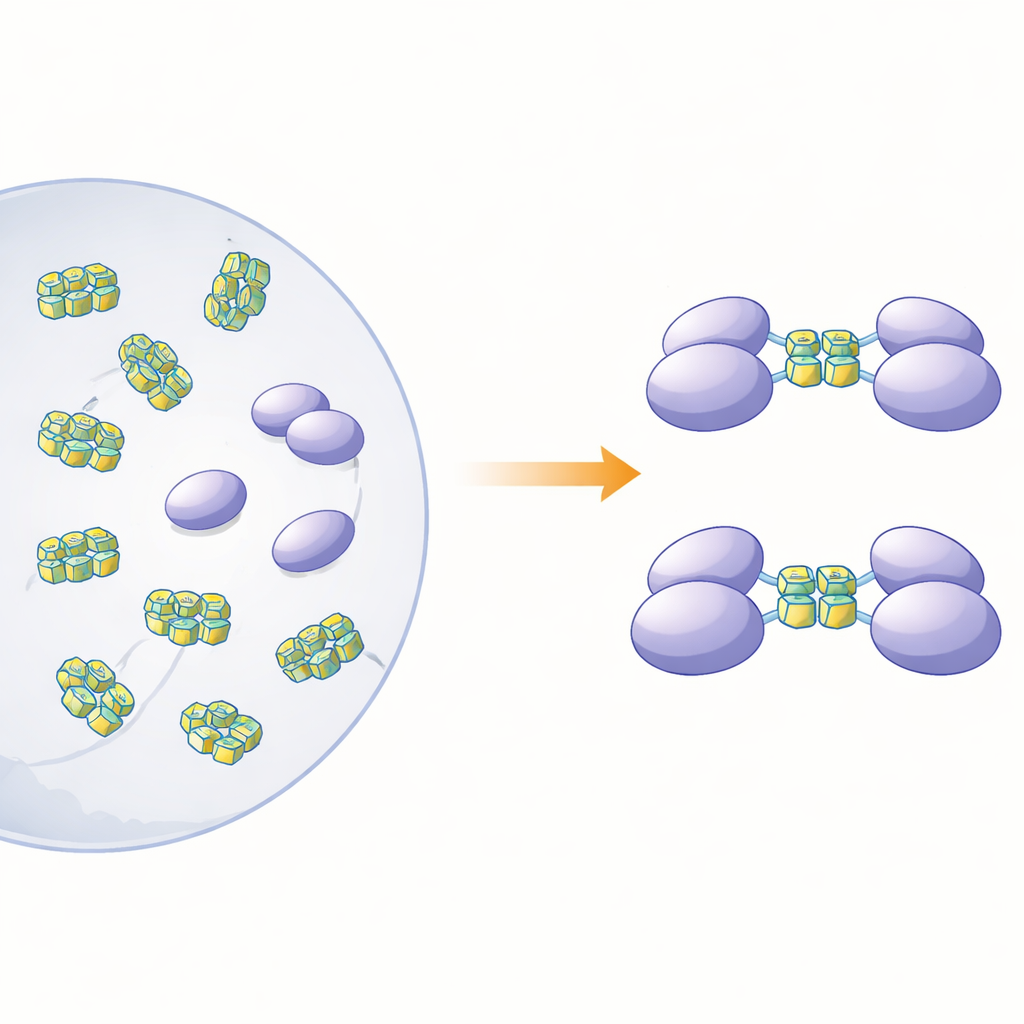
Um zu klären, wie die physische Gestalt dieses Proteins mit seiner Sensorfunktion zusammenhängt, stellten die Autorinnen und Autoren das vollständige hnRNP A2/B1 sowie mehrere verkürzte Versionen in Bakterien her. Bei Untersuchung des Vollproteins in Lösung zeigte sich, dass es sich nicht als ordentliche, separate Teilchen verhielt. Stattdessen bildete es große, unregelmäßige Klumpen – „lösliche amorphe Aggregate“ –, die instabil waren und zur weiteren Ausfällung neigten. Im Gegensatz dazu blieben drei verkürzte Versionen, denen verschiedene Abschnitte am Proteinende fehlten, als ordentliche Einzelmoleküle (Monomere) in Lösung. Computergestützte Strukturvorhersagen deuteten darauf hin, dass etwa drei Viertel von hnRNP A2/B1 aus beweglichen, ungeordneten Segmenten bestehen, besonders in der Nähe der Enden. Diese flexiblen Bereiche scheinen die Aggregation zu fördern und erklären, weshalb es so schwierig war, Kristalle des Proteins für hochauflösende Strukturstudien zu züchten.
Viraleartige DNA, die Proteine paaren lässt
Die Forschenden fragten dann, an welche Arten von DNA die monomeren Fragmente binden und was dieses Binden für den Zustand des Proteins bewirkt. Sie konzentrierten sich auf einzelsträngige DNA‑Segmente, die sich zu G‑Quadruplexen falten können – kompakte Stapel, die durch guaninreiche Sequenzen entstehen und den Strang in eine enge, U‑förmige Struktur biegen. Solche Formen finden sich in den Genomen vieler Viren und krebsrelevanter Gene. Mit kalorimetrischen Messungen und gelbasierten Bindungstests zeigte das Team, dass ein Fragment, das die sogenannten RRM‑ und RGG‑Regionen (Reste 15–250) umfasst, stark an einzelsträngige DNA bindet, nicht aber an die entsprechende doppelsträngige Form. Größenseparationen und Ultrazentrifugations‑Experimente enthüllten einen auffälligen Effekt: Wenn dieses Fragment auf G‑Quadruplex‑DNA mit 12 oder 22 Basen traf, schlossen sich zwei Kopien des Proteinfragments zu einem Dimer zusammen, während nicht‑Quadruplex‑DNA dieses Paaren nicht auslöste.
Blick in eine flexible Schnittstelle
Da experimentelle Kristallographieversuche wiederholt scheiterten, wandte sich das Team der computergestützten Modellierung zu, um zu visualisieren, wie das Proteinfragment ein G‑Quadruplex umfassen könnte. Modelle, die mit modernen Vorhersagetools erstellt wurden, legten nahe, dass die steiferen zentralen Domänen von hnRNP A2/B1 die gestapelte DNA‑Struktur umschließen, während die umgebenden ungeordneten Segmente beweglich bleiben. Docking‑Simulationen hoben eine Reihe spezifischer Aminosäuren aus mehreren Domänen hervor, die Wasserstoffbrücken mit dem G‑Quadruplex bilden könnten und so einen dimerischen Komplex stabilisieren, in dem zwei Proteinmoleküle dasselbe DNA‑Segment teilen. Bemerkenswert ist, dass diese interagierenden Reste sich von denen naher Verwandter von hnRNP A2/B1 unterscheiden, was darauf hindeutet, dass dieses Protein eine einzigartige Erkennungsweise für G‑Quadruplex‑DNA entwickelt hat.
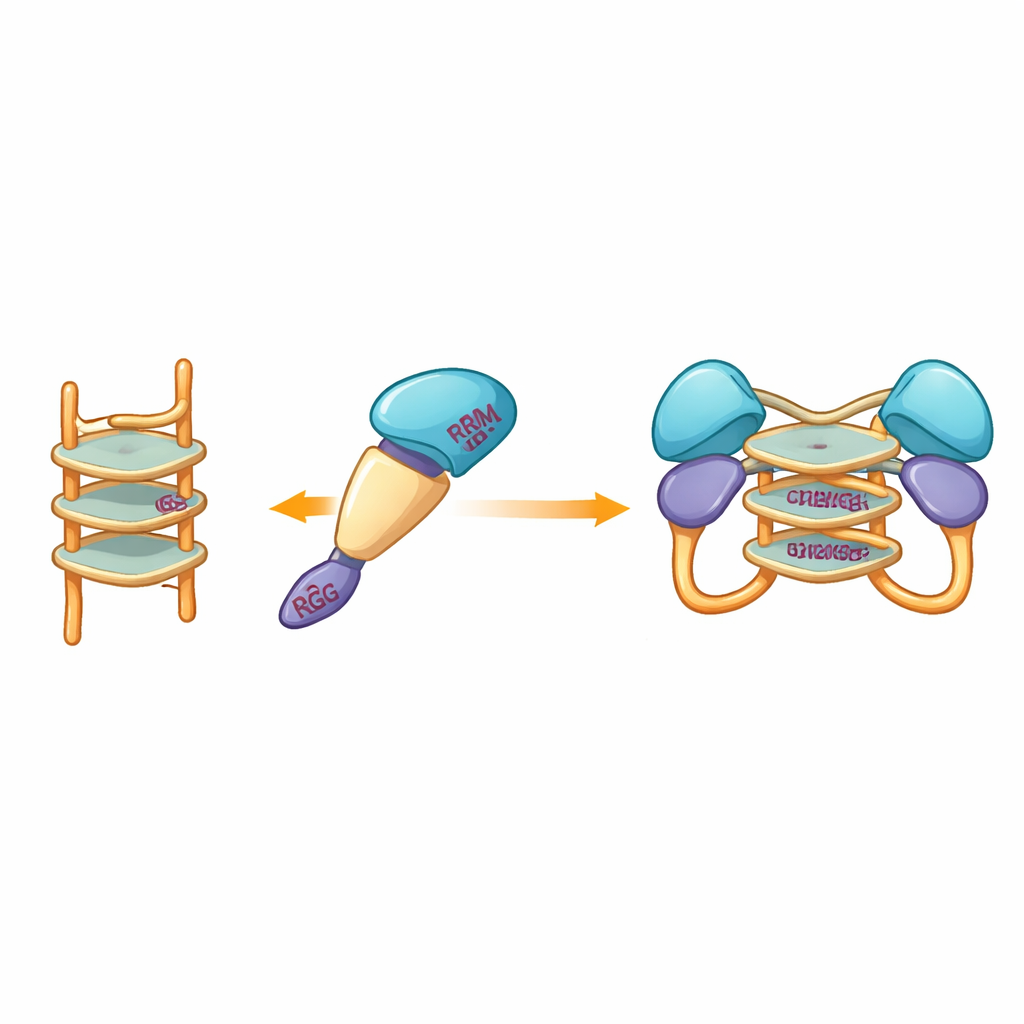
Vom Proteinpaar zur antiviralen Abwehr
Zusammengefasst zeigen die Ergebnisse, dass während das Vollprotein hnRNP A2/B1 dazu neigt, in instabile Aggregate zu verklumpen, sorgfältig beschnittene Versionen als geordnete Einzelmoleküle vorliegen, die sich beim Auftreffen auf G‑Quadruplex‑DNA paaren können. Diese kontrollierte Dimerbildung, die spezifisch von guaninreichen einzelsträngigen Sequenzen ausgehend ist—Sequenzen, die in vielen viralen Genomen reichlich vorkommen—, deutet auf einen plausiblen physikalischen Schritt hin, wie das Protein eindringende DNA erkennt und an der Aktivierung antiviraler Signalwege mitwirkt. Obwohl diese Ergebnisse in vitro gewonnen wurden und noch in lebenden Zellen und Infektionsmodellen bestätigt werden müssen, liefern sie ein klareres, konkreteres Bild davon, wie Veränderungen in der Proteinassemblierung mit dem Frühwarnsystem der Zelle gegen Viren verknüpft sein könnten — und sie bieten eine Roadmap für das Design kleiner Moleküle, die diese Reaktion in zukünftigen Therapien modifizieren könnten.
Zitation: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Schlüsselwörter: hnRNP A2/B1, G‑Quadruplex‑DNA, DNA‑Erkennung, antivirale Immunität, Proteindimerisierung