Clear Sky Science · pt
Reconhecimento molecular e dimerização induzida de truncamentos de hnRNP A2/B1 por DNA de fita simples em G-quadruplex
Como as células detectam DNA viral
Os vírus deixam rastros de seu material genético dentro de nossas células, e o organismo precisa reconhecer esses vestígios rapidamente para montar uma defesa. Este estudo investiga como uma proteína celular abundante, hnRNP A2/B1, pode ajudar a detectar formas incomuns de DNA que são comuns em muitos vírus. Ao entender como essa proteína muda de conformação quando se liga a esse tipo de DNA, os pesquisadores esperam lançar as bases para novas estratégias antivirais e anticâncer.
Uma proteína sensora de formas no núcleo
HnRNP A2/B1 é mais conhecida como uma proteína auxiliar que gerencia RNA, a cópia funcional da informação genética. Ela vive principalmente no núcleo celular e participa de várias tarefas essenciais, desde o splicing de mensagens de RNA até o controle de sua estabilidade. Trabalhos recentes, no entanto, revelaram uma segunda função para essa proteína: ela pode atuar como sensor de DNA estranho de vírus invasores. Quando DNA viral entra no núcleo, hnRNP A2/B1 participa da ativação de sinais da imunidade inata que desencadeiam a produção de moléculas antivirais chamadas interferons.
Desvendando uma proteína agregada
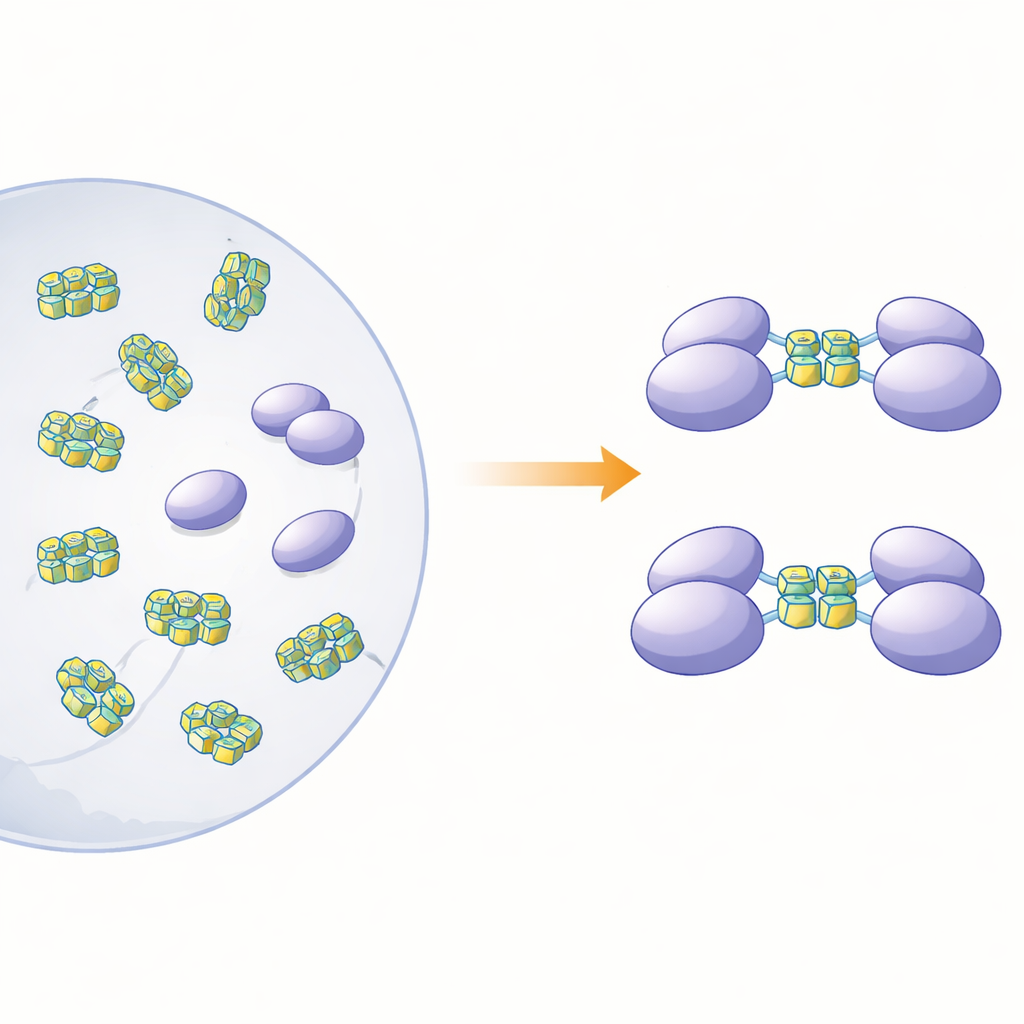
Para esclarecer como a forma física dessa proteína se relaciona com seu papel de detecção, os autores produziram hnRNP A2/B1 de comprimento total e várias versões encurtadas em bactérias. Ao examinar a proteína de comprimento total em solução, constataram que ela não se comportava como partículas limpas e separadas. Em vez disso, formava grandes grumos irregulares — “agregados amorfos solúveis” — que eram instáveis e propensos à precipitação. Em contraste, três versões truncadas que careciam de diferentes trechos na extremidade da cauda permaneceram como moléculas únicas ordenadas (monômeros) em solução. Previsões estruturais por computador sugeriram que cerca de três quartos de hnRNP A2/B1 são compostos por segmentos flexíveis e desordenados, especialmente perto das extremidades. Essas regiões móveis parecem promover a agregação e ajudam a explicar por que tem sido tão difícil obter cristais da proteína para estudos estruturais de alta resolução.
DNA semelhante ao viral que faz proteínas se emparelhar
Os pesquisadores então perguntaram que tipos de DNA os fragmentos monoméricos ligariam, e o que essa ligação faria com o estado da proteína. Eles se concentraram em segmentos de DNA de fita simples que podem se dobrar em G‑quadruplexes — pilhas compactas formadas por sequências ricas em guanina que curvam a fita em uma estrutura apertada em forma de U. Essas formas estão espalhadas pelos genomas de muitos vírus e de genes relacionados ao câncer. Usando calorimetria e testes de ligação baseados em gel, a equipe mostrou que um fragmento, abrangendo as chamadas regiões RRM e RGG (resíduos 15–250), liga fortemente DNA de fita simples, mas não a forma dupla correspondente. Experimentos de separação por tamanho e ultracentrifugação revelaram um efeito marcante: quando esse fragmento encontrou DNA G‑quadruplex de 12 ou 22 bases, duas cópias do fragmento proteico se juntaram para formar um dímero, mas DNA não‑quadruplex não desencadeou esse pareamento.
Espiando uma interface flexível
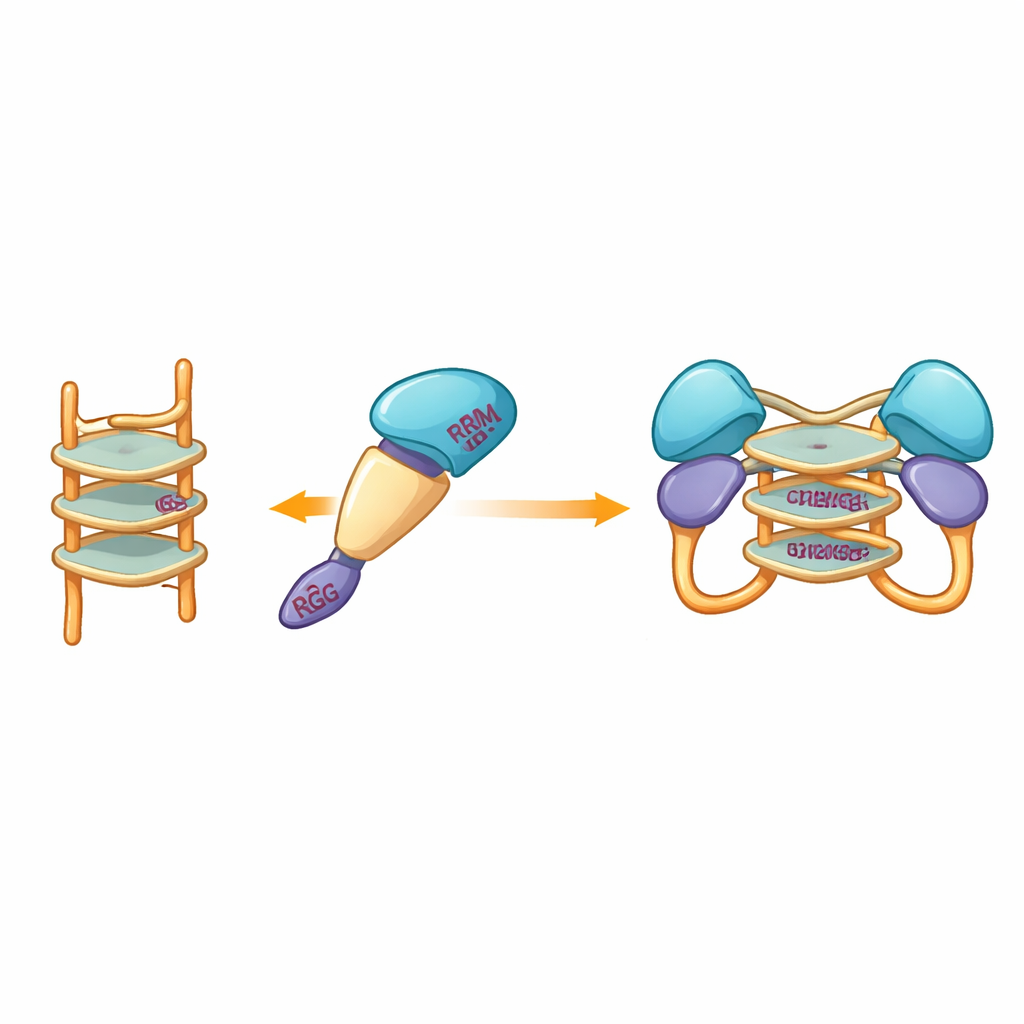
Como tentativas experimentais de cristalografia falharam repetidamente, a equipe recorreu à modelagem computacional para visualizar como o fragmento proteico poderia abraçar um G‑quadruplex. Modelos construídos com ferramentas modernas de predição sugeriram que os domínios centrais mais rígidos de hnRNP A2/B1 acomodam a estrutura de DNA empilhada, enquanto segmentos desordenados circundantes permanecem móveis. Simulações de docking destacaram um conjunto de aminoácidos específicos de vários domínios que poderiam formar ligações de hidrogênio com o G‑quadruplex, estabilizando um complexo dimérico no qual duas moléculas da proteína compartilham o mesmo segmento de DNA. Notavelmente, esses resíduos interagentes diferem daqueles usados por parentes próximos de hnRNP A2/B1, sugerindo que essa proteína evoluiu uma maneira única de reconhecer DNA em G‑quadruplex.
Do pareamento de proteínas à defesa antiviral
Em conjunto, os achados mostram que, enquanto hnRNP A2/B1 de comprimento total tende a se aglomerar em agregados instáveis, versões cuidadosamente aparadas se comportam como moléculas únicas ordenadas que podem se emparelhar quando encontram DNA em G‑quadruplex. Essa formação controlada de dímeros, impulsionada especificamente por sequências de fita simples ricas em guanina abundantes em muitos genomas virais, sugere um passo físico plausível em como a proteína detecta DNA invasor e ajuda a ativar vias de sinalização antiviral. Embora esses resultados tenham sido obtidos em tubos de ensaio e ainda precisem ser confirmados em células vivas e modelos de infecção, eles fornecem uma imagem mais clara e concreta de como mudanças na montagem proteica podem estar ligadas ao sistema de alerta precoce da célula contra vírus — e oferecem um roteiro para projetar pequenas moléculas que possam modular essa resposta em terapias futuras.
Citação: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Palavras-chave: hnRNP A2/B1, DNA G-quadruplex, detecção de DNA, imunidade antiviral, dimerização de proteínas