Clear Sky Science · pl
Rozpoznawanie molekularne i indukowana dymeryzacja fragmentów hnRNP A2/B1 przez jednoniciowe DNA G-kwadrupleksowe
Jak komórki wykrywają wirusowe DNA
Wirusy pozostawiają ślady swojego materiału genetycznego wewnątrz naszych komórek, a organizm musi szybko rozpoznać te ślady, by uruchomić obronę. W niniejszym badaniu analizowano, jak jedno z obficie występujących białek komórkowych, hnRNP A2/B1, może pomagać wykrywać nietypowe kształty DNA typowe dla wielu wirusów. Zrozumienie, jak to białko zmienia swoją formę po związaniu takiego DNA, może położyć podwaliny pod nowe strategie przeciwwirusowe i przeciwnowotworowe.
Sensor kształtu w jądrze komórkowym
HnRNP A2/B1 jest powszechnie znane jako białko wspomagające przetwarzanie RNA, roboczej kopii informacji genetycznej. Występuje głównie w jądrze komórkowym i bierze udział w szeregu kluczowych zadań — od składania (splicingu) komunikatów RNA po kontrolę ich stabilności. Ostatnie badania ujawniły jednak drugą rolę tego białka: może ono działać jako sensor obcego DNA pochodzącego z wirusów. Gdy wirusowe DNA trafia do jądra, hnRNP A2/B1 uczestniczy w uruchamianiu wrodzonych sygnałów odpornościowych, które prowadzą do wytwarzania przeciwwirusowych cząsteczek zwanych interferonami.
Rozplątywanie zagregowanego białka
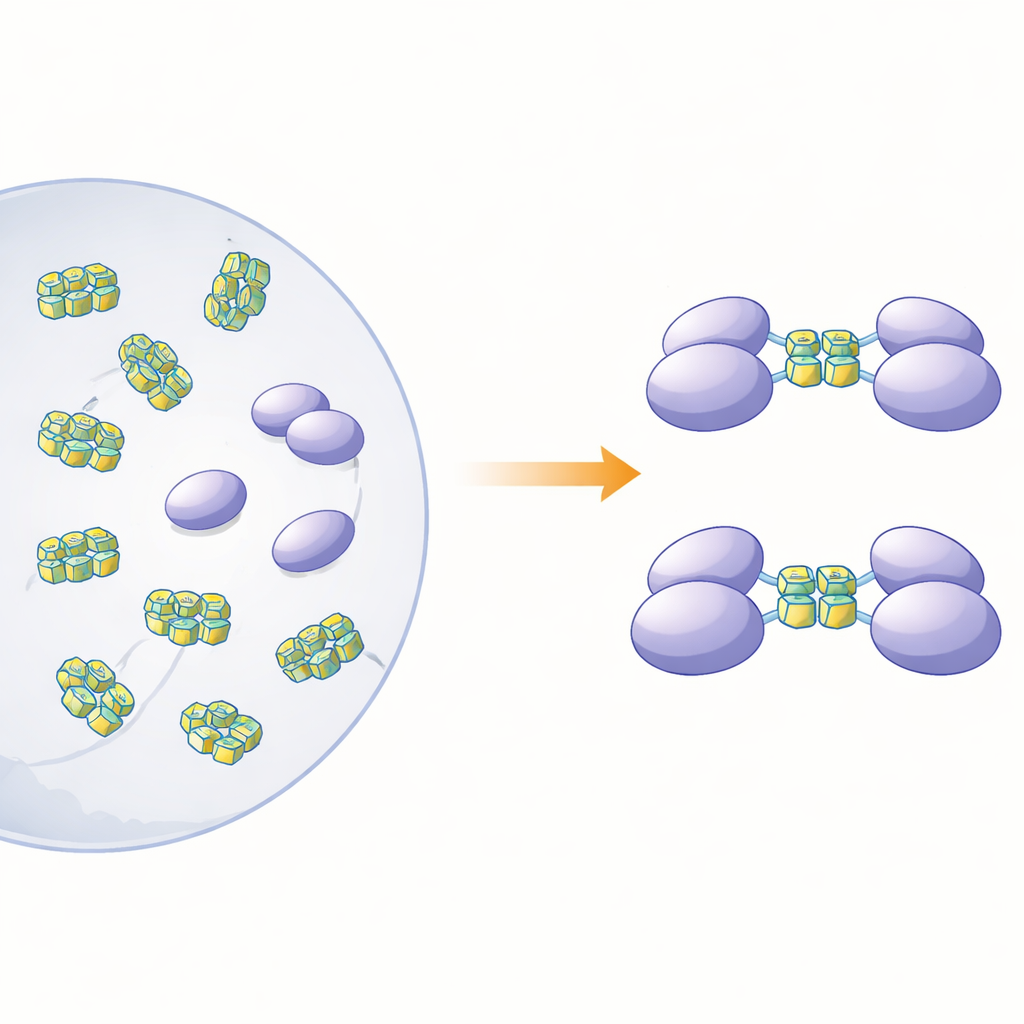
Aby wyjaśnić, w jaki sposób fizyczna postać tego białka wiąże się z jego rolą sensoryczną, autorzy wytworzyli pełnej długości hnRNP A2/B1 oraz kilka skróconych wersji w bakteriach. Badanie białka w roztworze wykazało, że pełnej długości forma nie zachowuje się jak pojedyncze, odseparowane cząsteczki. Zamiast tego tworzyła duże, nieregularne skupiska — „rozpuszczalne amorficzne agregaty” — które były niestabilne i podatne na dalszą precypitację. W przeciwieństwie do tego trzy skrócone wersje pozbawione różnych fragmentów na końcu ogonowym pozostawały w roztworze jako porządkowe pojedyncze cząsteczki (monomery). Predykcje struktury oparte na obliczeniach sugerowały, że około trzech czwartych hnRNP A2/B1 składa się z giętkich, nieuporządkowanych segmentów, zwłaszcza przy końcach. Te elastyczne regiony wydają się sprzyjać agregacji i pomagają wyjaśnić, dlaczego uzyskanie kryształów białka do badań o wysokiej rozdzielczości było tak trudne.
Wirusopodobne DNA, które powoduje parowanie białek
Następnie badacze sprawdzili, jakie rodzaje DNA będą wiązać monomeryczne fragmenty i co to wiązanie robi ze stanem białka. Skoncentrowali się na jednoniciowych segmentach DNA, które mogą fałdować się w G‑kwadrupleksy — zwarte stosy tworzone przez sekwencje bogate w guaninę, które zaginają nić w ciasną, literę U przypominającą strukturę. Takie kształty występują w genomach wielu wirusów i genach związanych z rakiem. Za pomocą kalorymetrii i testów wiązania opartych na żelach zespół wykazał, że jeden z fragmentów, obejmujący tzw. regiony RRM i RGG (reszidu 15–250), silnie wiąże jednoniciowe DNA, ale nie odpowiadający mu dwuniciowy kształt. Doświadczenia z separacją według rozmiaru i ultrawirowaniem ujawniły uderzający efekt: gdy ten fragment zetknął się z G‑kwadrupleksem z 12 lub 22 zasad, dwie kopie fragmentu białka łączyły się, tworząc dimer, podczas gdy DNA nie tworzące kwadrupleksu nie wywoływało takiego parowania.
Zaglądanie w elastyczne centrum interakcji
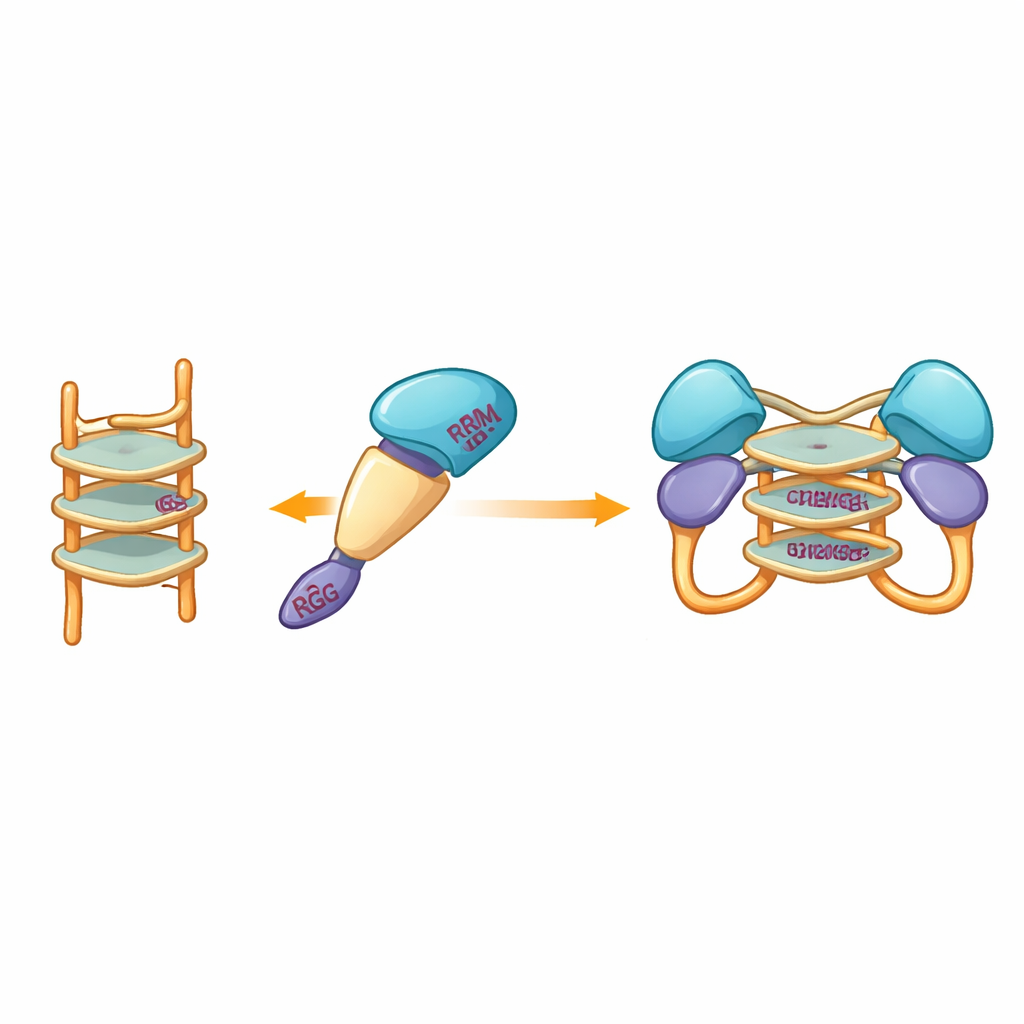
Ponieważ eksperymentalne próby krystalizacji wielokrotnie nie powiodły się, zespół zwrócił się ku modelowaniu komputerowemu, by zobrazować, jak fragment białka mógłby objąć G‑kwadrupleks. Modele zbudowane przy użyciu nowoczesnych narzędzi predykcyjnych sugerowały, że bardziej sztywne, centralne domeny hnRNP A2/B1 okalają ułożoną strukturę DNA, podczas gdy otaczające je nieuporządkowane segmenty pozostają ruchome. Symulacje dokowania wskazały zestaw specyficznych aminokwasów z kilku domen, które mogą tworzyć wiązania wodorowe z G‑kwadrupleksem, stabilizując kompleks dimerowy, w którym dwie cząsteczki białka dzielą ten sam fragment DNA. Co istotne, te oddziałujące reszidy różnią się od używanych przez bliskich krewniaków hnRNP A2/B1, co sugeruje, że to białko wyewoluowało unikalny sposób rozpoznawania DNA typu G‑kwadrupleks.
Od parowania białek do obrony przeciwwirusowej
Podsumowując, wyniki pokazują, że podczas gdy pełnej długości hnRNP A2/B1 ma skłonność do tworzenia niestabilnych agregatów, starannie przycięte wersje zachowują się jak uporządkowane pojedyncze cząsteczki, które mogą się parować po zetknięciu z G‑kwadrupleksem. Ta kontrolowana dimeryzacja, wywoływana specyficznie przez sekwencje jednoniciowe bogate w guaninę występujące w wielu genomach wirusów, sugeruje prawdopodobny fizyczny etap w mechanizmie, dzięki któremu białko wykrywa obce DNA i pomaga włączać ścieżki sygnałowe odpowiedzi przeciwwirusowej. Chociaż wyniki uzyskano w probówkach i wciąż wymagają potwierdzenia w żywych komórkach i modelach infekcji, dostarczają one wyraźniejszego, bardziej konkretnego obrazu tego, jak zmiany w organizacji białek mogą wiązać się z wcześniejszym systemem alarmowym komórki przeciw wirusom — oraz pokazują drogę do projektowania małych cząsteczek, które w przyszłości mogłyby modulować tę odpowiedź w terapii.
Cytowanie: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Słowa kluczowe: hnRNP A2/B1, DNA G-kwadrupleksowe, wykrywanie DNA, odporność przeciwwirusowa, dimeryzacja białek