Clear Sky Science · ar
التعرف الجزيئي والتضاعف المستحث لجزيئات hnRNP A2/B1 المقتطعة بواسطة حمض نووي أحادي الشريط بشكل رباعي الجوانين
كيف تكتشف الخلايا الحمض النووي الفيروسي
تترك الفيروسات آثاراً من مادتها الوراثية داخل خلايانا، ويجب على الجسم التعرف على هذه الآثار بسرعة ليدفع دفاعاً مناسباً. تستكشف هذه الدراسة كيف قد يساعد بروتين خلوي وفير، hnRNP A2/B1، في استشعار أشكال غير اعتيادية من الحمض النووي التي توجد في كثير من الفيروسات. من خلال فهم كيفية تغيير هذا البروتين لشكله عند ارتباطه بمثل هذا الحمض النووي، يأمل الباحثون في وضع أسس لاستراتيجيات جديدة مضادة للفيروسات والسرطان.
بروتين حساس للشكل داخل النواة
يشتهر hnRNP A2/B1 بدوره المساعد في إدارة الرنا، النسخة العاملة من المعلومات الجينية. يعيش هذا البروتين أساساً في نواة الخلية ويشارك في مجموعة من الوظائف الأساسية، من تقطيع الرنا إلى التحكم في ثبات رسائل الرنا. أظهرت أعمال حديثة، مع ذلك، حياة ثانية لهذا البروتين: يمكن أن يعمل كمستشعر للحمض النووي الأجنبي القادم من فيروسات غازية. عندما يدخل الحمض النووي الفيروسي إلى النواة، يشارك hnRNP A2/B1 في تشغيل إشارات المناعة الفطرية التي تحفز إنتاج جزيئات مضادة للفيروسات تُسمى الإنترفيرونات.
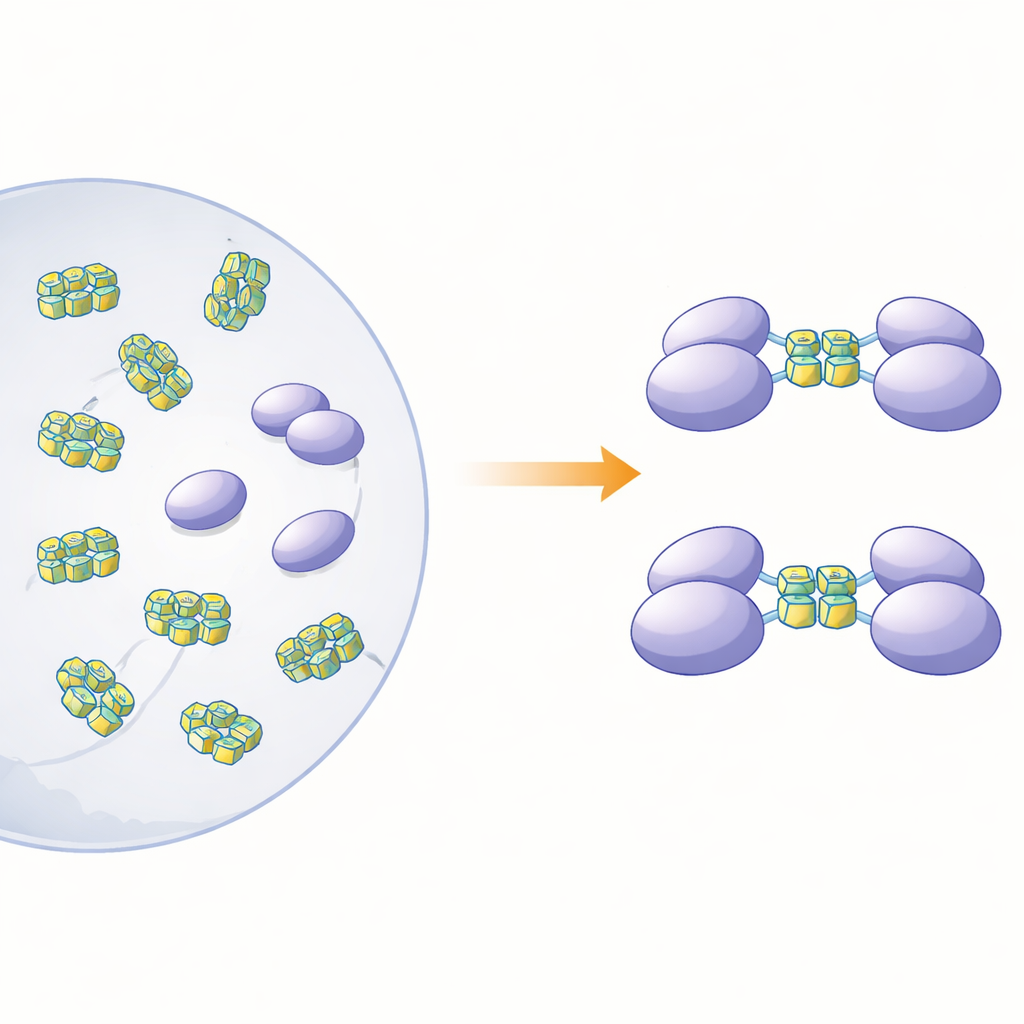
تفكيك بروتين متماثل التجمع
لتوضيح كيف يرتبط الشكل الفيزيائي لهذا البروتين بدوره الحسي، أنتج المؤلفون hnRNP A2/B1 بطوله الكامل وعدة نسخ مختصرة في بكتيريا. عند فحصهم للبروتين الكامل في المحلول، وجدوا أنه لا يتصرف كجزيئات منفصلة ومرتبة. بل شكل كتلات كبيرة وغير منتظمة — «تجمعات ذائبة غير بلورية» — كانت غير مستقرة وعرضة للاحتماء. في المقابل، بقت ثلاث نسخ مقتطعة تفتقر إلى أجزاء مختلفة من الطرف الخلفي للبروتين كجزيئات منفردة (مونومرات) في المحلول. أشارت تنبؤات هيكلية معتمدة على الحاسوب إلى أن نحو ثلاثة أرباع hnRNP A2/B1 يتألف من مقاطع رخوة ومضطربة، خصوصاً بالقرب من أطرافه. تبدو هذه المناطق المرنة مشجعة على التجمع وتساعد في تفسير صعوبة الحصول على بلورات للبروتين لدراسات هيكلية عالية الدقة.
حمض نووي شبيه بالفيروسي يجبر البروتين على الاقتران
سأل الباحثون بعد ذلك أي أنماط من الحمض النووي سترتبط بالشظايا المونومرية، وماذا سيفعل هذا الارتباط بحالة البروتين. ركزوا على مقاطع من الحمض النووي أحادي الشريط التي يمكنها أن تطوى إلى رباعيات جوانين — تراصات مدمجة تتشكل من مقاطع غنية بالغوانين تُثني الشريط إلى بنية ضيقة على شكل حرف U. تتوزع مثل هذه الأشكال في أنحاء جينومات العديد من الفيروسات وجينات مرتبطة بالسرطان. باستخدام المعايرة الحرارية واختبارات الترابط على الهلام، أظهر الفريق أن شظية واحدة، تغطي مناطق تُسمى RRM وRGG (البقايا 15–250)، ترتبط بقوة بالحمض النووي أحادي الشريط ولكن ليس بالشكل المزدوج المماثل. كشفت تجارب فصل حسب الحجم والطرد المركزي فائق السرعة تأثيراً لافتاً: عندما واجهت هذه الشظية حمضاً نووياً رباعي الجوانين طوله 12 أو 22 قاعدة، انضمت نسختان من شظية البروتين معاً لتشكلا ثنائياً (دايمر)، بينما لم تحفز الحمض النووي غير الرباعي هذا الاقتران.
التطلع إلى واجهة مرنة
ولأن محاولات التبلور التجريبية فشلت مراراً، لجأ الفريق إلى النمذجة الحاسوبية لتصوير كيف قد يحتضن شظية البروتين رباعية الجوانين. اقترحت النماذج المبنية بأدوات التنبؤ الحديثة أن المجالات الوسطية الأكثر صلابة في hnRNP A2/B1 تحيط بالهيكل المكدس للحمض النووي، بينما تبقى المقاطع المضطربة المحيطة متحركة. أبرزت محاكيات الالتحام مجموعة من الأحماض الأمينية المحددة من عدة نطاقات قد تشكل روابط هيدروجينية مع رباعية الجوانين، مثبتةً مركباً ثنائياً تشارك فيه جزيئتا بروتين نفس مقطع الحمض النووي. ومن اللافت أن بقايا التفاعل هذه تختلف عن تلك التي تستخدمها أقارب قريبة من hnRNP A2/B1، مما يوحي بأن هذا البروتين طوّر طريقة فريدة للتعرف على حمض نووي رباعي الجوانين.
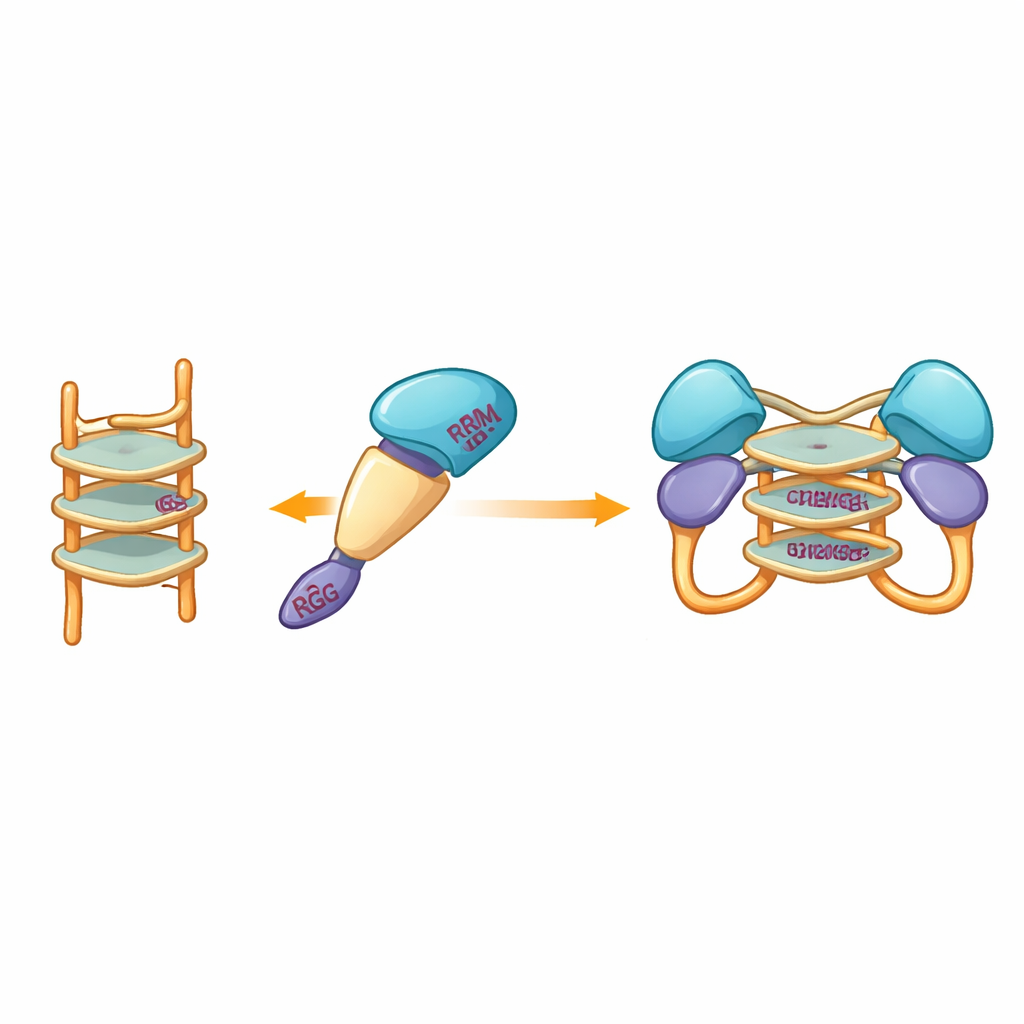
من اقتران البروتين إلى الدفاع المضاد للفيروسات
تُظهر النتائج مجتمعة أنه بينما يميل hnRNP A2/B1 الكامل الطول إلى التجمع في كتلات غير مستقرة، تتصرف النسخ المقتطعة بعناية كجزيئات منفردة مرتبة يمكن أن تقترن عندما تواجه حمضاً نووياً رباعي الجوانين. يشير هذا التشكّل المتحكم للتثنّي، المُحرَّك تحديداً بتسلسلات أحادية الشريط الغنية بالجوانين الشائعة في جينومات العديد من الفيروسات، إلى خطوة فيزيائية معقولة في كيفية استشعار البروتين للحمض النووي الغازي والمساعدة في تشغيل مسارات الإشارة المضادة للفيروسات. على الرغم من أن هذه النتائج حُصل عليها في أنابيب الاختبار وتحتاج إلى تأكيد في خلايا حية ونماذج الإصابة، فإنها تقدم صورة أوضح وأكثر ملموسية عن كيفية ارتباط تغيرات تركيب البروتين بنظام الإنذار المبكر في الخلية ضد الفيروسات — وتوفر خارطة طريق لتصميم جزيئات صغيرة قد تضبط هذا الاستجابة في علاجات مستقبلية.
الاستشهاد: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
الكلمات المفتاحية: hnRNP A2/B1, حمض نووي رباعي الجوانين, استشعار الحمض النووي, المناعة المضادة للفيروسات, تزاوج البروتينات