Clear Sky Science · it
Riconoscimento molecolare e dimerizzazione indotta di troncamenti di hnRNP A2/B1 da parte di DNA a singolo filamento a G-quadruplex
Come le cellule individuano il DNA virale
I virus lasciano tracce del loro materiale genetico all’interno delle nostre cellule, e l’organismo deve riconoscere rapidamente queste tracce per attivare una difesa. Questo studio esplora come una proteina cellulare abbondante, hnRNP A2/B1, possa aiutare a rilevare forme di DNA insolite comuni a molti virus. Capire come questa proteina cambi la propria conformazione quando si lega a tali DNA può gettare le basi per nuove strategie antivirali e antitumorali.
Una proteina sensibile alle forme nel nucleo
HnRNP A2/B1 è nota soprattutto come proteina ausiliaria che gestisce l’RNA, la copia operativa dell’informazione genetica. Risiede principalmente nel nucleo cellulare e partecipa a molte funzioni essenziali, dallo splicing dei messaggi di RNA al controllo della loro stabilità. Studi recenti, tuttavia, hanno rivelato una seconda vita per questa proteina: può agire come sensore del DNA estraneo proveniente da virus invasori. Quando il DNA virale entra nel nucleo, hnRNP A2/B1 contribuisce ad attivare segnali immunitari innati che scatenano la produzione di molecole antivirali chiamate interferoni.
Disvelare una proteina aggregata
Per chiarire come la forma fisica di questa proteina si relazioni al suo ruolo di sensore, gli autori hanno prodotto hnRNP A2/B1 a lunghezza completa e diverse versioni accorciate in batteri. Analizzando la proteina a lunghezza intera in soluzione, hanno scoperto che non si comportava come particelle nette e separate. Piuttosto, formava grandi ammassi irregolari — «aggregati amorfi solubili» — instabili e inclini a ulteriore precipitazione. Invece, tre versioni troncate prive di diverse porzioni nella coda della proteina rimasero come molecole ordinate e singole (monomeri) in soluzione. Previsioni strutturali via computer suggerirono che circa tre quarti di hnRNP A2/B1 è costituito da segmenti flessuosi e disordinati, specialmente vicino agli estremi. Queste regioni flessibili sembrano favorire l’aggregazione e aiutano a spiegare perché è stato così difficile ottenere cristalli della proteina per studi strutturali ad alta risoluzione.
DNA simile a quello virale che induce l’accoppiamento delle proteine
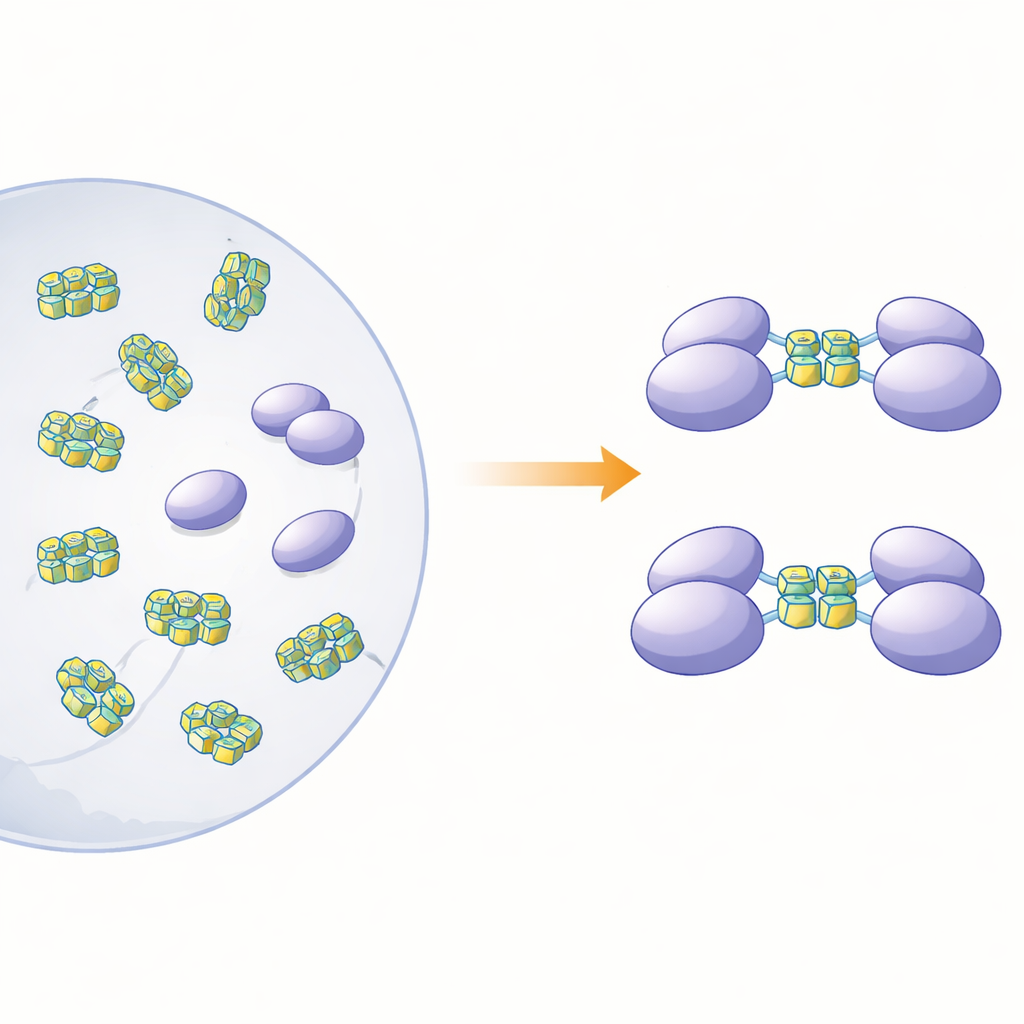
I ricercatori hanno poi chiesto a quali tipi di DNA si legherebbero i frammenti monomerici e cosa quel legame farebbe allo stato della proteina. Si sono concentrati su segmenti di DNA a singolo filamento che possono ripiegarsi in G-quadruplex — pile compatte formate da sequenze ricche di guanine che piegano il filamento in una struttura a U compatta. Queste forme sono diffuse nei genomi di molti virus e in geni legati al cancro. Usando calorimetria e saggi di legame su gel, il team ha mostrato che un frammento, che comprende le regioni note come RRM e RGG (residui 15–250), si lega fortemente al DNA a singolo filamento ma non alla corrispondente forma a doppio filamento. Esperimenti di separazione in base alla dimensione e ultracentrifugazione hanno rivelato un effetto notevole: quando questo frammento incontrava DNA a G-quadruplex di 12 o 22 basi, due copie del frammento proteico si univano per formare un dimero, mentre il DNA non-quadruplex non innescava questo accoppiamento.
Un’interfaccia flessibile sotto la lente
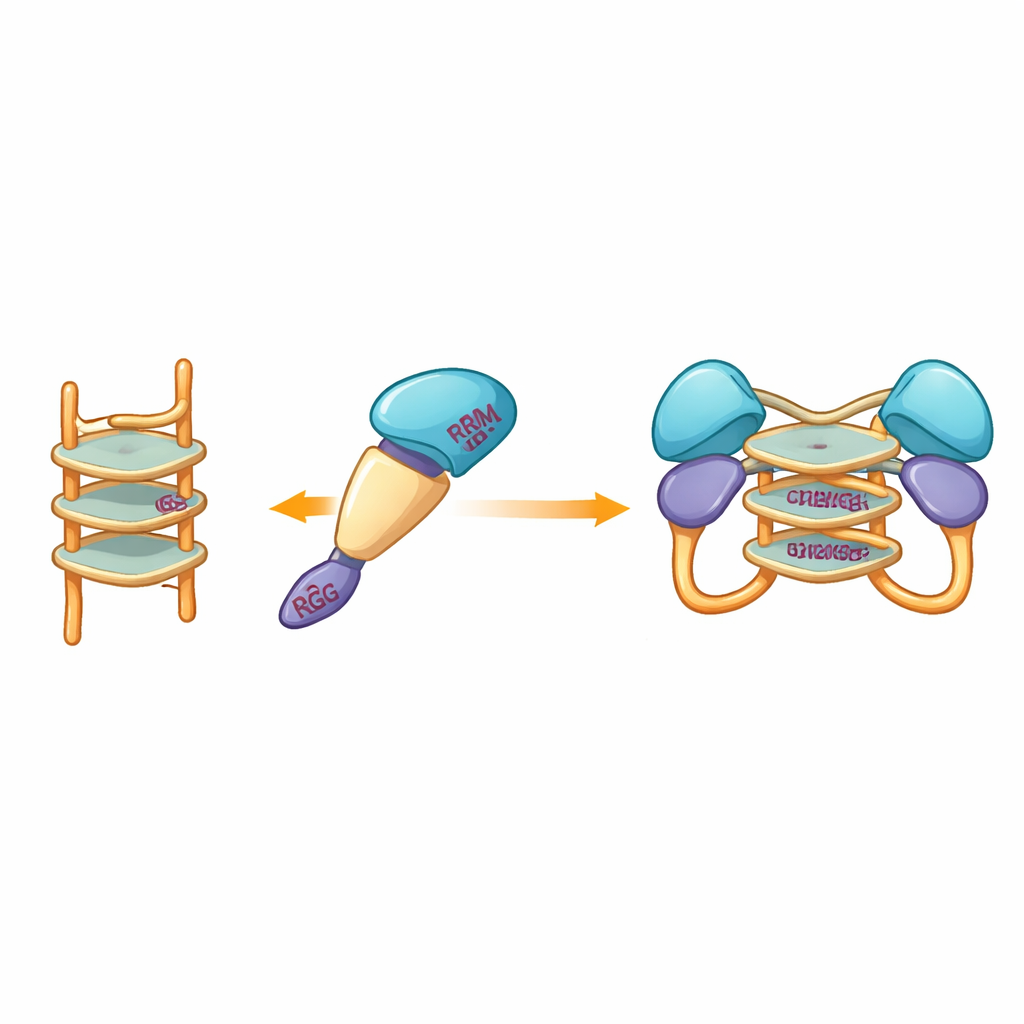
Poiché i tentativi sperimentali di cristallografia fallivano ripetutamente, il team si è rivolto alla modellizzazione computazionale per visualizzare come il frammento proteico potesse avvolgere un G-quadruplex. Modelli costruiti con strumenti moderni di predizione suggerivano che i domini centrali più rigidi di hnRNP A2/B1 accolgono la struttura a pile del DNA, mentre i segmenti disordinati circostanti rimangono mobili. Simulazioni di docking hanno evidenziato un insieme di amminoacidi specifici di diversi domini che potrebbero formare legami a idrogeno con il G-quadruplex, stabilizzando un complesso dimerico in cui due molecole proteiche condividono lo stesso segmento di DNA. Notevolmente, questi residui interagenti differiscono da quelli usati da stretti parenti di hnRNP A2/B1, suggerendo che questa proteina abbia evoluto un modo unico di riconoscere il DNA a G-quadruplex.
Dall’accoppiamento proteico alla difesa antivirale
Nel complesso, i risultati mostrano che mentre hnRNP A2/B1 a lunghezza intera tende ad ammassi instabili, versioni opportunamente tagliate si comportano come molecole ordinate che possono accoppiarsi quando incontrano DNA a G-quadruplex. Questa formazione controllata del dimero, guidata specificamente da sequenze a singolo filamento ricche di guanine abbondanti in molti genomi virali, suggerisce un passaggio fisico plausibile nel modo in cui la proteina rileva il DNA invasore e contribuisce ad attivare le vie di segnalazione antivirale. Sebbene questi risultati siano stati ottenuti in provetta e debbano ancora essere confermati in cellule viventi e modelli di infezione, offrono un quadro più chiaro e concreto di come i cambiamenti nell’assemblaggio proteico possano essere legati al sistema di allerta precoce della cellula contro i virus — e indicano una strada per progettare piccole molecole che potrebbero modulare questa risposta in future terapie.
Citazione: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Parole chiave: hnRNP A2/B1, DNA a G-quadruplex, rilevamento del DNA, immunità antivirale, dimerizzazione proteica