Clear Sky Science · sv
Molekylär igenkänning och inducerad dimerisering av hnRNP A2/B1-trunkeringar av G-quadruplex enkelsträngat DNA
Hur celler upptäcker viralt DNA
Virus lämnar spår av sitt genetiska material inne i våra celler, och kroppen måste snabbt känna igen dessa spår för att sätta igång ett försvar. Denna studie undersöker hur ett vanligt förekommande cellulärt protein, hnRNP A2/B1, kan hjälpa till att känna av ovanliga DNA-strukturer som är vanliga i många virus. Genom att förstå hur detta protein ändrar form när det binder till sådant DNA hoppas forskarna lägga grunden för nya antivirala och anticancerstrategier.
En formkännande protein i kärnan
HnRNP A2/B1 är mest känd som ett hjälpande protein som hanterar RNA, den arbetande kopian av genetisk information. Det lever främst i cellkärnan och deltar i en rad viktiga uppgifter, från splitsning av RNA-meddelanden till att reglera deras stabilitet. Nyare arbete har dock visat att proteinet har ett andra skede: det kan fungera som en sensor för främmande DNA från invaderande virus. När viralt DNA kommer in i kärnan deltar hnRNP A2/B1 i att slå på medfödda immunsignaler som triggar produktionen av antivirala molekyler kallade interferoner.
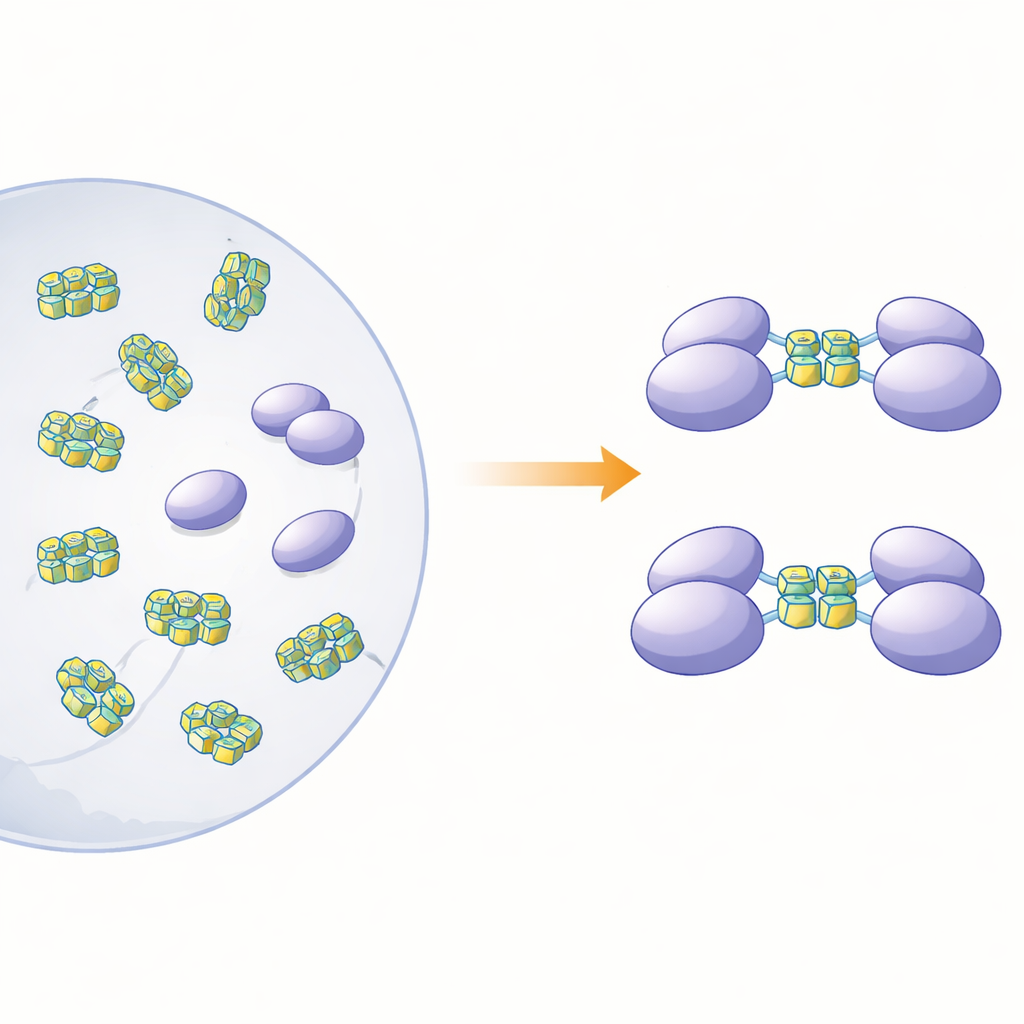
Att nysta upp ett aggregerat protein
För att klargöra hur proteinets fysiska form hänger samman med dess sensoriska roll framställde författarna fullängds hnRNP A2/B1 och flera förkortade versioner i bakterier. När de undersökte fullängdsproteinet i lösning fann de att det inte uppförde sig som prydliga, separata partiklar. Istället bildade det stora, oregelbundna klumpar — ”lösliga amorfa aggregat” — som var instabila och benägna att fälla ut ytterligare. I kontrast förblev tre trunkerade versioner som saknade olika delar i proteinets C-terminala ände ordnade, enskilda molekyler (monomerer) i lösning. Datorbaserade strukturprediktioner antydde att ungefär tre fjärdedelar av hnRNP A2/B1 består av flexibla, oordnade segment, särskilt nära ändarna. Dessa rörliga regioner verkar främja aggregering och bidrar till att förklara varför det varit så svårt att odla kristaller av proteinet för högupplösta strukturella studier.
Viruslikt DNA som får proteiner att para ihop sig
Forskarna frågade sedan vilka slags DNA de monomeriska fragmenten skulle binda till, och vad den bindningen skulle göra med proteinets tillstånd. De fokuserade på enkelsträngade DNA-segment som kan vikas till G-quadruplex — täta staplar bildade av guaninrika sekvenser som böjer tråden till en snäv, U-formad struktur. Sådana former finns spridda i många virusgenom och i gener kopplade till cancer. Med kalorimetri och gellagringsbaserade bindningstester visade teamet att ett fragment, som täcker de så kallade RRM- och RGG-regionerna (rester 15–250), binder starkt till enkelsträngat DNA men inte till motsvarande dubbelsträngade form. Storleksbaserad separation och ultracentrifugeringsförsök avslöjade en slående effekt: när detta fragment mötte G-quadruplex-DNA av 12 eller 22 nukleotider gick två kopior av proteinfragmentet ihop och bildade en dimer, medan icke-quadruplex-DNA inte utlöste denna parning.
In i ett flexibelt gränssnitt
Eftersom experimentella kristallografiförsök upprepade gånger misslyckades vände sig teamet till datormodellering för att visualisera hur proteinfragmentet kan omfamna ett G-quadruplex. Modeller byggda med moderna prediktionsverktyg föreslog att de mer styva centrala domänerna i hnRNP A2/B1 vaggar den staplade DNA-strukturen, medan omkringliggande oordnade segment förblir rörliga. Dockningssimulationer pekade ut en uppsättning specifika aminosyror från flera domäner som skulle kunna bilda vätebindningar med G-quadruplexet och stabilisera ett dimeriskt komplex där två proteinkopior delar samma DNA-segment. Noterbart skiljer sig dessa interagerande rester från dem som används av nära släktingar till hnRNP A2/B1, vilket antyder att detta protein utvecklat ett unikt sätt att känna igen G-quadruplex-DNA.
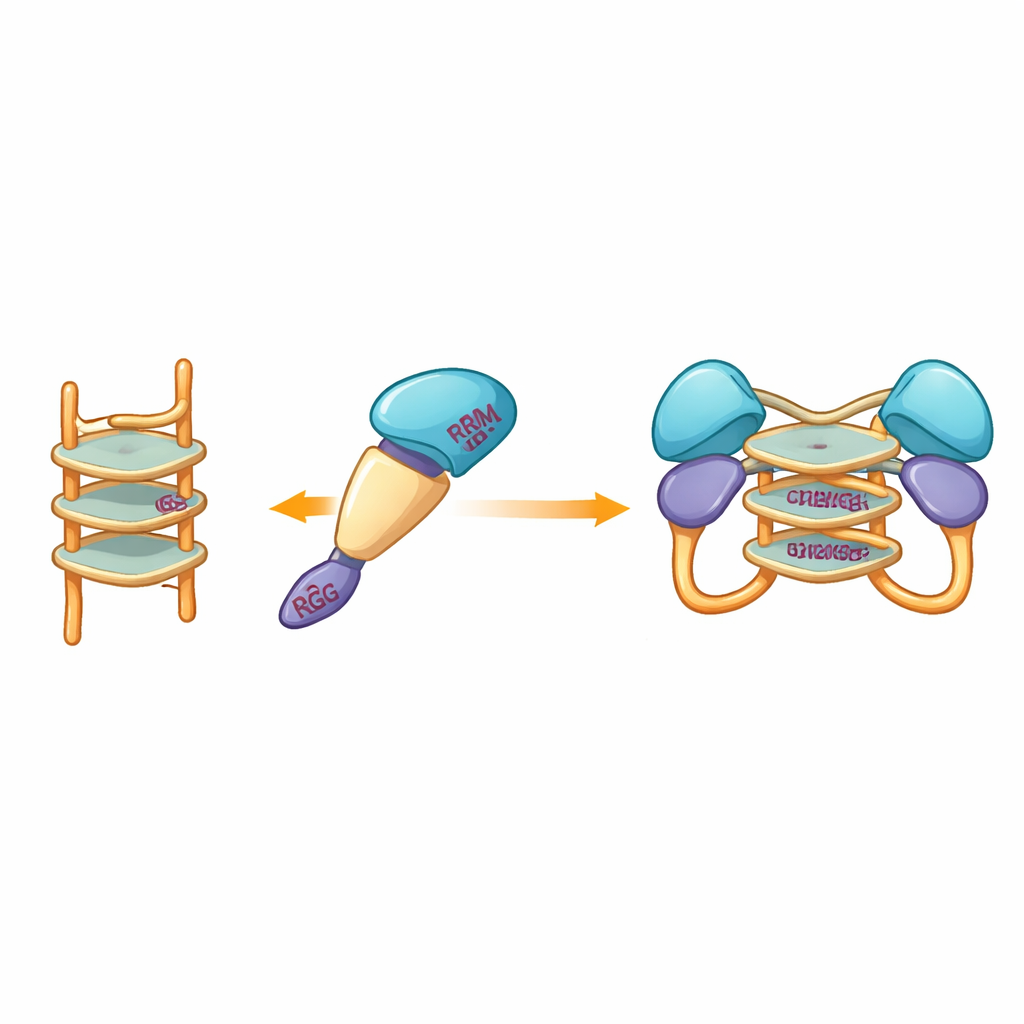
Från proteinparning till antiviralt försvar
Sammantaget visar fynden att medan fullängds hnRNP A2/B1 tenderar att klumpa ihop sig till instabila aggregat, beter sig noggrant trimmande versioner som ordnade enkelmolekyler som kan para ihop sig när de möter G-quadruplex-DNA. Denna kontrollerade dimerbildning, driven specifikt av guaninrika enkelsträngade sekvenser som är vanliga i många virusgenom, föreslår ett troligt fysikaliskt steg i hur proteinet känner av invaderande DNA och hjälper till att slå på antivirala signalvägar. Även om dessa resultat erhölls i provrör och fortfarande behöver bekräftas i levande celler och infektionsmodeller, ger de en tydligare, mer konkret bild av hur förändringar i proteinets sammankoppling kan kopplas till cellens tidiga varningssystem mot virus — och erbjuder en färdplan för att designa småmolekyler som kan finjustera detta svar i framtida terapier.
Citering: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Nyckelord: hnRNP A2/B1, G-quadruplex DNA, DNA-avkänning, antiviral immunitet, proteindimerisering