Clear Sky Science · ru
Молекулярное распознавание и индуцированная димеризация укороченных вариантов hnRNP A2/B1 белка при связывании с одноцепочечной G-квадруплексной ДНК
Как клетки распознают вирусную ДНК
Вирусы оставляют следы своего генетического материала внутри наших клеток, и организму нужно быстро распознавать эти следы, чтобы выработать защиту. В этом исследовании изучается, как один из распространённых клеточных белков — hnRNP A2/B1 — может помогать обнаруживать необычные формы ДНК, часто встречающиеся у многих вирусов. Поняв, как этот белок меняет свою форму при связывании с такой ДНК, учёные надеются заложить основу для новых антивирусных и противораковых стратегий.
Белок-чувствитель к форме в ядре
HnRNP A2/B1 наиболее известен как вспомогательный белок, участвующий в работе с РНК, рабочей копией генетической информации. Он преимущественно локализуется в ядре клетки и участвует во множестве важных процессов — от сплайсинга РНК до контроля её устойчивости. Последние исследования однако выявили вторую роль этого белка: он может действовать как сенсор чужеродной ДНК из вторгающихся вирусов. Когда вирусная ДНК попадает в ядро, hnRNP A2/B1 участвует в запуске врождённых иммунных сигналов, приводящих к продуцированию антивирусных молекул — интерферонов.
Раскрывая агрегированный белок
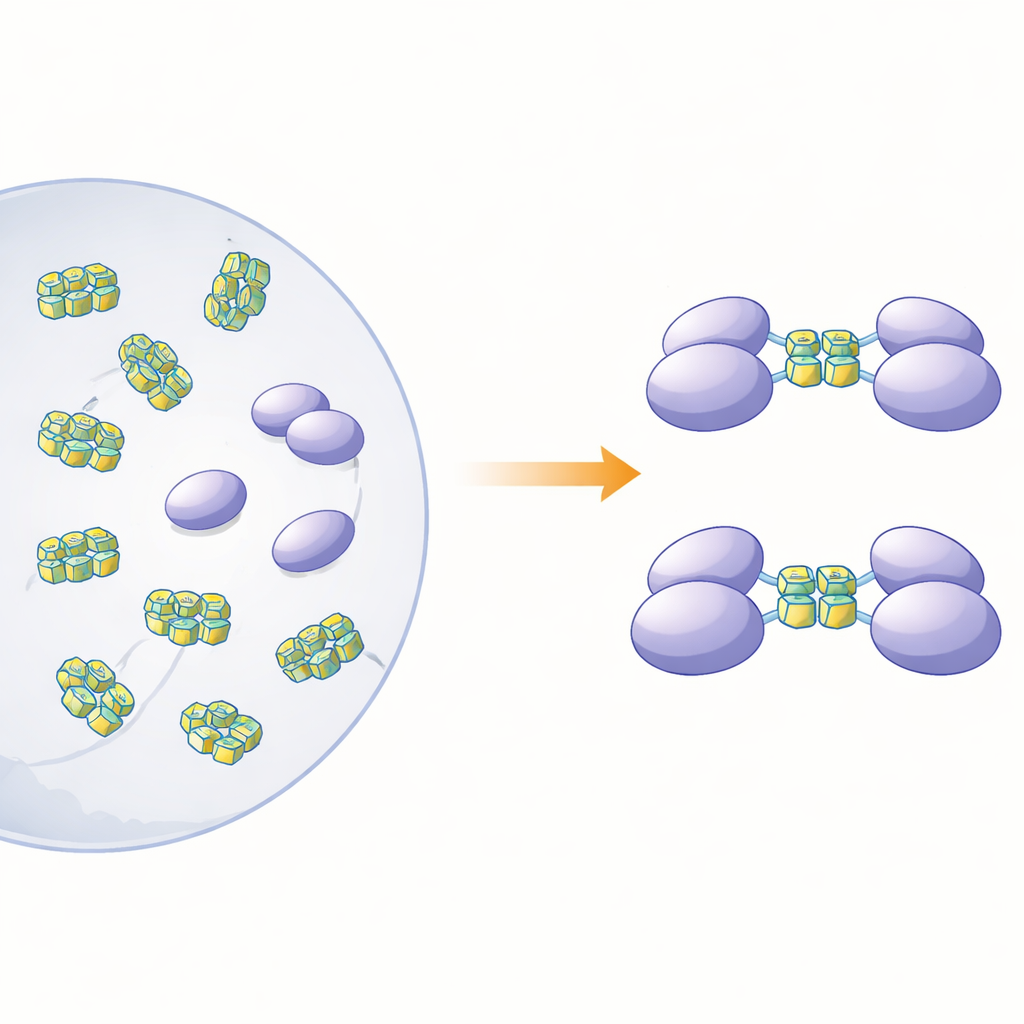
Чтобы прояснить, как физическая форма этого белка связана с его ролью сенсора, авторы получили полноразмерный hnRNP A2/B1 и несколько укороченных вариантов в бактериях. При изучении полноразмерного белка в растворе они обнаружили, что он не ведёт себя как аккуратные отдельные частицы. Вместо этого он образует большие неправильные сгустки — «растворимые аморфные агрегаты» — которые нестабильны и склонны к дальнейшей осадке. Напротив, три укороченных варианта, лишённые разных участков на С-конце белка, оставались в растворе в виде аккуратных одиночных молекул (мономеров). Компьютерные предсказания структуры показали, что примерно три четверти hnRNP A2/B1 состоят из гибких, неупорядоченных фрагментов, особенно у концов. Эти подвижные регионы, по-видимому, способствуют агрегации и помогают объяснить, почему было так трудно получить кристаллы белка для исследования с высоким разрешением.
Вирусоподобная ДНК, заставляющая белки соединяться попарно
Далее исследователи поинтересовались, с какими типами ДНК будут связываться мономерные фрагменты и как это влияет на состояние белка. Они сосредоточились на одноцепочечных сегментах ДНК, способных сворачиваться в G‑квадруплексы — плотные стопки, образуемые гуанин‑богатыми последовательностями, которые изгибают нить в тесную U‑образную структуру. Такие формы встречаются во многих вирусных геномах и в генах, связанных с раком. С помощью калориметрии и гель‑анализов команда показала, что один фрагмент, охватывающий так называемые области RRM и RGG (остатки 15–250), сильно связывается с одноцепочечной ДНК, но не с соответствующей двуцепочечной формой. Эксперименты с разделением по размеру и ультрацентрифугированием выявили поразительный эффект: при контакте этого фрагмента с G‑квадруплексной ДНК длиной 12 или 22 нуклеотида два копии белкового фрагмента соединялись в димер, тогда как не‑квадруплексная ДНК не вызывала такого объединения.
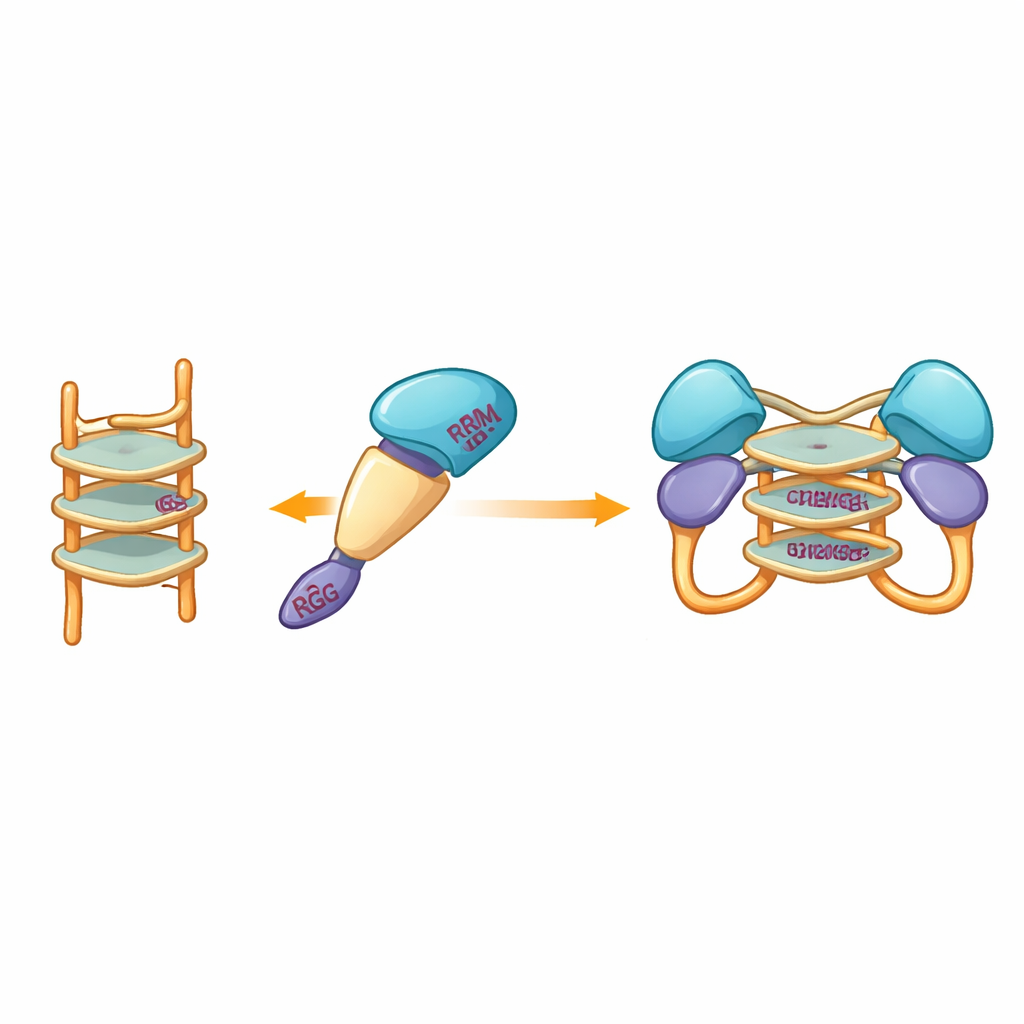
Заглядывая в гибкий интерфейс
Поскольку попытки получить кристаллы экспериментальным путём неоднократно не удавались, команда обратилась к вычислительному моделированию, чтобы визуализировать, как фрагмент белка может охватывать G‑квадруплекс. Модели, построенные с современными инструментами предсказания, предположили, что более жёсткие центральные домены hnRNP A2/B1 обхватывают стопку ДНК, тогда как окружающие их неупорядоченные сегменты остаются подвижными. Моделирование докинга выделило набор специфических аминокислот из нескольких доменов, которые могли бы образовывать водородные связи с G‑квадруплексом, стабилизируя димерный комплекс, в котором две молекулы белка совместно удерживают один и тот же сегмент ДНК. Примечательно, что эти взаимодействующие остатки отличаются от тех, что используются близкими родственниками hnRNP A2/B1, что указывает на то, что этот белок эволюционировал уникальный способ распознавания G‑квадруплексной ДНК.
От парообразования белков к антивирусной защите
В совокупности результаты показывают, что в то время как полноразмерный hnRNP A2/B1 склонен собираться в нестабильные агрегаты, аккуратно подрезанные варианты ведут себя как упорядоченные одиночные молекулы, которые могут попарно соединяться при встрече с G‑квадруплексной ДНК. Это контролируемое образование димеров, вызванное специфически гуанин‑богатыми одноцепочечными последовательностями, распространёнными во многих вирусных геномах, предлагает правдоподобный физический шаг в том, как белок распознаёт внедряющуюся ДНК и способствует включению антивирусных сигнальных путей. Хотя эти результаты получены в пробирке и ещё требуют подтверждения в живых клетках и моделях инфекции, они дают более ясную и конкретную картину того, как изменения в сборке белков могут быть связаны с ранней системой оповещения клетки против вирусов — и предлагают дорожную карту для разработки малых молекул, которые в будущем могли бы регулируровать эту реакцию в терапиях.
Цитирование: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Ключевые слова: hnRNP A2/B1, G-квадруплексная ДНК, распознавание ДНК, антивирусный иммунитет, димеризация белков