Clear Sky Science · tr
hnRNP A2/B1 kesintilerinin moleküler tanınması ve G-katradört tek iplikli DNA ile indüklenen dimerizasyonu
Hücreler Viral DNA’yı Nasıl Fark Eder
Virüsler, genetik materyallerinin izlerini hücrelerimizin içine bırakır ve vücut bir savunma başlatmak için bu izleri hızla tanımalıdır. Bu çalışma, hücrede bol bulunan bir proteinin, hnRNP A2/B1’in, birçok virüste yaygın olan sıra dışı DNA şekillerini algılamaya nasıl yardımcı olabileceğini inceliyor. Bu proteinin böyle bir DNA’ya bağlandığında formunun nasıl değiştiğini anlamak, araştırmacıların yeni antiviral ve antikanser stratejilerinin temelini atmalarına yardımcı olabilir.
Çekirdekte Şekil Algılayan Bir Protein
HnRNP A2/B1, genetik bilginin çalışan kopyası olan RNA’yı yöneten yardımcı bir protein olarak en iyi bilinir. Başlıca hücre çekirdeğinde bulunur ve RNA’nın kesilmesinden kararlılığının kontrolüne kadar birçok temel göreve katılır. Ancak son çalışmalar bu proteinin ikinci bir hayatını ortaya koydu: konukçı virüslerden gelen yabancı DNA için bir sensör olarak işlev görebilir. Viral DNA çekirdeğe girdiğinde, hnRNP A2/B1 interferon adı verilen antiviral moleküllerin üretimini tetikleyen doğuştan gelen bağışıklık sinyallerinin açılmasına katılır.
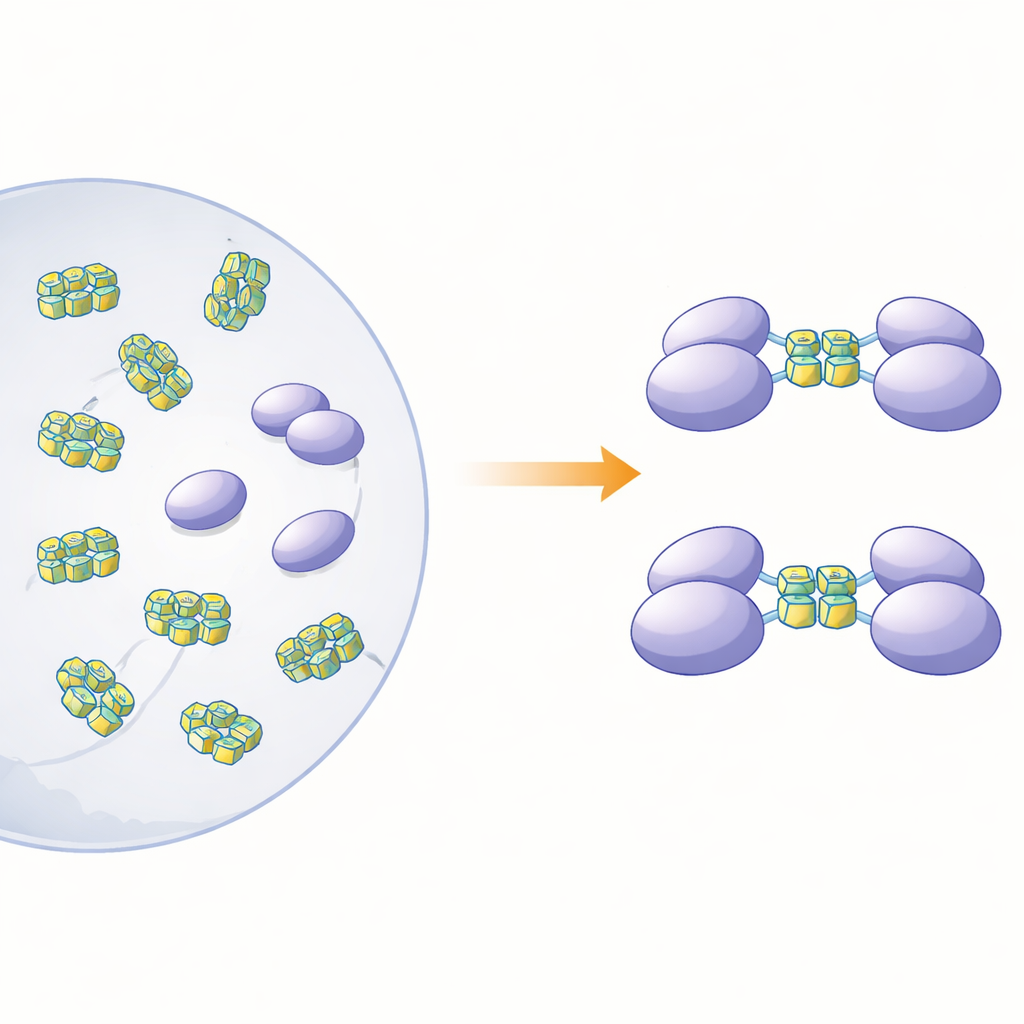
Aggrege Olmuş Bir Proteinin Çözülmesi
Proteinin fiziksel formunun algılama rolüyle nasıl ilişkili olduğunu netleştirmek için yazarlar, tam uzunluklu hnRNP A2/B1’i ve farklı kısaltılmış versiyonlarını bakteride ürettiler. Tam uzunluklu proteini çözeltide incelediklerinde, düzenli ayrı parçalar gibi davranmadığını buldular. Bunun yerine büyük, düzensiz kümeler—"çözünebilir amorf agregatlar"—oluşturuyor; bunlar kararsızdı ve daha fazla çökme eğilimindeydi. Buna karşılık, proteinin kuyruk ucunda farklı bölümler eksik olan üç kesilmiş versiyon çözeltide düzenli, tek moleküller (monomerler) olarak kaldı. Bilgisayar tabanlı yapı tahminleri, hnRNP A2/B1’in yaklaşık dörtte üçünün özellikle uçlarına yakın gevşek, düzensiz segmentlerden oluştuğunu öne sürdü. Bu esnek bölgeler agregasyonu teşvik ediyor gibi görünmekte ve proteinin yüksek çözünürlüklü yapısal çalışmaları için kristallerinin elde edilmesini neden zorlaştırdığını açıklamaya yardımcı oluyor.
Virüse Benzer DNA Proteinin Eşleşmesini Sağlıyor
Araştırmacılar daha sonra monomerik fragmanların hangi tür DNA’ya bağlandığını ve bu bağlanmanın proteinin durumuna ne yaptığını sordular. Odaklandıkları, G‑katradörtlere katlanabilen tek iplikli DNA segmentleriydi—guanin açısından zengin dizilerin oluşturduğu sıkışık yığınlar olup zinciri U biçimli, sıkı bir yapıya büküyor. Bu tür şekiller birçok virüs genomu ve kanserle ilişkili genlerde serpiştirilmiştir. Kalorimetri ve jel tabanlı bağlanma testleri kullanılarak ekip, RRM ve RGG bölgelerini kapsayan (residü 15–250) bir fragmanın tek iplikli DNA’ya güçlü bağlandığını, ancak karşılık gelen çift iplikli forma bağlanmadığını gösterdi. Boyuta göre ayrım ve ultrasentrifügasyon deneyleri çarpıcı bir etki ortaya koydu: bu fragman 12 veya 22 baz uzunluğundaki G‑katradört DNA ile karşılaştığında, proteinin iki kopyası birleşerek bir dimer oluşturdu; non‑katradört DNA ise bu eşleşmeyi tetiklemedi.
Esnek Bir Arayüze Bakmak
Deneysel kristalografik girişimler tekrar tekrar başarısız olduğundan ekip, proteinin fragmanının G‑katradörtü nasıl kavrayabileceğini görselleştirmek için hesaplamalı modellemeye yöneldi. Modern tahmin araçlarıyla oluşturulan modeller, hnRNP A2/B1’in daha sert merkezi bölgelerinin yığılmış DNA yapısını kavradığını, çevredeki düzensiz segmentlerin ise hareketli kaldığını öne sürdü. Yerleştirme (docking) simülasyonları, birden çok alandan gelen belirli amino asitlerin G‑katradört ile hidrojen bağları oluşturabileceğini ve iki protein molekülünün aynı DNA segmentini paylaştığı dimerik bir kompleksin stabilleşmesini vurguladı. Dikkate değer şekilde, bu etkileşimde yer alan kalıntılar hnRNP A2/B1’in yakın akrabalarının kullandıklarından farklı; bu da bu proteinin G‑katradört DNA’yı tanıma konusunda benzersiz bir yol geliştirdiğine işaret ediyor.
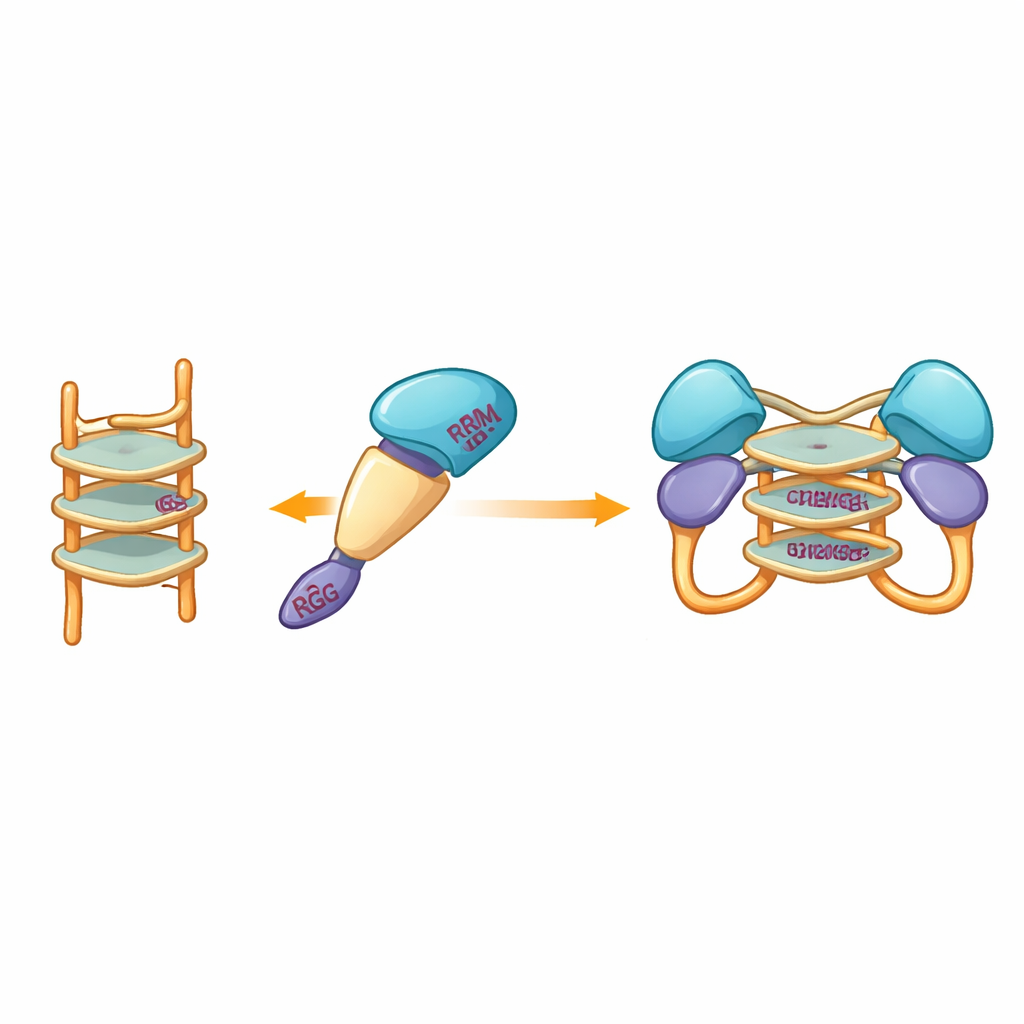
Protein Eşleşmesinden Antiviral Savunmaya
Bir araya getirildiğinde bulgular, tam uzunluklu hnRNP A2/B1’in kararsız agregatlara yatkınken, dikkatle kırpılmış versiyonların düzenli tek moleküller olarak davrandığını ve G‑katradört DNA ile karşılaştıklarında eşleşebildiğini gösteriyor. Bu kontrollü dimer oluşumu, özellikle birçok viral genomda bol bulunan guanin açısından zengin tek iplikli diziler tarafından yönlendiriliyor; bu da proteinin işgal eden DNA’yı algılamasında ve antiviral sinyal yollarını açmasında muhtemel fiziksel bir adımı öne sürüyor. Bu sonuçlar tüp içi deneylerden elde edilmiş olup canlı hücrelerde ve enfeksiyon modellerinde doğrulanması gerekiyor olsa da, protein montajındaki değişikliklerin hücrenin virüslere karşı erken uyarı sistemiyle nasıl ilişkili olabileceğine dair daha net, somut bir tablo sağlıyor—ve gelecekte bu yanıta ayar verebilecek küçük moleküllerin tasarımı için bir yol haritası sunuyor.
Atıf: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Anahtar kelimeler: hnRNP A2/B1, G-katradört DNA, DNA algılama, antiviral bağışıklık, protein dimerizasyonu