Clear Sky Science · nl
Moleculaire herkenning en geïnduceerde dimerisatie van hnRNP A2/B1-truncaties door enkelstrengs G-quadruplex-DNA
Hoe cellen viraal DNA opsporen
Virussen laten sporen van hun genetisch materiaal achter in onze cellen, en het lichaam moet die sporen snel herkennen om een verdediging op te bouwen. Deze studie onderzoekt hoe één veelvoorkomend cellulair eiwit, hnRNP A2/B1, kan helpen ongewone DNA-vormen te detecteren die in veel virussen voorkomen. Door te begrijpen hoe dit eiwit van vorm verandert wanneer het aan zulk DNA bindt, hopen de onderzoekers een basis te leggen voor nieuwe antivirale en antikankerstrategieën.
Een vorm-voelende eiwit in de kern
HnRNP A2/B1 staat vooral bekend als een helper-eiwit dat RNA beheert, de werkversie van genetische informatie. Het bevindt zich voornamelijk in de celkern en neemt deel aan tal van essentiële taken, van het spleten van RNA-berichten tot het reguleren van hun stabiliteit. Recente onderzoeken hebben echter een tweede rol voor dit eiwit aan het licht gebracht: het kan fungeren als sensor voor vreemd DNA van binnendringende virussen. Wanneer viraal DNA de kern bereikt, draagt hnRNP A2/B1 bij aan het aanzetten van innate immuunsignalen die de productie van antivirale moleculen, interferonen genoemd, op gang brengen.
Een geaggregeerd eiwit ontrafelen
Om te verduidelijken hoe de fysieke toestand van dit eiwit samenhangt met zijn sensorsfunctie, produceerden de auteurs het volledige hnRNP A2/B1 en verschillende ingekorte versies in bacteriën. Toen ze het volledige eiwit in oplossing onderzochten, bleek dat het zich niet gedroeg als nette, afzonderlijke deeltjes. In plaats daarvan vormde het grote, onregelmatige klonten — "oplosbare amorfe aggregaten" — die instabiel waren en tot verder neerslaan neigden. Ter vergelijking bleven drie getruncateerde versies zonder verschillende delen van de staartregio als keurig enkele moleculen (monomeren) in oplossing. Computergebaseerde structuurvoorspellingen suggereerden dat ongeveer driekwart van hnRNP A2/B1 uit flexibele, ongeordende segmenten bestaat, vooral nabij de uiteinden. Deze beweeglijke regio’s lijken aggregatie te bevorderen en verklaren waarom het zo moeilijk is geweest om kristallen van het eiwit te kweken voor studies met hoge resolutie.
Viraal-achtig DNA dat eiwitten doet paren
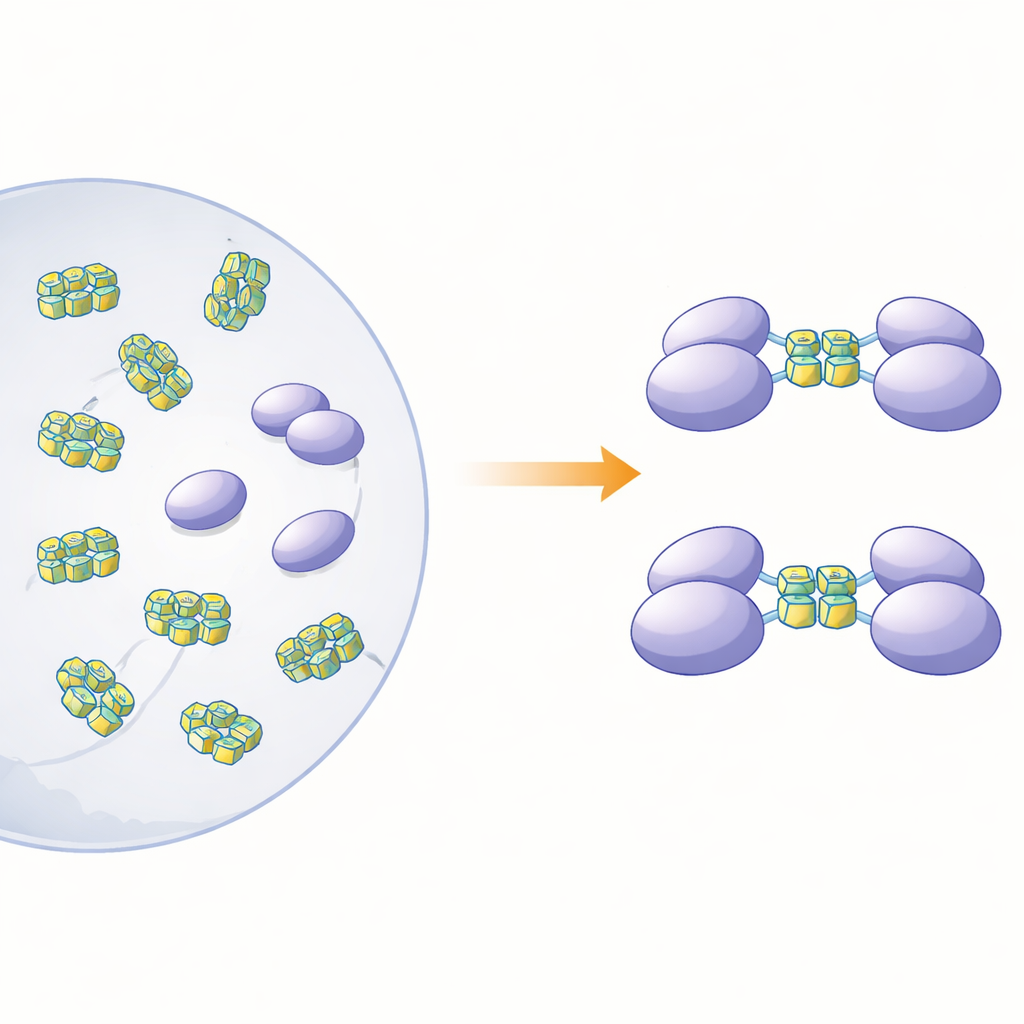
De onderzoekers onderzochten vervolgens welke soorten DNA de monomerische fragmenten zouden binden en wat die binding met de toestand van het eiwit zou doen. Ze concentreerden zich op enkelstrengs DNA-segmenten die kunnen vouwen tot G-quadruplexen — compacte stapelingen gevormd door guanine-rijke sequenties die de streng in een strakke, U-vormige structuur buigen. Dergelijke vormen komen verspreid voor in de genomen van veel virussen en genen gerelateerd aan kanker. Met calorimetrie en gelgebaseerde bindingsproeven toonde het team aan dat één fragment, dat de zogenaamde RRM- en RGG-regio’s omvat (residuen 15–250), sterk bindt aan enkelstrengs DNA maar niet aan de overeenkomstige dubbelstrengs vorm. Scheiding op basis van grootte en ultracentrifugatie-experimenten toonden een opvallend effect: wanneer dit fragment een G-quadruplex-DNA van 12 of 22 basen tegenkwam, sloten twee kopieën van het eiwitfragment zich samen tot een dimeer, terwijl niet-quadruplex-DNA deze koppeling niet veroorzaakte.
Kijken in een flexibele interface
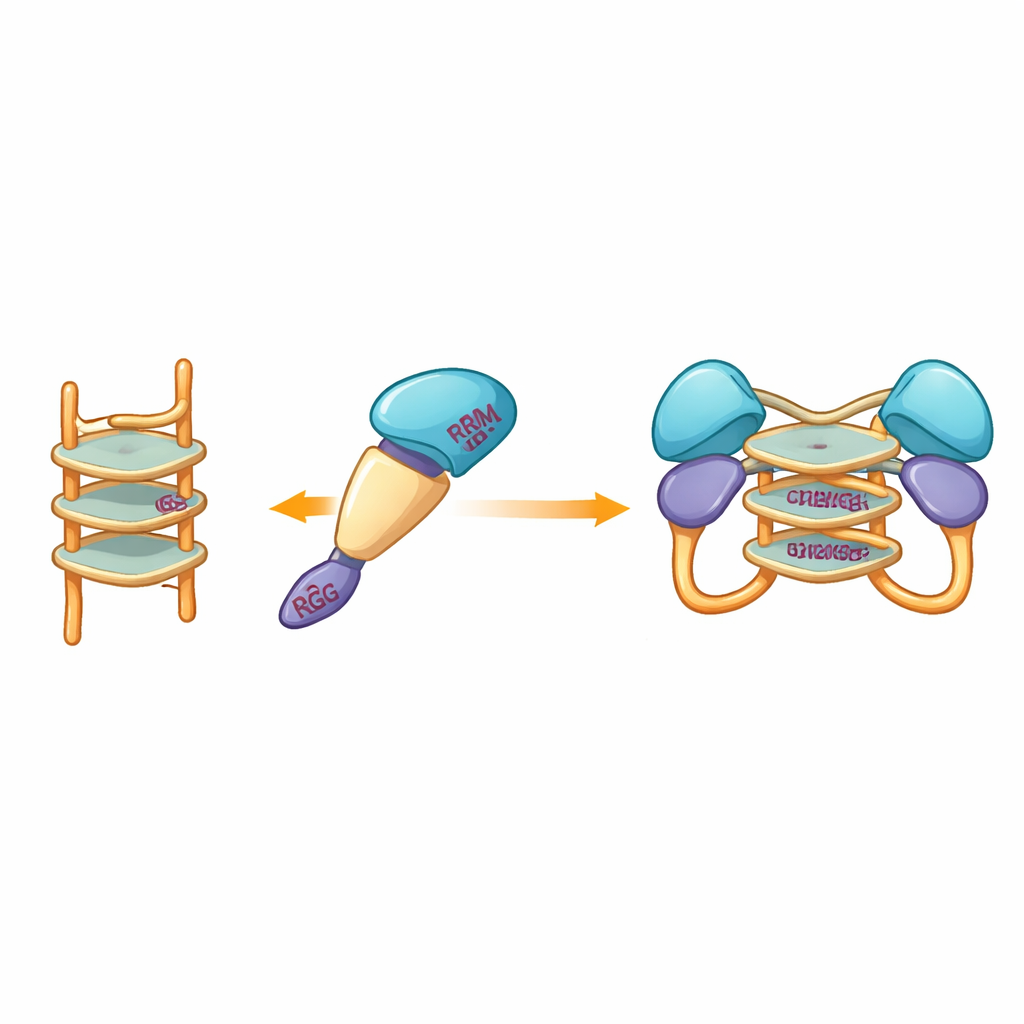
Aangezien experimentele kristallografiepogingen herhaaldelijk mislukten, wendde het team zich tot computationele modellering om te visualiseren hoe het eiwitfragment een G-quadruplex zou kunnen omvatten. Modellen gebouwd met moderne voorspellingsinstrumenten suggereerden dat de stijvere centrale domeinen van hnRNP A2/B1 de gestapelde DNA-structuur omsluiten, terwijl omliggende ongeordende segmenten mobiel blijven. Docking-simulaties belichtten een reeks specifieke aminozuren uit verschillende domeinen die mogelijk waterstofbruggen met het G-quadruplex kunnen vormen, waardoor een dimerisch complex wordt gestabiliseerd waarin twee eiwitmoleculen hetzelfde DNA-segment delen. Opvallend is dat deze interacterende residuen verschillen van die gebruikt door nauwe verwanten van hnRNP A2/B1, wat erop wijst dat dit eiwit een unieke manier heeft ontwikkeld om G-quadruplex-DNA te herkennen.
Van eiwitkoppeling naar antivirale verdediging
Samengevat tonen de bevindingen aan dat hoewel het volledige hnRNP A2/B1 de neiging heeft om samen te klonteren in instabiele aggregaten, zorgvuldig bijgesneden versies zich gedragen als ordelijke enkele moleculen die kunnen paren wanneer ze G-quadruplex-DNA tegenkomen. Deze gecontroleerde dimervorming, specifiek aangedreven door guanine-rijke enkelstrengse sequenties die in veel virale genomen overvloedig aanwezig zijn, suggereert een aannemelijke fysieke stap in hoe het eiwit binnendringend DNA waarneemt en helpt antivirale signaalroutes te activeren. Hoewel deze resultaten in reageerbuizen zijn verkregen en nog bevestigd moeten worden in levende cellen en infectiemodellen, geven ze een helderder, concreter beeld van hoe veranderingen in eiwitsamenstelling gekoppeld kunnen zijn aan het vroege waarschuwingssysteem van de cel tegen virussen — en bieden ze een routekaart voor het ontwerpen van kleine moleculen die deze respons in toekomstige therapieën kunnen bijsturen.
Bronvermelding: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Trefwoorden: hnRNP A2/B1, G-quadruplex-DNA, DNA-detectie, antivirale immuniteit, proteïnedimerisatie