Clear Sky Science · fr
Reconnaissance moléculaire et dimérisation induite des tronçons d'hnRNP A2/B1 par l'ADN simple brin en G-quadruplex
Comment les cellules détectent l'ADN viral
Les virus laissent des traces de leur matériel génétique à l'intérieur de nos cellules, et l'organisme doit reconnaître ces traces rapidement pour déclencher une réponse. Cette étude examine comment une protéine cellulaire abondante, hnRNP A2/B1, peut contribuer à détecter des formes d'ADN inhabituelles fréquentes chez de nombreux virus. En comprenant comment cette protéine change de conformation lorsqu'elle se lie à ce type d'ADN, les chercheurs espèrent jeter les bases de nouvelles stratégies antivirales et anticancéreuses.
Une protéine détectrice de formes dans le noyau
HnRNP A2/B1 est surtout connue comme une protéine d'assistance qui gère l'ARN, la copie active de l'information génétique. Elle réside principalement dans le noyau cellulaire et participe à de nombreuses fonctions essentielles, du découpage (épissage) des messages ARN au contrôle de leur stabilité. Des travaux récents ont cependant révélé une seconde fonction pour cette protéine : elle peut agir comme un détecteur d'ADN étranger provenant de virus envahisseurs. Lorsque l'ADN viral pénètre dans le noyau, hnRNP A2/B1 participe à l'activation des signaux de l'immunité innée qui déclenchent la production de molécules antivirales appelées interférons.
Démêler une protéine agrégée
Pour clarifier comment la forme physique de cette protéine se rapporte à son rôle de capteur, les auteurs ont produit l'hnRNP A2/B1 en intégralité ainsi que plusieurs versions tronquées dans des bactéries. En examinant la protéine pleine longueur en solution, ils ont constaté qu'elle ne se comportait pas comme des particules nettes et séparées. Au contraire, elle formait de gros amas irréguliers — « agrégats amorphes solubles » — instables et susceptibles de précipiter davantage. En revanche, trois versions tronquées, dépourvues de différentes portions de l'extrémité C-terminale, restaient des molécules isolées (monomères) en solution. Des prédictions structurales informatiques ont suggéré qu'environ les trois quarts de hnRNP A2/B1 sont composés de segments souples et désordonnés, en particulier près de ses extrémités. Ces régions flexibles semblent favoriser l'agrégation et aident à expliquer pourquoi il a été si difficile d'obtenir des cristaux de la protéine pour des études structurales à haute résolution.
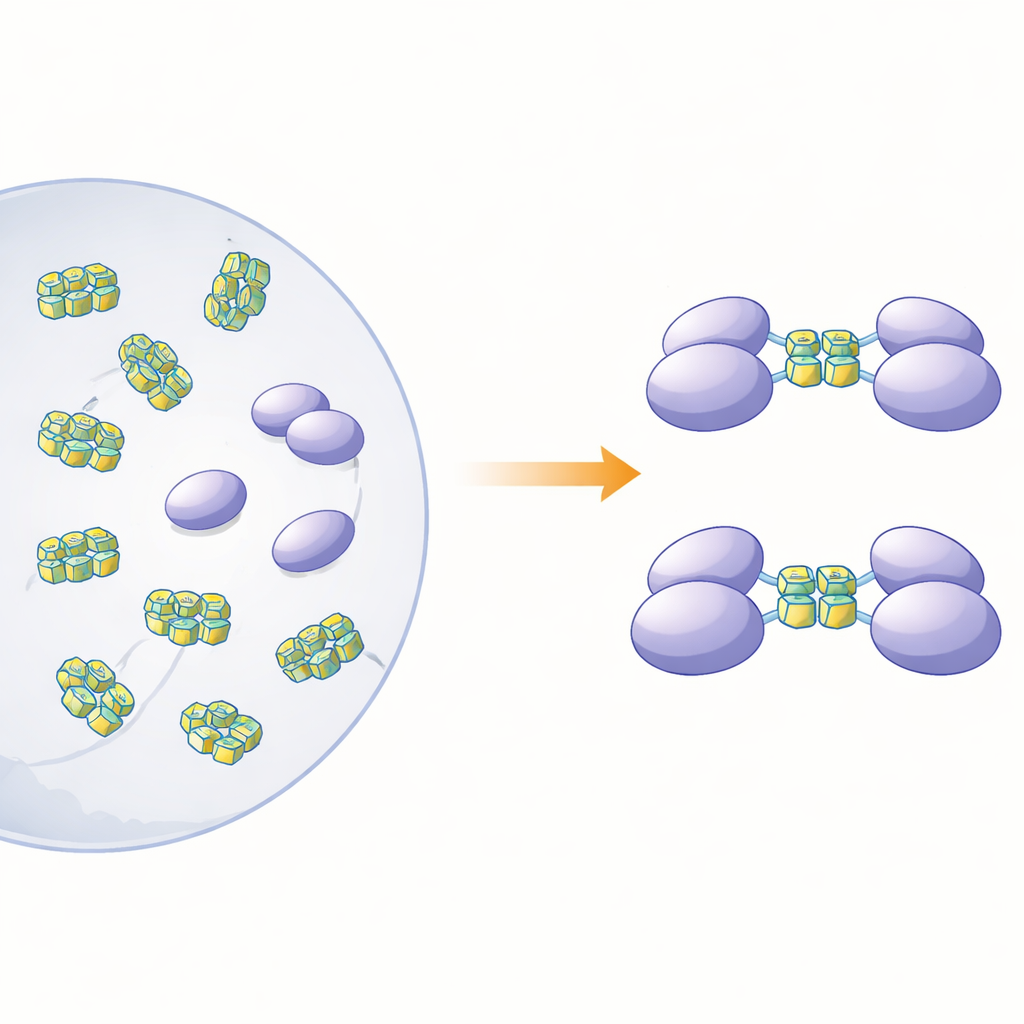
Un ADN de type viral qui pousse les protéines à se jumeler
Les chercheurs ont ensuite cherché à savoir quels types d'ADN les fragments monomériques lieraient, et quel effet cette liaison aurait sur l'état de la protéine. Ils se sont concentrés sur des segments d'ADN simple brin capables de se replier en G‑quadruplex — empilements compacts formés par des séquences riches en guanines qui courbent le brin en une structure resserrée en U. De telles formes parsèment les génomes de nombreux virus et de gènes impliqués dans le cancer. À l'aide de calorimétrie et d'essais de liaison sur gel, l'équipe a montré qu'un fragment en particulier, couvrant les régions dites RRM et RGG (résidus 15–250), se lie fortement à l'ADN simple brin mais pas à la forme double brin correspondante. Des expériences de séparation par taille et d'ultracentrifugation ont révélé un effet frappant : lorsque ce fragment rencontrait de l'ADN en G‑quadruplex de 12 ou 22 bases, deux copies du fragment protéique se joignaient pour former un dimère, alors que l'ADN non‑quadruplex ne déclenchait pas cet appariement.
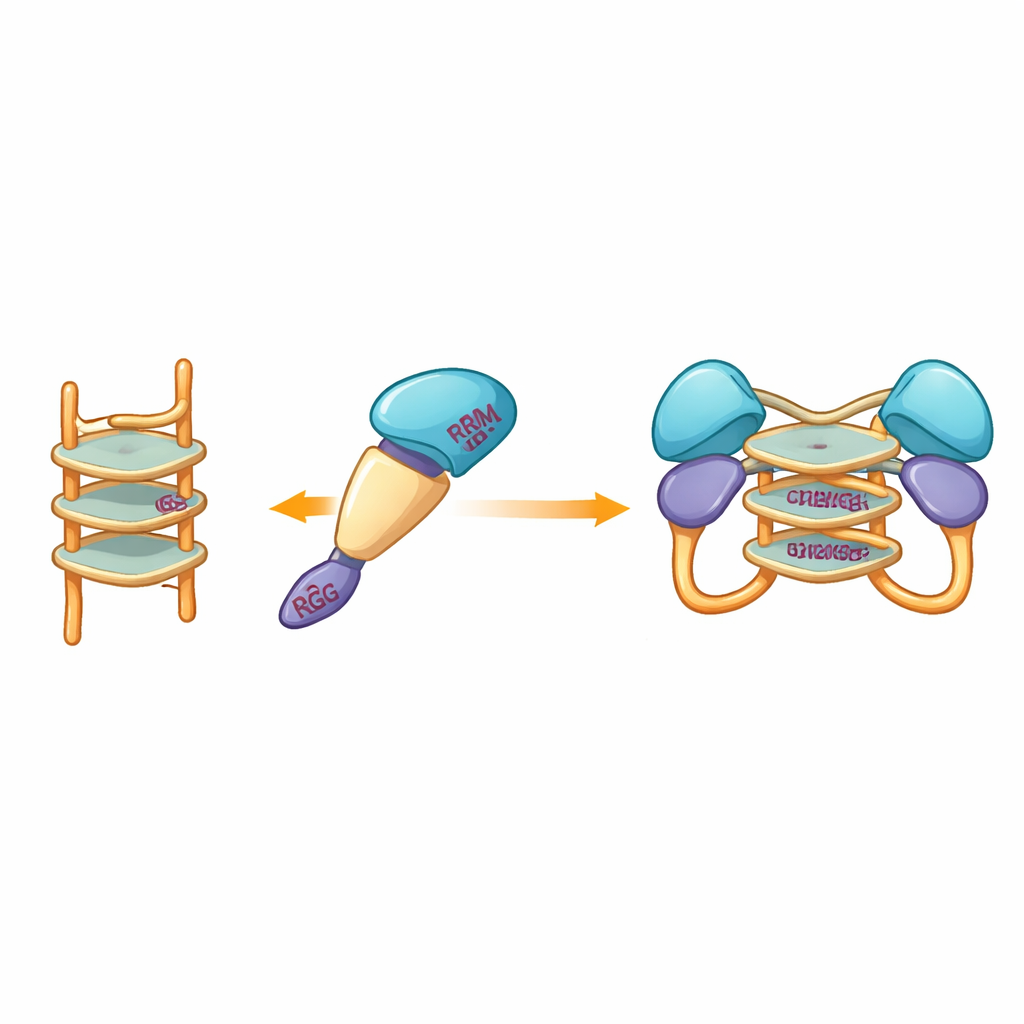
Plongée dans une interface flexible
Comme les tentatives expérimentales de cristallographie ont échoué à plusieurs reprises, l'équipe s'est tournée vers la modélisation computationnelle pour visualiser comment le fragment protéique pourrait enlacer un G‑quadruplex. Des modèles construits avec des outils de prédiction modernes suggèrent que les domaines centraux plus rigides de hnRNP A2/B1 accueillent la structure d'ADN empilée, tandis que les segments désordonnés environnants demeurent mobiles. Des simulations d'arrimage ont mis en évidence un ensemble d'acides aminés spécifiques issus de plusieurs domaines pouvant former des liaisons hydrogène avec le G‑quadruplex, stabilisant un complexe dimérique dans lequel deux molécules protéiques partagent le même segment d'ADN. Fait notable, ces résidus d'interaction diffèrent de ceux utilisés par des homologues proches d'hnRNP A2/B1, ce qui suggère que cette protéine a évolué une manière unique de reconnaître l'ADN en G‑quadruplex.
De l'appariement des protéines à la défense antivirale
Pris ensemble, les résultats montrent que tandis que l'hnRNP A2/B1 en pleine longueur a tendance à former des agrégats instables, des versions soigneusement tronquées se comportent comme des molécules ordonnées qui peuvent se jumeler lorsqu'elles rencontrent de l'ADN en G‑quadruplex. Cette dimérisation contrôlée, induite spécifiquement par des séquences simple brin riches en guanine, abondantes dans de nombreux génomes viraux, suggère une étape physique plausible expliquant comment la protéine détecte l'ADN envahisseur et contribue à activer les voies de signalisation antivirales. Bien que ces résultats aient été obtenus in vitro et doivent encore être confirmés dans des cellules vivantes et des modèles d'infection, ils offrent une image plus claire et concrète de la manière dont les changements d'assemblage protéique peuvent être liés au système d'alerte précoce de la cellule contre les virus — et fournissent une feuille de route pour concevoir des petites molécules capables de moduler cette réponse dans de futures thérapies.
Citation: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Mots-clés: hnRNP A2/B1, ADN en G-quadruplex, détection de l'ADN, immunité antivirale, dimérisation des protéines