Clear Sky Science · he
זיהוי מולקולרי ודימריזציה מושרת של חיתוכים ב‑hnRNP A2/B1 על‑ידי DNA חד‑גדילי מסוג G‑quadruplex
כיצד תאים מזהים DNA ויראלי
וירוסים משאירים עקבות של החומר הגנטי שלהם בתוך התאים שלנו, והגוף צריך לזהות עקבות אלה במהירות כדי להגיב בהגנה. מחקר זה בוחן כיצד חלבון אחד רב‑שכיח בתא, hnRNP A2/B1, עשוי לסייע לחוש צורות DNA לא שגרתיות הנפוצות ברבים מהוירוסים. בהבנת האופן שבו חלבון זה משנה את צורתו בעת קשירה ל‑DNA כזה, החוקרים מקווים לסלול יסודות לאסטרטגיות אנטי‑וירליות ואנטי‑סרטניות חדשות.
חלבון חישה בציטורגרמת הגרעין
hnRNP A2/B1 ידוע בעיקר כעוזר בניהול RNA, העותק העובד של המידע הגנטי. הוא חי בעיקר בגרעין התא ומשתתף במגוון משימות חיוניות — מביצוע חיתוך (splicing) של הודעות RNA ועד לשליטה ביציבותן. עם זאת, עבודות אחרונות חשפו חיים שניים לחלבון זה: הוא יכול לפעול כחיישן ל‑DNA זר שמגיע מוירוסים פולשים. כאשר DNA ויראלי נכנס לגרעין, hnRNP A2/B1 משתתף בהפעלת אותות חיסון מולד שמובילים לייצור מולקולות אנטי‑וירליות הנקראות אינטרפרונים.
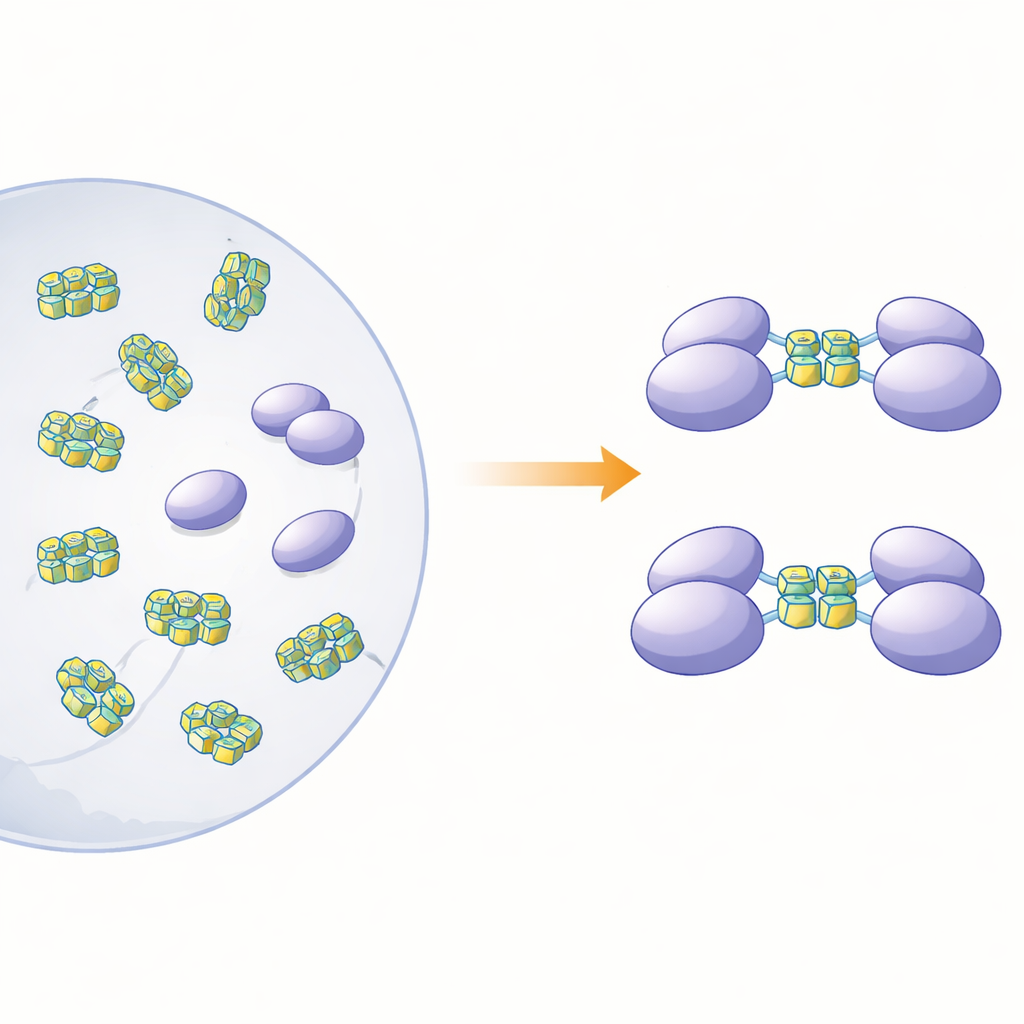
פיענוח חלבון שהצטבר באגרגטים
כדי להבהיר כיצד הצורה הפיזיקלית של החלבון קשורה לתפקידו כחיישן, המחברים ייצרו hnRNP A2/B1 מלא וכן כמה גרסאות מקוצרות בחיידקים. כאשר בחנו את החלבון המלא בתמיסה, מצאו שהוא לא מתנהג כיחידות מסודרות ונפרדות. במקום זאת, הוא יצר גושים גדולים ובלתי סדירים — "אגרגטים אמורפיים מסיסים" — שהיו בלתי יציבים ושאפו להפרידף (precipitate). לעומת זאת, שלוש גרסאות מקוצרות שחסרו מקטעים שונים בקצה הזנב נשארו כמולקולות מסודרות בודדות (מונומרים) בתמיסה. חיזוי מבני במחשב הציע שכ‑כ‑רוב hnRNP A2/B1 מורכב ממקטעים גמישים ובלתי‑מסודרים, במיוחד בסמוך לקצוותיו. האזורים הגמישים הללו נראים כמקדמים אגגרגציה ומסבירים מדוע קשה כל כך לגדל גבישים של החלבון ללימודים מבניים ברזולוציה גבוהה.
DNA בדומה לוירוס שגורם לזיווג חלבונים
לאחר מכן בדקו החוקרים אילו סוגי DNA הקטעים המונומריים יקשרו, ומה תעשה קשירה זו למצב החלבון. הם התמקדו בחתיכות DNA חד‑גדיליות היכולות לקפל ל‑G‑quadruplexes — ערימות קומפקטיות הנוצרות על ידי רצפי גואנין עשירים שמקפלים את הגדיל למבנה צורת U הדוק. צורות כאלה מפוזרות בגנומים של רבים מהוירוסים וגם בגנים הקשורים לסרטן. באמצעות קלורימטריה ובדיקות קשירה במשטח ג'ל, הראו שהקטע שכולל את אזורי ה‑RRM וה‑RGG (חומצות אמינו 15–250) נקשר בחוזקה ל‑DNA חד‑גדילי אך לא לצורתו הכפולה. ניסויים של הפרדה לפי גודל ואולטרה‑צנטריפוגה גילו השפעה בולטת: כאשר קטע זה נתקל ב‑G‑quadruplex DNA באורך 12 או 22 בסיסים, שתי עותקים של קטע החלבון התאחדו ויצרו דימר, בעוד ש‑DNA שאינו יוצר קואדרופלקס לא עורר זיווג זה.
מציצים לממשק גמיש
מכיוון שניסיונות גבישולוגיה ניסיוניים כשלו שוב ושוב, פנו החוקרים למודלים חישוביים כדי לדמות כיצד קטע החלבון עשוי לאחוז ב‑G‑quadruplex. מודלים שנבנו בכלי חיזוי מודרניים הציעו שהדומיינים המרכזיים הקשיחים יותר של hnRNP A2/B1 מחבקים את המבנה הערום המוטל, בעוד שמקטעים בלתי‑מסודרים מקיפים וממשיכים להיות ניידים. סימולציות דוקינג הדגישו קבוצת חומצות אמינו ספציפיות מכמה דומיינים שעשויות ליצור קשרי מימן עם ה‑G‑quadruplex, לייצב קומפלקס דימרי שבו שתי מולקולות חלבון חולקות את אותו מקטע DNA. לשם הבחנה, שארית‑האינטראקציה הללו שונות מאלה שבשימושם של קרובי משפחה קרובים של hnRNP A2/B1, מה שמרמז שהחלבון פיתח דרך ייחודית לזהות G‑quadruplex DNA.
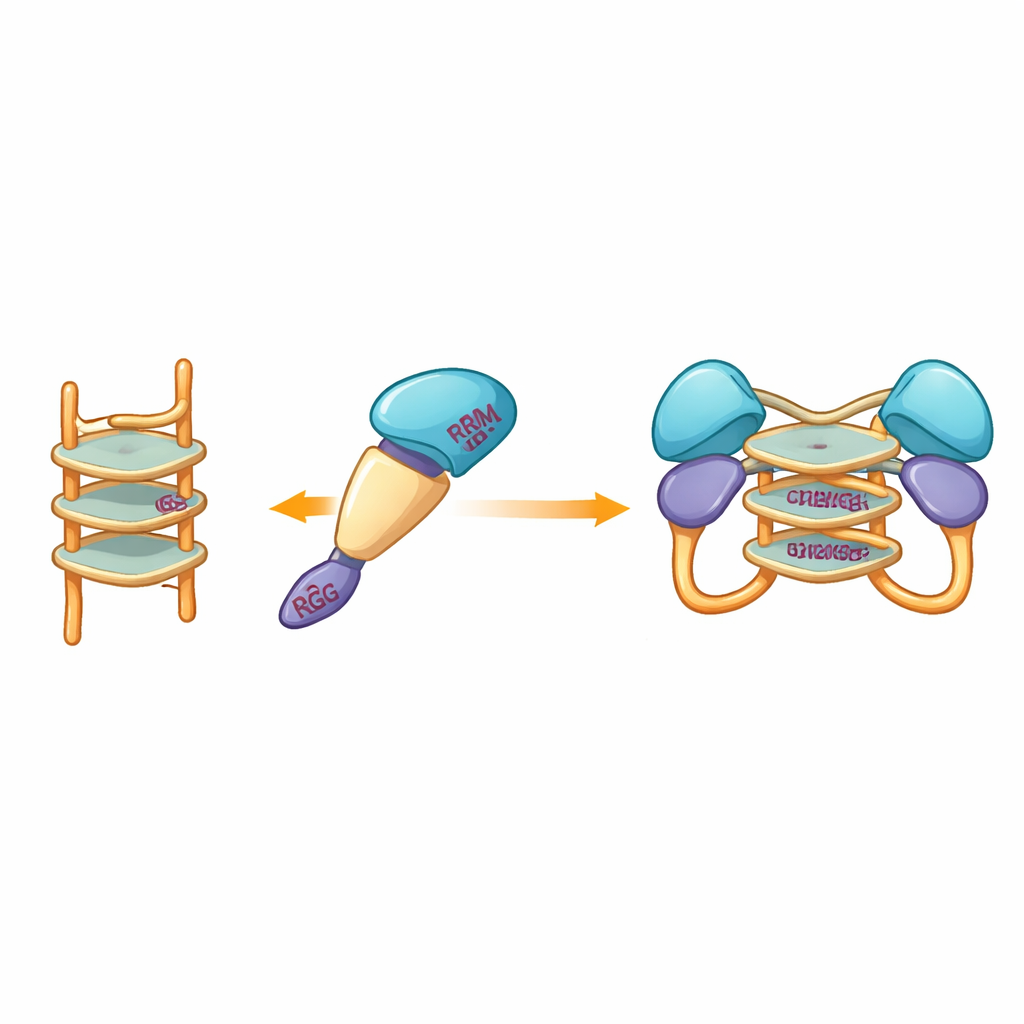
מזיווג חלבוני להגנה אנטי‑ויראלית
בסיכום, הממצאים מראים שבזמן ש‑hnRNP A2/B1 המלא נוטה להצטבר באגרגטים בלתי יציבים, גרסאות משופרות בקפידה מתנהגות כמולקולות בודדות מסודרות שיכולות לזווג כאשר הן פוגשות DNA מסוג G‑quadruplex. יצירת הדימר המבוקרת הזאת, שמונעת במיוחד על‑ידי רצפים חד‑גדיליים עשירי גואנין השכיחים בגנומי וירוסים רבים, מציעה שלב פיזיקלי סביר בדרך שבה החלבון חוֹשׁ את ה‑DNA הפולש וסייע בהפחתת מסלולי איתות אנטי‑וירליים. אף על‑פי שהתוצאות הופקו בצינור ובניסויים מבחנה ודורשות אימות בתאים חיים ובמודלים של זיהום, הן מספקות תמונה ברורה ומוחשית יותר של איך שינויים באספה של חלבונים עשויים להיות קשורים למערכת האזעקה המוקדמת של התא נגד וירוסים — ומציעות מפת דרכים לתכנון מולקולות קטנות שיכולות לכוונן תגובה זו בטיפולים עתידיים.
ציטוט: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
מילות מפתח: hnRNP A2/B1, DNA G‑quadruplex, חישה של DNA, חיסון אנטי‑וירלי, דימריזציה של חלבון