Clear Sky Science · es
Reconocimiento molecular e inducida dimerización de truncamientos de hnRNP A2/B1 por ADN monocatenario en G-cuádruplex
Cómo las células detectan el ADN viral
Los virus dejan rastros de su material genético dentro de nuestras células, y el organismo debe reconocer esos rastros con rapidez para montar una defensa. Este estudio explora cómo una proteína celular abundante, hnRNP A2/B1, podría ayudar a detectar formas inusuales de ADN que son comunes en muchos virus. Al comprender cómo cambia la conformación de esta proteína cuando se une a ese ADN, los investigadores esperan sentar las bases para nuevas estrategias antivirales y anticancerígenas.
Una proteína detectora de formas en el núcleo
HnRNP A2/B1 es conocida principalmente como una proteína auxiliar que gestiona el ARN, la copia operativa de la información genética. Reside sobre todo en el núcleo celular y participa en numerosas tareas esenciales, desde el splicing de los mensajes de ARN hasta el control de su estabilidad. Sin embargo, trabajos recientes han revelado una segunda función para esta proteína: puede actuar como sensor del ADN extraño procedente de virus invasores. Cuando el ADN viral entra en el núcleo, hnRNP A2/B1 participa en la activación de señales de la inmunidad innata que desencadenan la producción de moléculas antivirales llamadas interferones.
Desentrañando una proteína agregada
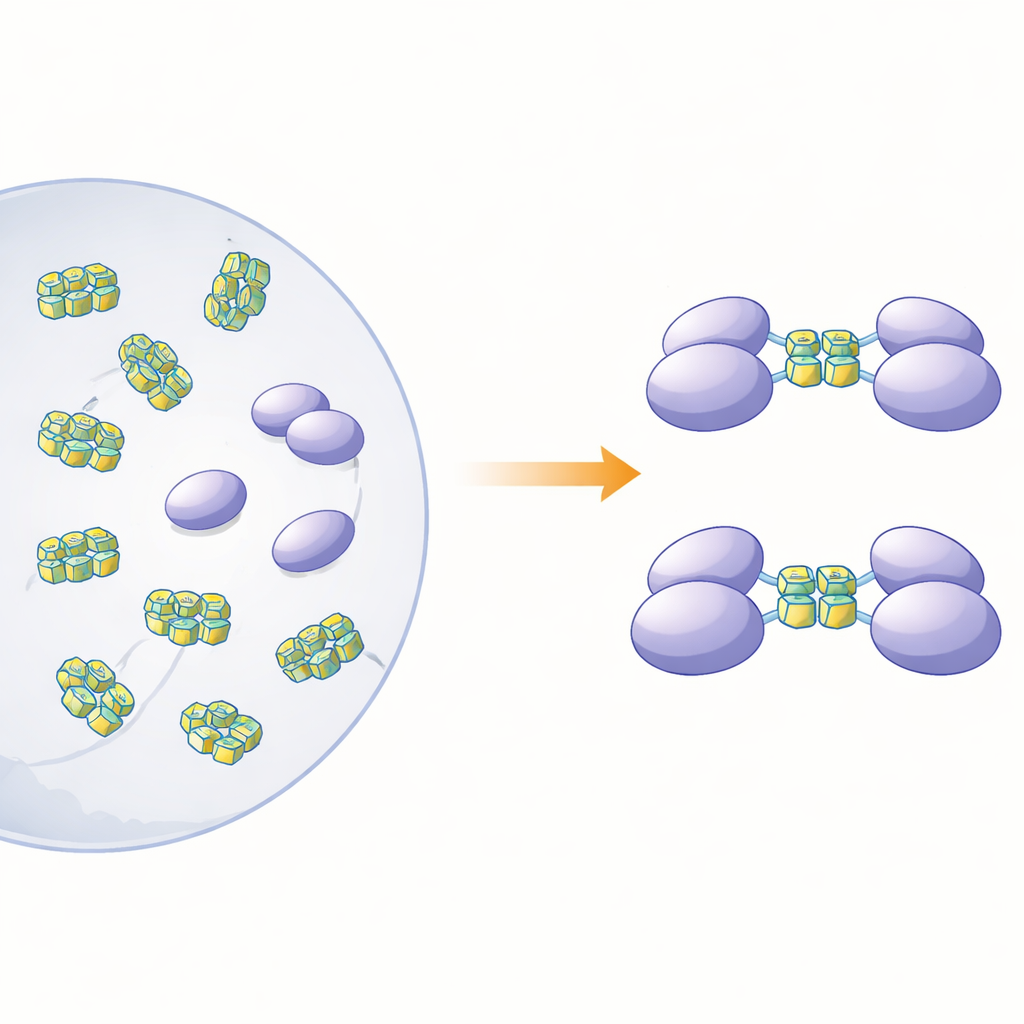
Para esclarecer cómo la forma física de esta proteína se relaciona con su papel de sensor, los autores produjeron hnRNP A2/B1 de longitud completa y varias versiones truncadas en bacterias. Al examinar la proteína completa en solución, encontraron que no se comportaba como partículas separadas y ordenadas. En lugar de ello, formaba grandes cúmulos irregulares —«agregados amorfos solubles»— que eran inestables y tendían a precipitar. En contraste, tres versiones truncadas que carecían de distintos tramos en el extremo C-terminal permanecieron como moléculas individuales (monómeros) ordenadas en solución. Predicciones estructurales por ordenador sugirieron que aproximadamente tres cuartas partes de hnRNP A2/B1 están formadas por segmentos flexibles y desordenados, especialmente cerca de sus extremos. Estas regiones móviles parecen promover la agregación y ayudan a explicar por qué ha sido tan difícil cristalizar la proteína para estudios estructurales de alta resolución.
ADN similar al viral que induce el apareamiento de proteínas
Los investigadores se preguntaron entonces a qué tipos de ADN se unirían los fragmentos monoméricos y qué efecto tendría esa unión sobre el estado de la proteína. Se centraron en segmentos de ADN monocatenario que pueden plegarse en G‑cuádruplexes: apilamientos compactos formados por secuencias ricas en guanina que doblan la hebra en una estructura cerrada en forma de U. Estas conformaciones están dispersas por los genomas de muchos virus y genes relacionados con el cáncer. Utilizando calorimetría y ensayos de unión basados en gel, el equipo mostró que un fragmento, que abarca las regiones denominadas RRM y RGG (residuos 15–250), se une con fuerza al ADN monocatenario pero no a la forma bicatenaria correspondiente. Experimentos de separación por tamaño y ultracentrifugación revelaron un efecto llamativo: cuando este fragmento encontró ADN en G‑cuádruplex de 12 o 22 nucleótidos, dos copias del fragmento proteico se unieron para formar un dímero, mientras que el ADN que no formaba cuádruplex no provocó este apareamiento.
Un vistazo a una interfaz flexible
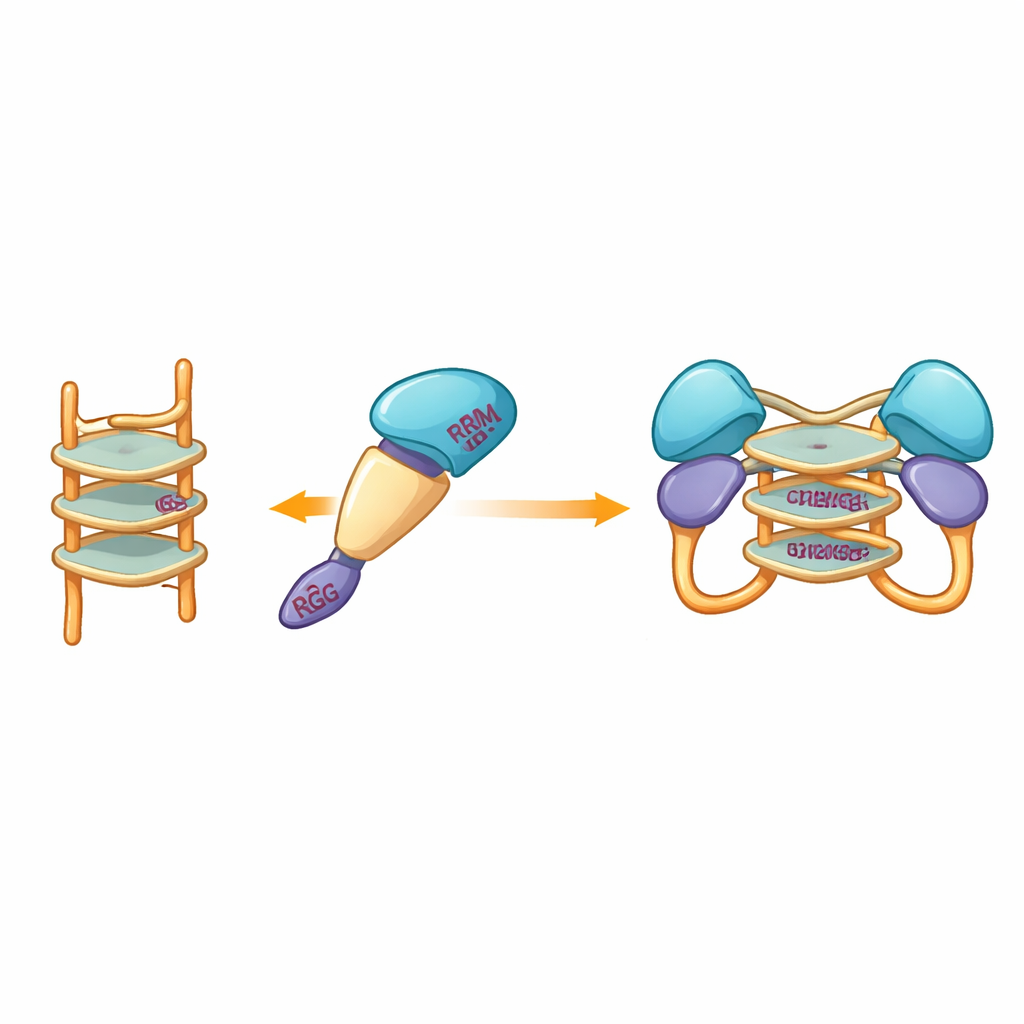
Dado que los intentos experimentales de cristalografía fracasaron repetidamente, el equipo recurrió a modelado computacional para visualizar cómo podría abrazar el fragmento proteico a un G‑cuádruplex. Modelos construidos con herramientas modernas de predicción sugirieron que los dominios centrales más rígidos de hnRNP A2/B1 acunan la estructura de ADN apilada, mientras que los segmentos desordenados circundantes permanecen móviles. Simulaciones de acoplamiento destacaron un conjunto de aminoácidos específicos de varios dominios que podrían formar enlaces de hidrógeno con el G‑cuádruplex, estabilizando un complejo dimérico en el que dos moléculas de proteína comparten el mismo segmento de ADN. Notablemente, estos residuos de interacción difieren de los empleados por parientes cercanos de hnRNP A2/B1, lo que sugiere que esta proteína ha evolucionado una manera única de reconocer el ADN en G‑cuádruplex.
Del apareamiento proteico a la defensa antiviral
En conjunto, los hallazgos muestran que, mientras que la hnRNP A2/B1 de longitud completa tiende a agruparse en agregados inestables, versiones recortadas con cuidado se comportan como moléculas individuales ordenadas que pueden aparearse cuando encuentran ADN en G‑cuádruplex. Esta formación de dímeros controlada, impulsada específicamente por secuencias monocatenarias ricas en guanina y abundantes en muchos genomas virales, sugiere un paso físico plausible en cómo la proteína detecta el ADN invasor y contribuye a activar las vías de señalización antiviral. Aunque estos resultados se obtuvieron en tubos de ensayo y aún deben confirmarse en células vivas y modelos de infección, proporcionan una imagen más clara y concreta de cómo los cambios en el ensamblaje proteico pueden estar ligados al sistema de alarma temprana de la célula frente a los virus —y ofrecen una hoja de ruta para diseñar pequeñas moléculas que podrían modular esta respuesta en terapias futuras.
Cita: Shahatibieke, D., Tang, X., Zheng, X. et al. Molecular recognition and induced dimerization of hnRNP A2/B1 truncations by G-quadruplex single strand DNA. Sci Rep 16, 10970 (2026). https://doi.org/10.1038/s41598-026-44646-7
Palabras clave: hnRNP A2/B1, ADN en G-cuádruplex, detección de ADN, inmunidad antiviral, dimerización de proteínas