Clear Sky Science · zh
肌营养不良蛋白dysferlin在心肌梗死后稳定心肌细胞膜微区
为什么心肌细胞需要紧急修补
当患者从心肌梗死幸存下来,真正的战斗才刚刚开始。受损区域不像简单的切口那样愈合;相反,瘢痕边缘存活的心肌细胞必须在剧烈的机械应力下持续收缩。该研究揭示了一种鲜为人知的修复蛋白dysferlin如何像微观补丁箱一样作用于这些承受过大应力的细胞,帮助其脆弱的细胞膜保持完整,从而维持心脏的泵血功能。
生存与瘢痕之间的高压边界
心肌梗死后,部分心脏的血流被阻断,许多细胞直接死亡,中心留下瘢痕。在这块死亡核心的周围是一条狭窄的“边界区”,那里的心肌细胞仍然存活,但要承受低氧、炎症以及随每次心跳产生的强烈牵张。这些环境使细胞的外膜及其复杂皱褶结构承受巨大压力,这些皱褶中布置着负责电信号和钙处理的关键构件。作者猜想,如果能在该区域保护膜的微观结构,或许可以挽救更多心功能。
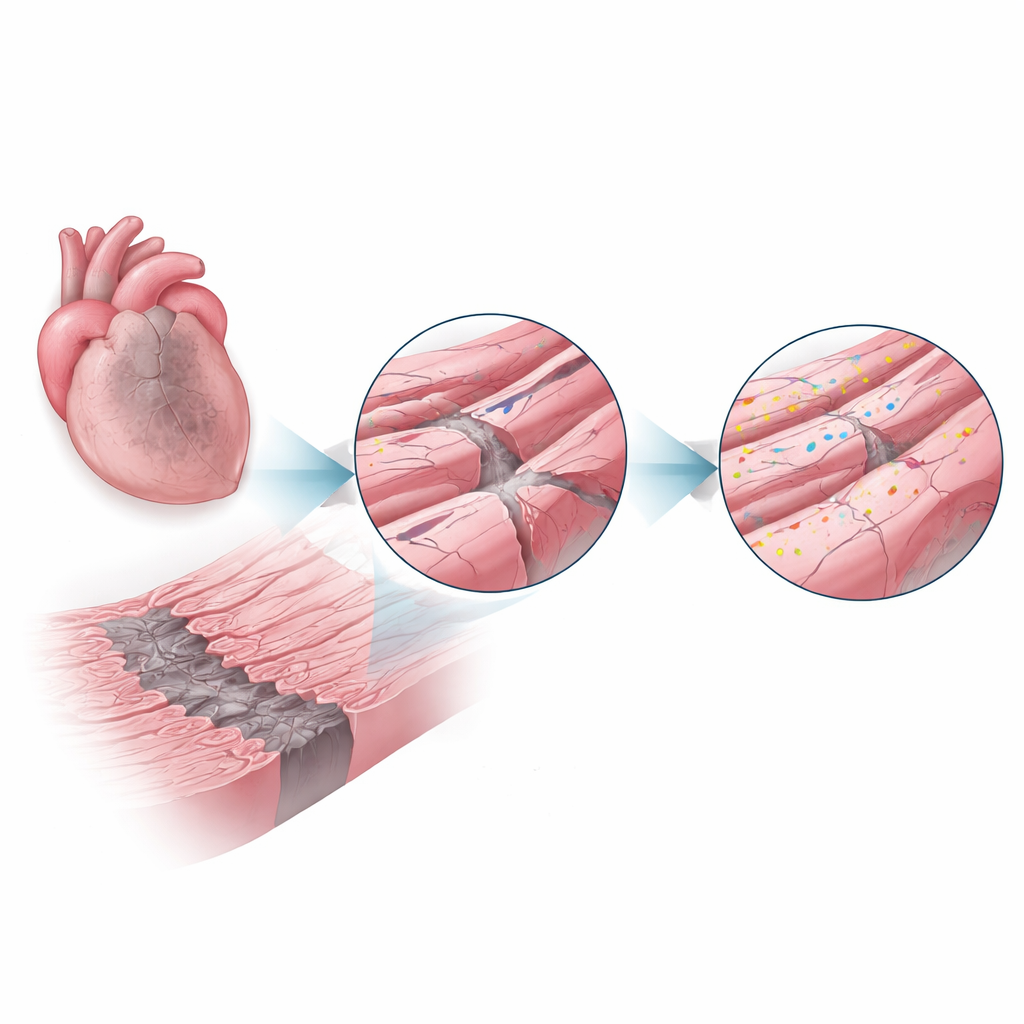
一种修复蛋白走上舞台
dysferlin是一种大型蛋白,在罕见的肌肉疾病中其缺失会导致骨骼肌乏力,部分原因是受损肌纤维无法高效修复膜结构。在本研究中,研究者探讨dysferlin是否在心脏中也发挥类似的保护作用。他们使用具有正常dysferlin或完全缺失dysferlin的小鼠,诱导心肌梗死并在一周和四周后检查心脏。正常小鼠在边界区的dysferlin水平激增,超过健康心脏的两倍,表明细胞在应力最高处主动动员这一修复系统。
dysferlin缺失会发生什么
研究组随后比较了有无dysferlin小鼠的结局。缺失该蛋白的动物形成了明显更大的瘢痕,左心室更扩张、功能更差。它们每搏泵出的血量减少,表明更多存活的心肌失去了功能。一种强大的蛋白组学技术让研究者能够在不同心脏区域目录化数千种蛋白。他们发现,dysferlin缺失改变了这些蛋白谱,尤其是在梗死区和边界区,改变了与细胞死亡、炎症和钙信号相关的通路——这些变化与细胞更脆弱和进展性功能衰竭相一致。
处于修复状态的微观结构
高分辨率成像放大观察了心肌细胞的精细结构。在健康组织中,细胞膜以规则的隧道格局向内凹陷,形成横-轴小管网络(transverse–axial tubule network),有助于电信号触发钙释放和收缩。心肌梗死后,该网络在边界区变得紊乱并部分丧失,尤其是横向成分受损。然而,残存的小管被明亮的dysferlin簇包裹,并被小的内陷膜泡环绕,暗示着活跃的修复与重塑。在细胞–细胞的连接处(心肌细胞交换电信号并相互附着的部位),dysferlin也与关键连接蛋白一起富集。生化实验显示dysferlin在大复合体中与这些伴侣发生物理关联,支持其在应力下维持和重建这些连接位点的作用。
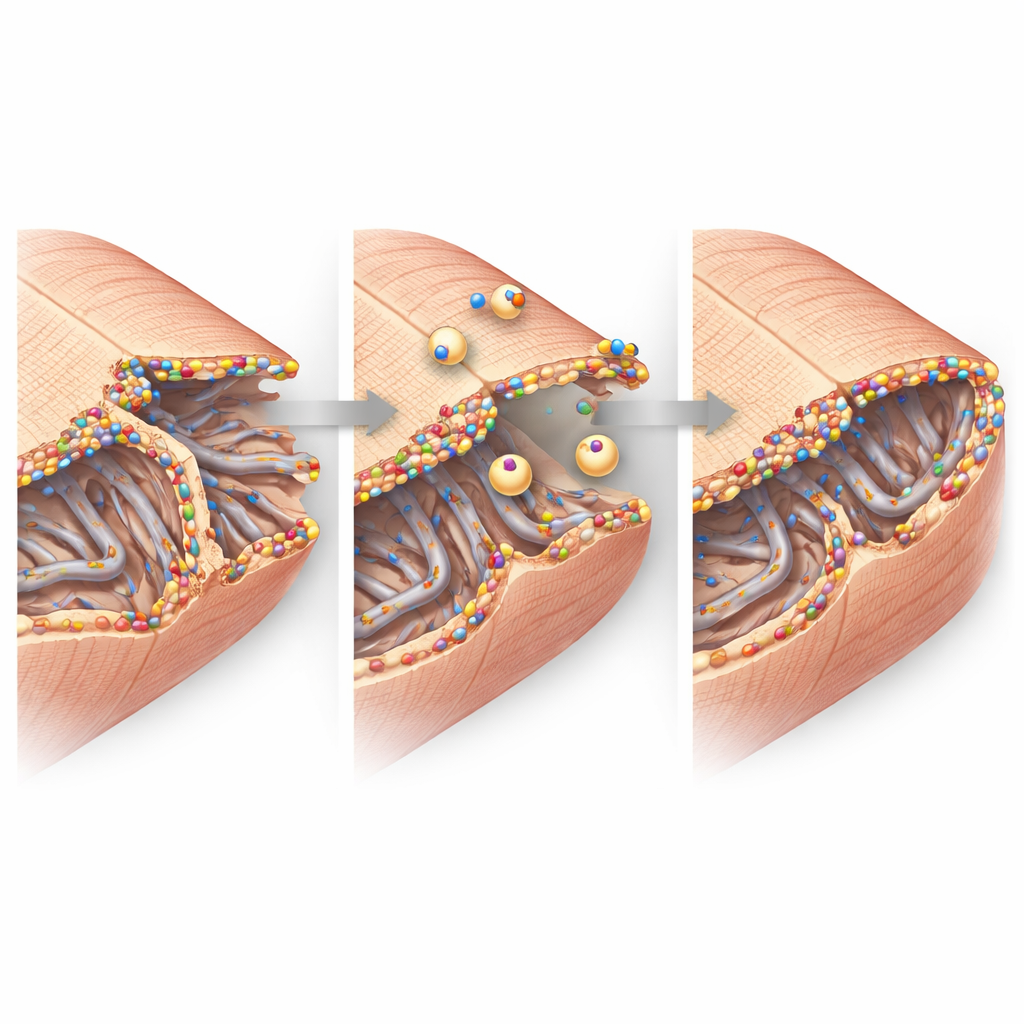
从分子到心脏功能的联系
将这些发现综合起来,研究描绘出dysferlin作为心肌梗死后边界区细胞膜守护者的形象。当dysferlin存在并被上调时,它在受损的小管网络和细胞–细胞连接皱褶处聚集,招募修复囊泡并稳定这些虽小但至关重要的结构。当dysferlin缺失时,这些纳米级的支持更容易瓦解,更多细胞丧失或功能受损,心脏的泵血能力随之下降。对于患者而言,这项工作表明,增强dysferlin活性或模拟其修复功能,将来可能成为在心肌梗死后通过保护使心肌细胞协同搏动的膜结构来限制心力衰竭的一种策略。
引用: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
关键词: 心肌梗死, 心肌细胞膜修复, dysferlin, 心力衰竭预防, 纳米区重塑