Clear Sky Science · pl
Dysferlin stabilizuje nanodomeny błon kardiomiocytów po zawale mięśnia sercowego
Dlaczego komórki serca potrzebują awaryjnych łat
Kiedy ktoś przeżyje zawał, prawdziwa walka dopiero się zaczyna. Uszkodzony obszar serca nie goi się jak zwykłe rozcięcie; zamiast tego żyjące komórki mięśnia sercowego na krawędzi blizny muszą dalej się kurczyć pod silnym stresem mechanicznym. Badanie to pokazuje, jak mało znane białko naprawcze, dysferlina, działa jak mikroskopijny zestaw łatek dla tych przeciążonych komórek, pomagając ich delikatnym błonom zachować integralność i utrzymać siłę pompowania serca.
Stresujące granice między życiem a blizną
Po zawale przepływ krwi do części serca jest zablokowany, co prowadzi do obumarcia wielu komórek i powstania centralnej blizny. Wokół tego martwego rdzenia znajduje się wąska „strefa brzeżna” z żyjącymi komórkami mięśnia sercowego, które znoszą niedotlenienie, stan zapalny i potężne rozciąganie przy każdym uderzeniu. Te warunki obciążają błonę komórkową i jej złożone fałdy, które mieszczą kluczowe struktury odpowiedzialne za sygnalizację elektryczną i regulację wapnia. Autorzy podejrzewali, że jeśli drobne elementy architektury błony w tej strefie da się chronić, można uratować więcej funkcji serca.
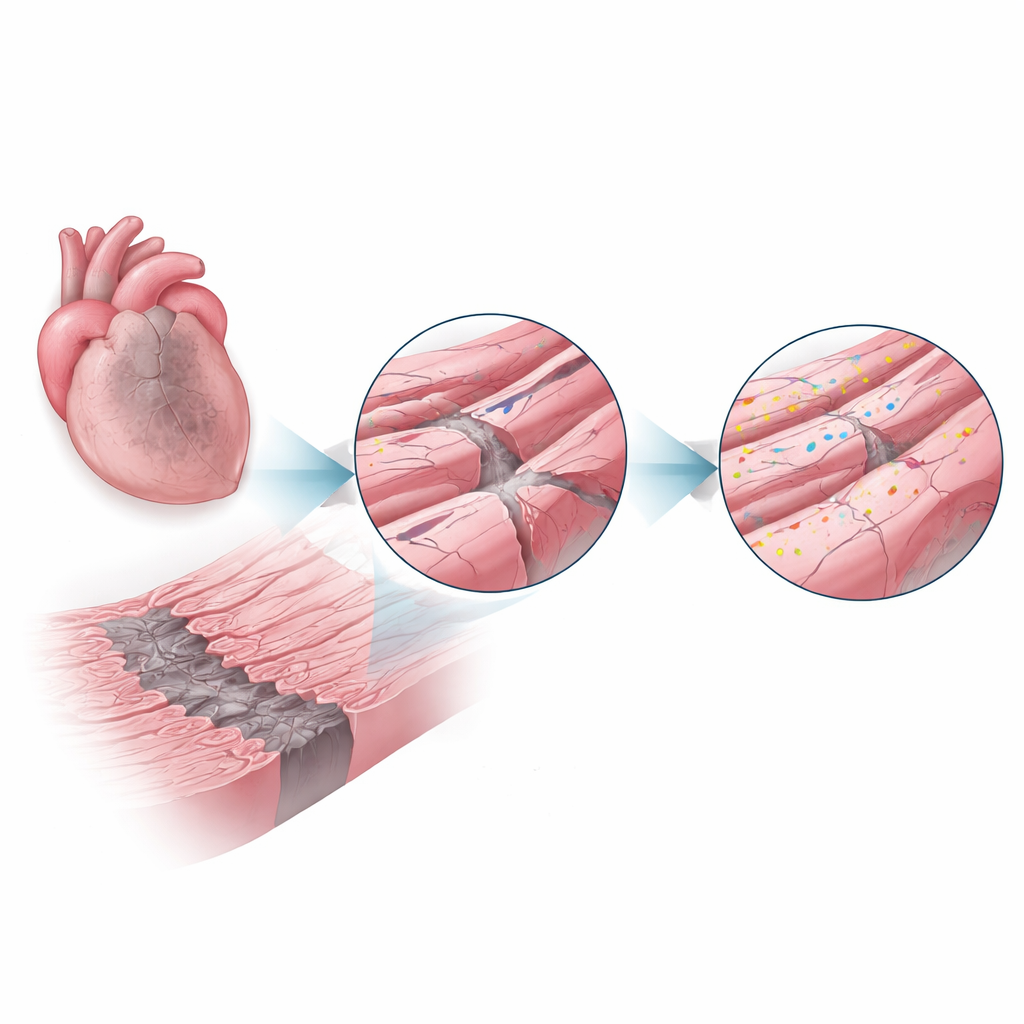
Białko naprawcze wchodzi na scenę
Dysferlina to duże białko znane z rzadkich chorób mięśni, w których jego brak prowadzi do osłabienia mięśni szkieletowych, częściowo dlatego, że uszkodzone włókna nie potrafią skutecznie naprawiać błon. W tym badaniu naukowcy sprawdzili, czy dysferlina pełni podobną ochronną rolę w sercu. Użyli myszy z normalną dysferliną i myszy całkowicie pozbawionych tego białka, wywołali zawały i analizowali serca po jednym i czterech tygodniach. U normalnych myszy poziomy dysferliny w strefie brzeżnej wzrosły ponad dwukrotnie w porównaniu z sercami zdrowymi, co sugeruje, że komórki aktywnie mobilizują ten system naprawczy tam, gdzie stres jest największy.
Co się dzieje, gdy brakuje dysferliny
Zespół porównał następnie wyniki u myszy z i bez dysferliny. Zwierzęta pozbawione białka rozwinęły znacznie większe blizny oraz bardziej rozdęte, słabsze lewe komory. Ich serca wyrzucały mniej krwi przy każdym uderzeniu, co wskazuje, że więcej przetrwałego mięśnia sercowego zawiodło. Silna technika proteomiczna pozwoliła badaczom zidentyfikować tysiące białek w różnych obszarach serca. Stwierdzili, że niedobór dysferliny przekształcał te profile białkowe, szczególnie w strefie zawału i strefie brzeżnej, zmieniając szlaki związane z obumieraniem komórek, stanem zapalnym i sygnalizacją wapniową — zmiany zgodne z bardziej kruchymi komórkami i postępującą niewydolnością.
Mikroskopowa architektura pod naprawą
Obrazowanie o wysokiej rozdzielczości przybliżyło finezyjną strukturę komórek serca. W zdrowej tkance błona komórkowa wpukla się do środka w regularną siatkę tuneli zwaną siecią kanalików poprzeczno–osiowych, która pomaga impulsom elektrycznym wyzwalać uwalnianie wapnia i skurcz. Po zawale ta sieć w strefie brzeżnej ulegała dezorganizacji i częściowej utracie, szczególnie jej elementy poprzeczne. Pozostałe kanaliki były jednak pokryte jasnymi skupiskami dysferliny i otoczone małymi wewnętrznymi pęcherzykami błonowymi, co wskazuje na aktywną naprawę i przebudowę. W miejscach połączeń międzykomórkowych, gdzie komórki serca wymieniają impulsy elektryczne i łączą się ze sobą, dysferlina również gromadziła się obok kluczowych białek stykowych. Eksperymenty biochemiczne pokazały, że dysferlina fizycznie wiąże się z tymi partnerami w dużych kompleksach, co wspiera tezę, że pomaga utrzymać i odbudować te miejsca styku pod wpływem stresu.
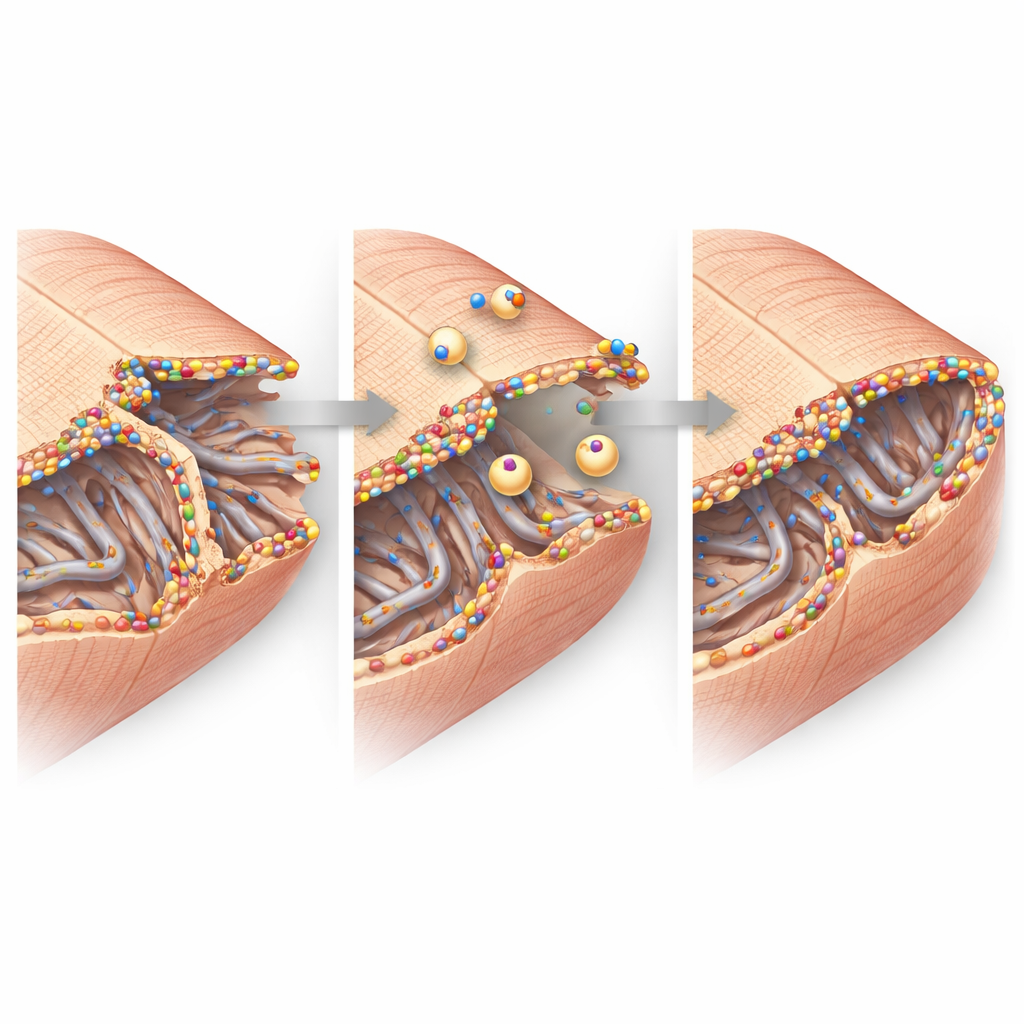
Od cząsteczek do funkcji serca
Składając te obserwacje w całość, badanie przedstawia dysferlinę jako strażnika błony komórkowej w wrażliwej strefie brzeżnej po zawale. Gdy jest obecna i jej ekspresja rośnie, dysferlina gromadzi się przy uszkodzonych sieciach kanalików i fałdach połączeń międzykomórkowych, przyciągając pęcherzyki naprawcze i stabilizując te mikroskopijne, lecz kluczowe struktury. Gdy jej brakuje, te nanostrukturalne podpory łatwiej się rozpadają, więcej komórek ginie lub działa nieprawidłowo, a zdolność pompowania serca maleje. Dla pacjentów wynika z tego, że zwiększenie aktywności dysferliny lub naśladowanie jej funkcji naprawczej mogłoby kiedyś stać się strategią ograniczania niewydolności serca po zawale poprzez ochronę błon niezbędnych, by komórki serca biły synchronicznie.
Cytowanie: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Słowa kluczowe: zawał mięśnia sercowego, naprawa błony kardiomiocytów, dysferlina, zapobieganie niewydolności serca, remodeling nanodomen