Clear Sky Science · ar
ديسفيرلين يثبت نانومجالات غشاء خلايا القلب بعد احتشاء عضلة القلب
لماذا تحتاج خلايا القلب إلى ترقيع طارئ
عندما ينجو شخص من نوبة قلبية، فإن المعركة الحقيقية قد بدأت للتو. المنطقة المتضررة من القلب لا تلتئم مثل جرح سطحي؛ بل يجب على خلايا عضلة القلب الباقية عند حافة النُّدبة أن تواصل الانقباض تحت إجهاد ميكانيكي شديد. تكشف هذه الدراسة كيف يلعب بروتين إصلاحي غير معروف جيداً، الديسفيرلين، دورًا يشبه حقيبة ترقيع ميكروسكوبية لهذه الخلايا المتحمّلة، مساعداً أغشيتها الرقيقة على التماسك وحفظ قدرة القلب على الضخ.
الحدود المجهدة بين الحياة والنُّدبة
بعد نوبة قلبية، يُمنع تدفّق الدم إلى جزء من القلب، ما يؤدي إلى موت العديد من الخلايا وترك ندبة مركزية. يحيط بهذا النواة الميتة نطاق ضيّق «منطقة الحد» لخلايا عضلة القلب الحية التي تتحمّل نقص الأكسجين والالتهاب والتمدد القوي مع كل نبضة. تضغط هذه الظروف على غشاء الخلية الخارجي وطياته المعقّدة، التي تضم هياكل حاسمة للإشارات الكهربائية والتعامل مع الكالسيوم. افترض المؤلفون أنه إذا أمكن حماية الميزات المعمارية الدقيقة للغشاء في هذه المنطقة، فربما يمكن إنقاذ وظيفة قلبية أكبر.
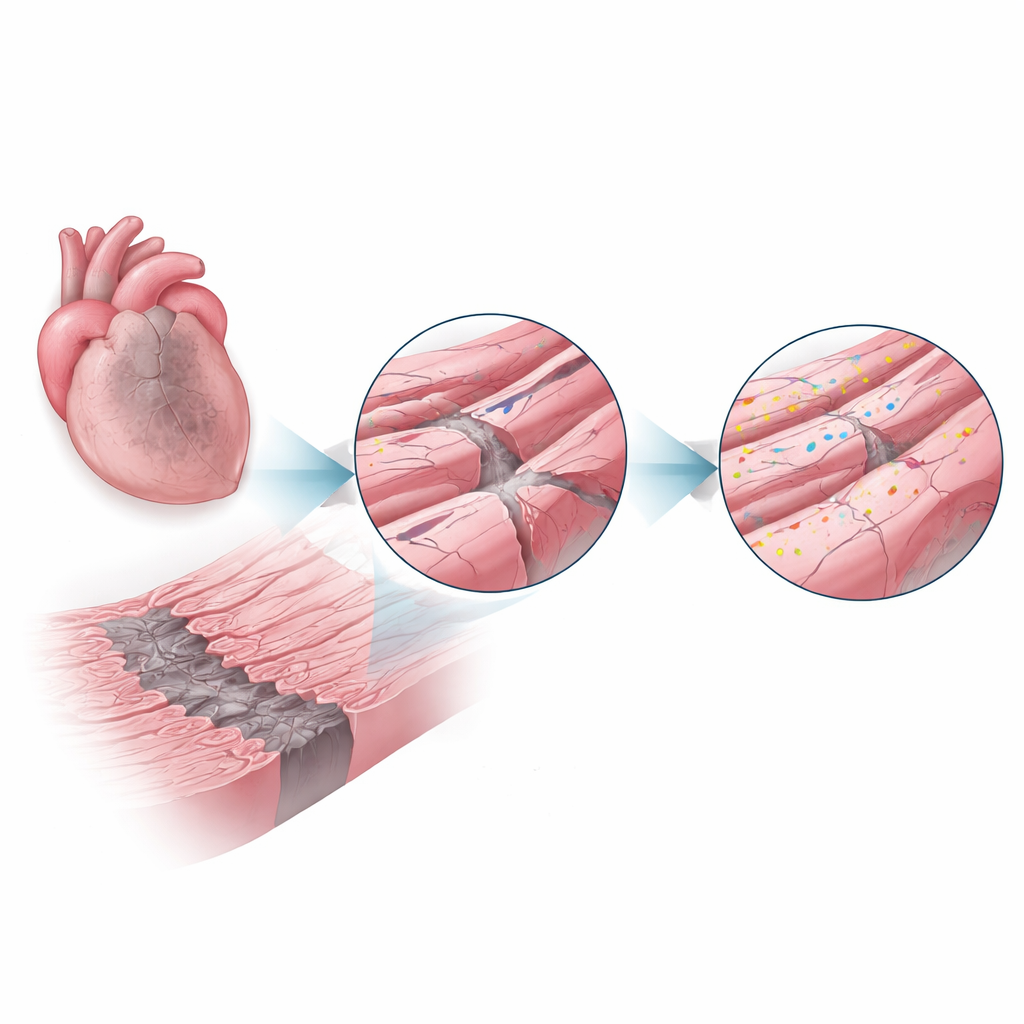
بروتين إصلاح يخطو إلى دائرة الضوء
الديسفيرلين بروتين كبير معروف من أمراض العضلات النادرة حيث يؤدي غيابه إلى ضعف العضلات الهيكلية، جزئياً لأن الألياف المتضررة لا تستطيع إصلاح أغشيتها بكفاءة. هنا، تساءل الباحثون ما إذا كان للديسفيرلين دور وقائي مماثل في القلب. باستخدام فئران كانت إما تملك ديسفيرلين طبيعي أو تفتقر إليه تماماً، أحدثوا نوبات قلبية وفحصوا القلوب بعد أسبوع وأربعة أسابيع. في الفئران الطبيعية، قفزت مستويات الديسفيرلين في منطقة الحد إلى أكثر من ضعفين مقارنة بالقلوب الصحية، ما يشير إلى أن الخلايا كانت تستدعي هذا النظام الإصلاحي حيث كان الإجهاد أعلى.
ماذا يحدث عند غياب الديسفيرلين
قارن الفريق بعد ذلك النتائج في الفئران التي تملك الديسفيرلين وتلك التي تفتقر إليه. طورت الحيوانات التي تفتقر إلى البروتين ندباً أكبر بكثير وبطينات يسرى أكثر تمدداً وضعفاً. كانت قلوبها تضخ دماً أقل مع كل نبضة، ما يبيّن أن جزءاً أكبر من النسيج القلبي الباقي قد فشل. سمحت تقنية مسح البروتينات المتقدمة للباحثين بفهرسة آلاف البروتينات في مناطق قلبية مختلفة. وجدوا أن نقص الديسفيرلين أعاد تشكيل هذه البروفايلات البروتينية، خصوصاً في مناطق الاحتشاء ومنطقة الحد، مغيراً مسارات مرتبطة بموت الخلايا والالتهاب وإشارات الكالسيوم—تغييرات تتوافق مع خلايا أكثر هشاشة وفشل متقدم.
العمارة المجهرية تحت الإصلاح
صُوّرت البنية الدقيقة لخلايا القلب بدقة عالية. في الأنسجة السليمة، ينغمس غشاء الخلية داخلياً في شبكة منتظمة من الأنفاق تُسمى شبكة القُصُور العرضية والمحورية، التي تساعد الإشارات الكهربائية على تحفيز إطلاق الكالسيوم والانقباض. بعد النوبة القلبية، أصبحت هذه الشبكة في منطقة الحد مشوشة وفُقد جزء منها، لا سيما العناصر العرضية. ومع ذلك، كانت الأنابيب المتبقية مغطاة بعناقيد لامعة من الديسفيرلين ومحاطة بفقاعات داخلية صغيرة من الغشاء، مما يوحي بحدوث إصلاح وإعادة تشكيل نشطة. عند وصلات الخلية بالخلية، حيث تتبادل خلايا القلب النبضات الكهربائية وتتلاصق مع بعضها، تراكم الديسفيرلين أيضاً إلى جانب بروتينات الوصل الأساسية. أظهرت تجارب كيميائية حيوية أن الديسفيرلين يرتبط فعلياً بهذه الشركاء في مركبات كبيرة، داعمةً الفكرة أنه يساعد في الحفاظ على هذه المواقع التلامسية وإعادة بنائها تحت الإجهاد.
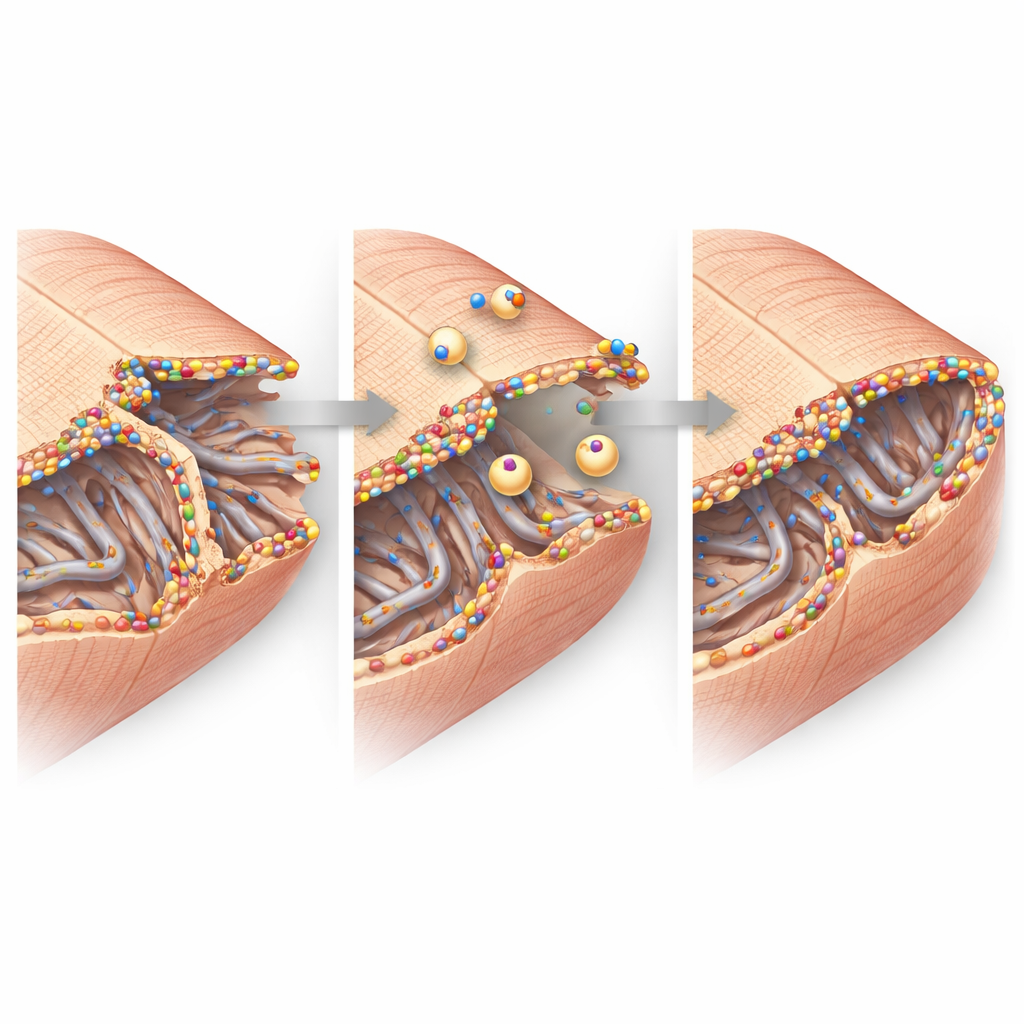
من الجزيئات إلى وظيفة القلب
بجمع هذه النتائج، تبرز الدراسة صورة للديسفيرلين كحارس لغشاء خلية القلب في منطقة الحد الضعيفة بعد النوبة القلبية. عندما يكون موجوداً ومعبرّاً عنه بكمية أكبر، يتجمع الديسفيرلين عند الشبكات الأنبوبية المتضررة وطيات وصلات الخلايا، مستدعياً حويصلات الإصلاح ومثبتاً هذه البنى الصغيرة ولكن الحيوية. عند غيابه، تنهار تلك الدعامات النانоскопية بسهولة أكبر، تُفقد أو تتعرض للمشكلات خلايا أكثر، وتتناقص قدرة القلب على الضخ. بالنسبة للمرضى، تشير هذه النتائج إلى أن تعزيز نشاط الديسفيرلين أو تقليد وظيفته الإصلاحية قد يصبح يوماً ما استراتيجية لتقليل فشل القلب بعد النوبة القلبية عن طريق حماية الأغشية التي تتيح لخلايا القلب النبض بانسجام.
الاستشهاد: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
الكلمات المفتاحية: احتشاء عضلة القلب, إصلاح غشاء خلايا القلب, ديسفيرلين, الوقاية من فشل القلب, إعادة تشكيل النانومجالات