Clear Sky Science · sv
Dysferlin stabiliserar membrannanodomäner i hjärtmuskelceller efter hjärtinfarkt
Varför hjärtceller behöver akut lagning
När någon överlever ett hjärtinfarkt börjar den verkliga kampen först. Det skadade området i hjärtat läker inte som ett enkelt sår; istället måste de överlevande hjärtmuskelcellerna i kanten av ärret fortsätta att kontrahera under intensiv mekanisk påfrestning. Denna studie visar hur ett relativt okänt reparationsprotein, dysferlin, fungerar som en sorts mikroskopiskt lagningskit för dessa överbelastade celler, hjälper deras känsliga membran att hålla ihop och bevara hjärtats pumpförmåga.
Den påfrestande gränsen mellan liv och ärr
Efter en hjärtinfarkt blockeras blodflödet till en del av hjärtat, vilket dödar många celler och lämnar ett centralt ärr. Runt denna döda kärna finns en smal ”gränszon” av fortfarande levande hjärtmuskelceller som utsätts för låg syretillförsel, inflammation och kraftig uttänjning för varje hjärtslag. Dessa förhållanden stressar cellernas yttermembran och dess invecklade veck, som rymmer viktiga strukturer för elektriska signaler och kalciumhantering. Författarna antog att om membranets små arkitektoniska egenskaper kunde skyddas i denna zon, skulle mer hjärtfunktion kunna räddas.
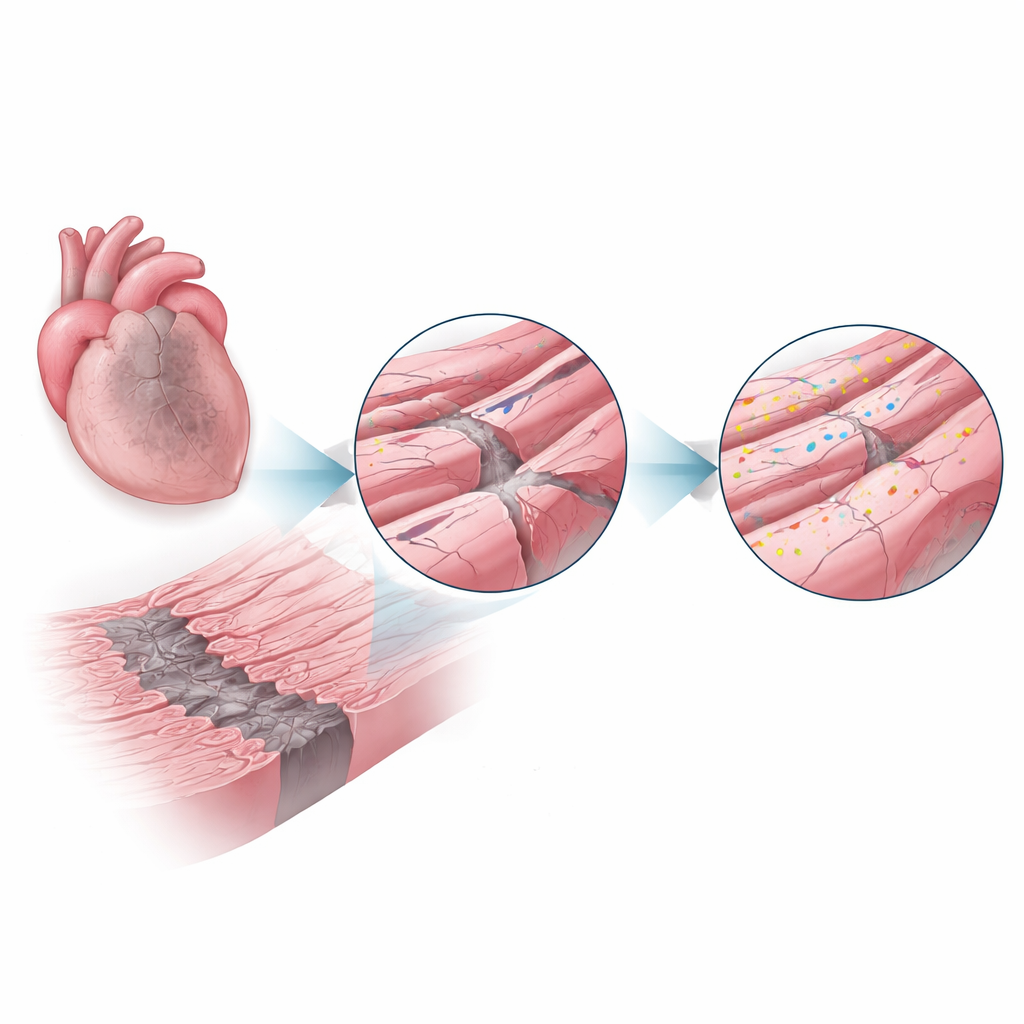
Ett reparationsprotein träder fram
Dysferlin är ett stort protein känt från sällsynta muskelsjukdomar där dess frånvaro leder till svaga skelettmuskler, delvis eftersom skadade fibrer inte kan reparera sina membran effektivt. Här undersökte forskarna om dysferlin spelar en liknande skyddande roll i hjärtat. Genom att använda möss som antingen hade normal dysferlinnivå eller saknade proteinet helt, inducerade de hjärtinfarkter och undersökte hjärtana en respektive fyra veckor senare. Hos normala möss ökade dysferlinnivåerna i gränszonen till mer än dubbla jämfört med friska hjärtan, vilket tyder på att cellerna aktivt kallade in detta reparationssystem där påfrestningen var som störst.
Vad som händer när dysferlin saknas
Gruppen jämförde sedan utfallen hos möss med och utan dysferlin. Djur som saknade proteinet utvecklade avsevärt större ärr och mer utspända, svagare vänsterkammare. Deras hjärtan pumpade mindre blod per slag, vilket visar att mer av den överlevande hjärtmuskulaturen hade sviktat. En kraftfull proteomanalysteknik gjorde det möjligt för forskarna att katalogisera tusentals proteiner i olika hjärtregioner. De fann att dysferlinbrist omformade dessa proteinprofiler, särskilt i infarkt- och gränszonerna, och påverkade vägar kopplade till celldöd, inflammation och kalciumsignalering — förändringar som stämmer överens med mer sårbara celler och progressiv svikt.
Den mikroskopiska arkitekturen under reparation
Avancerad avbildning zoomade in på hjärtmuskelcellernas fina struktur. I frisk vävnad böjer sig cellmembranet inåt i ett regelbundet gitter av tunnlar kallade det tvärgående–axiala tubulätverket, vilket hjälper elektriska signaler att utlösa kalciumfrisättning och kontraktion. Efter en hjärtinfarkt blev detta nätverk i gränszonen oorganiserat och delvis förlorat, särskilt dess tvärgående element. Ändå var de kvarvarande tubulerna täckta av ljusa kluster av dysferlin och omgivna av små inre membranblåsor, vilket antyder aktiv reparation och ombyggnad. Vid cell–cell‑junctionerna, där hjärtceller utbyter elektriska impulser och fäster vid varandra, ansamlades också dysferlin tillsammans med nyckelproteiner för kontakterna. Biokemiska experiment visade att dysferlin fysiskt associerar med dessa partners i stora komplex, vilket stöder idén att det hjälper till att bibehålla och bygga upp dessa kontaktpunkter under stress.
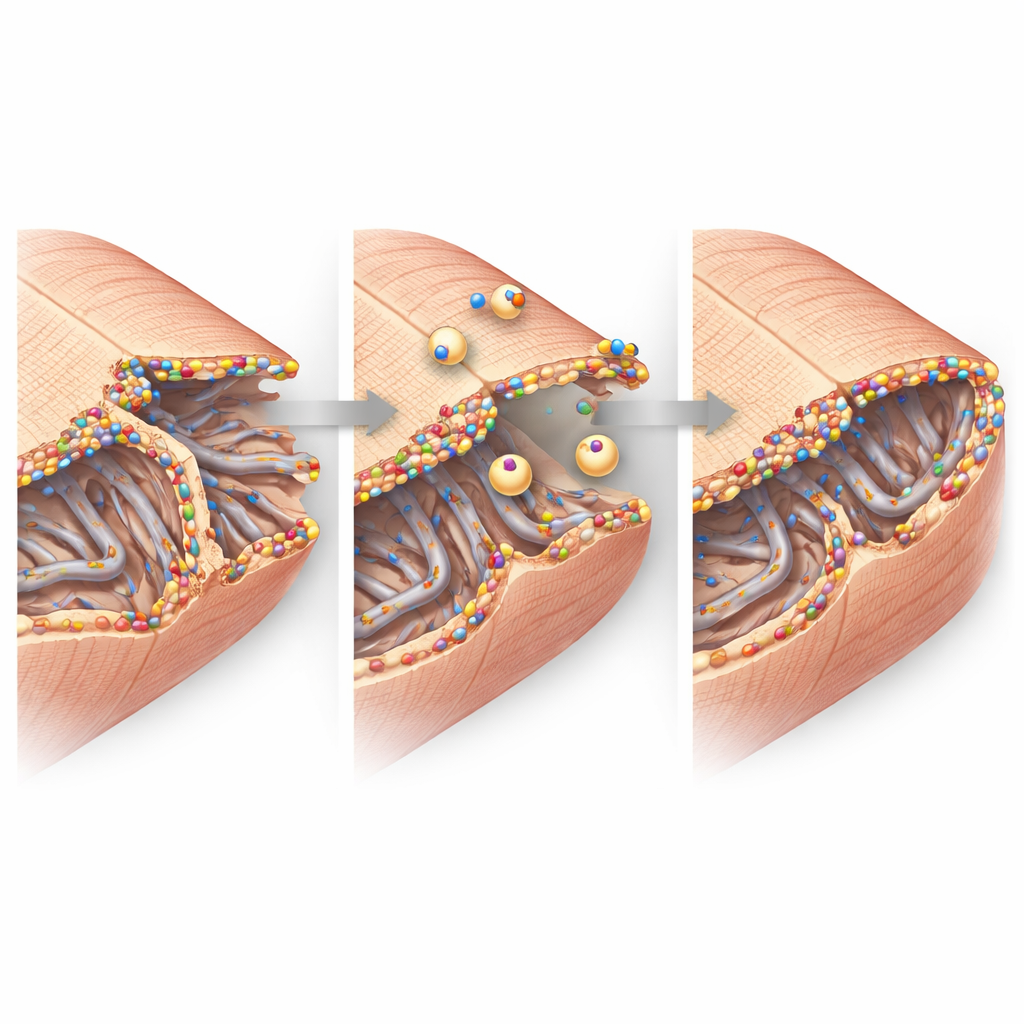
Från molekyler till hjärtfunktion
Sammanfattningsvis målar studien upp en bild av dysferlin som en väktare av hjärtmuskelcellens membran i den sårbara gränszonen efter en hjärtinfarkt. När det är närvarande och uppreglerat klustras dysferlin vid skadade tubulära nätverk och cell–cell‑junctioners veck, rekryterar reparationsvesiklar och stabiliserar dessa små men viktiga strukturer. När det saknas kollapsar dessa nanoskala stödfunktioner lättare, fler celler går förlorade eller fungerar dåligt och hjärtats pumpförmåga sjunker. För patienter tyder detta arbete på att förstärkning av dysferlinaktivitet eller efterliknande av dess reparationsfunktion en dag skulle kunna bli en strategi för att begränsa hjärtsvikt efter en hjärtinfarkt genom att skydda just de membran som gör att hjärtceller kan slå i takt.
Citering: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Nyckelord: hjärtinfarkt, reparation av hjärtmuskelcellers membran, dysferlin, förebyggande av hjärtsvikt, ombyggnad av nanodomäner