Clear Sky Science · de
Dysferlin stabilisiert Membran‑Nanobereiche von Kardiomyozyten nach Myokardinfarkt
Warum Herzmuskelzellen Notfallflicken brauchen
Wenn jemand einen Herzinfarkt überlebt, hat der eigentliche Kampf gerade erst begonnen. Der geschädigte Bereich des Herzens heilt nicht wie ein einfacher Schnitt; vielmehr müssen die überlebenden Herzmuskelzellen am Rand der Narbe unter enormer mechanischer Belastung weiter kontrahieren. Diese Studie zeigt, wie ein wenig bekanntes Reparaturprotein, Dysferlin, als eine Art mikroskopisches Flickzeug für diese überlasteten Zellen wirkt, ihre empfindlichen Membranen zusammenhält und so die Pumpkraft des Herzens bewahrt.
Die belastende Grenze zwischen Leben und Narbe
Nach einem Herzinfarkt ist die Blutversorgung eines Herzbezirks unterbrochen, viele Zellen sterben ab und es bildet sich eine zentrale Narbe. Um diesen toten Kern herum liegt eine schmale „Grenzzone“ mit noch lebenden Herzmuskelzellen, die in jeder Kontraktion niedrigen Sauerstoffwerten, Entzündung und starkem Dehnen ausgesetzt sind. Diese Bedingungen belasten die Zellmembran und ihre komplexen Faltungen, die wichtige Strukturen für elektrische Signale und Kalziumregulation beherbergen. Die Autoren vermuteten, dass mehr Herzfunktion erhalten bleiben könnte, wenn die winzigen architektonischen Merkmale der Membran in dieser Zone geschützt würden.
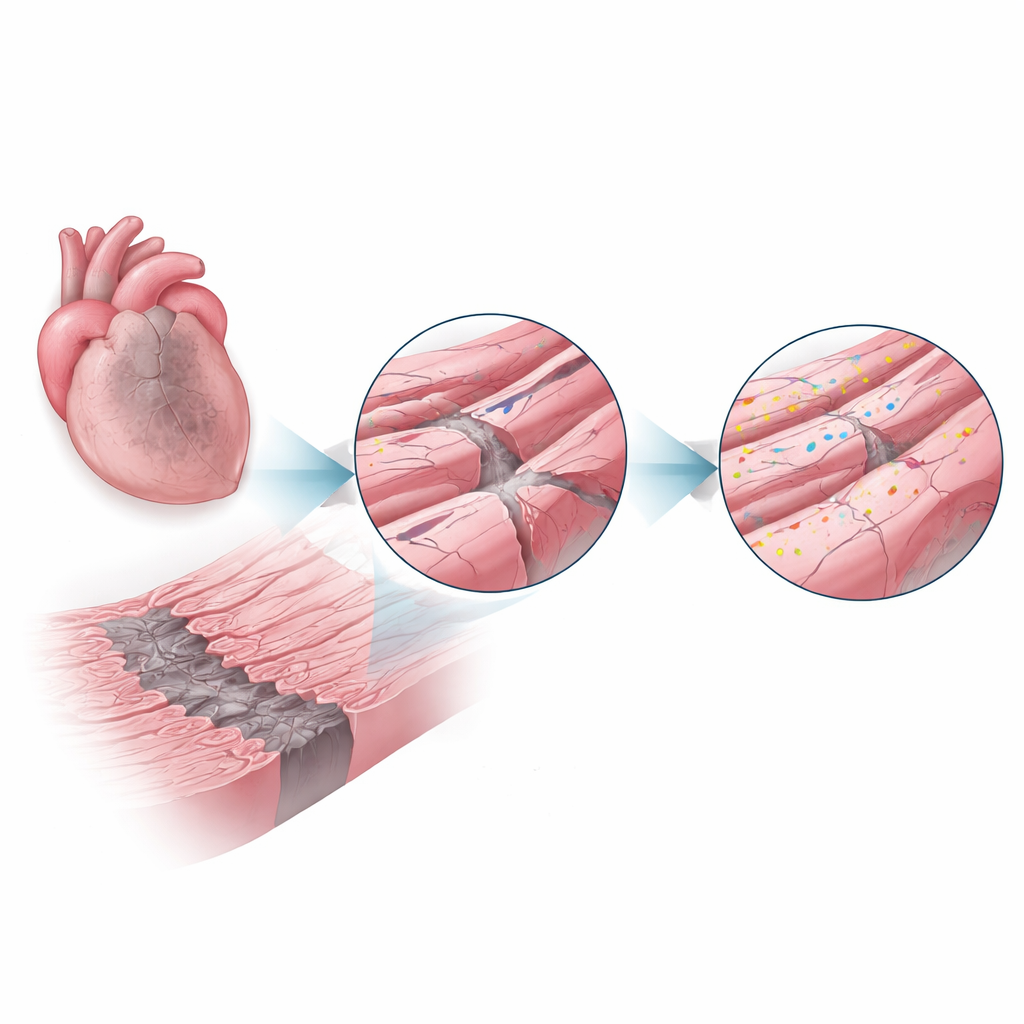
Ein Reparaturprotein rückt ins Rampenlicht
Dysferlin ist ein großes Protein, das aus seltenen Muskelerkrankungen bekannt ist, bei denen sein Fehlen zu schwachen Skelettmuskeln führt, weil beschädigte Fasern ihre Membranen nicht effizient reparieren können. Hier untersuchten die Forschenden, ob Dysferlin eine vergleichbare Schutzfunktion im Herzen übernimmt. An Mäusen mit normalem Dysferlingehalt oder vollständigem Fehlen des Proteins lösten sie Herzinfarkte aus und untersuchten die Herzen eine und vier Wochen später. Bei normalen Mäusen stiegen die Dysferlinspiegel in der Grenzzone auf mehr als das Doppelte gegenüber gesunden Herzen, was darauf hindeutet, dass die Zellen dieses Reparatursystem gezielt dorthin rekrutieren, wo die Belastung am höchsten ist.
Was passiert, wenn Dysferlin fehlt
Das Team verglich dann die Ergebnisse bei Mäusen mit und ohne Dysferlin. Tiere ohne das Protein entwickelten deutlich größere Narben und stärker dilatierte, schwächere linke Ventrikel. Ihre Herzen pumpten bei jedem Schlag weniger Blut, was darauf hinweist, dass mehr des überlebenden Myokards versagte. Eine leistungsfähige Proteomanalyse ermöglichte es den Forschenden, Tausende Proteine in verschiedenen Herzregionen zu katalogisieren. Sie fanden heraus, dass Dysferlinmangel diese Proteinprofile umgestaltete, besonders in Infarkt‑ und Grenzzonen, und Signalwege veränderte, die mit Zelltod, Entzündung und Kalziumsignalisierung verbunden sind — Veränderungen, die zu zerbrechlicheren Zellen und fortschreitendem Versagen passen.
Mikroskopische Architektur unter Reparatur
Hochauflösende Bildgebung blickte auf die feine Struktur der Herzmuskelzellen. In gesundem Gewebe wölbt sich die Zellmembran regelmäßig in ein Gitter von Kanälen, das transversale–axiale Tubulusnetzwerk, das elektrische Signale an die Kalziumfreisetzung und Kontraktion koppelt. Nach einem Herzinfarkt wurde dieses Netzwerk in der Grenzzone unorganisiert und teilweise verloren, besonders seine transversalen Elemente. Die verbliebenen Tubuli waren jedoch mit hellen Dysferlin‑Clustern überzogen und von kleinen inneren Membranblasen umgeben, was auf aktive Reparatur und Umgestaltung hindeutet. An den Zell‑Zell‑Verbindungen, wo Herzzellen elektrische Impulse austauschen und aneinander haften, sammelte sich Dysferlin ebenfalls neben Schlüsselproteinen der Kontakte. Biochemische Experimente zeigten, dass Dysferlin physisch mit diesen Partnern in großen Komplexen assoziiert, was die Idee stützt, dass es hilft, diese Kontaktstellen unter Stress zu erhalten und wieder aufzubauen.
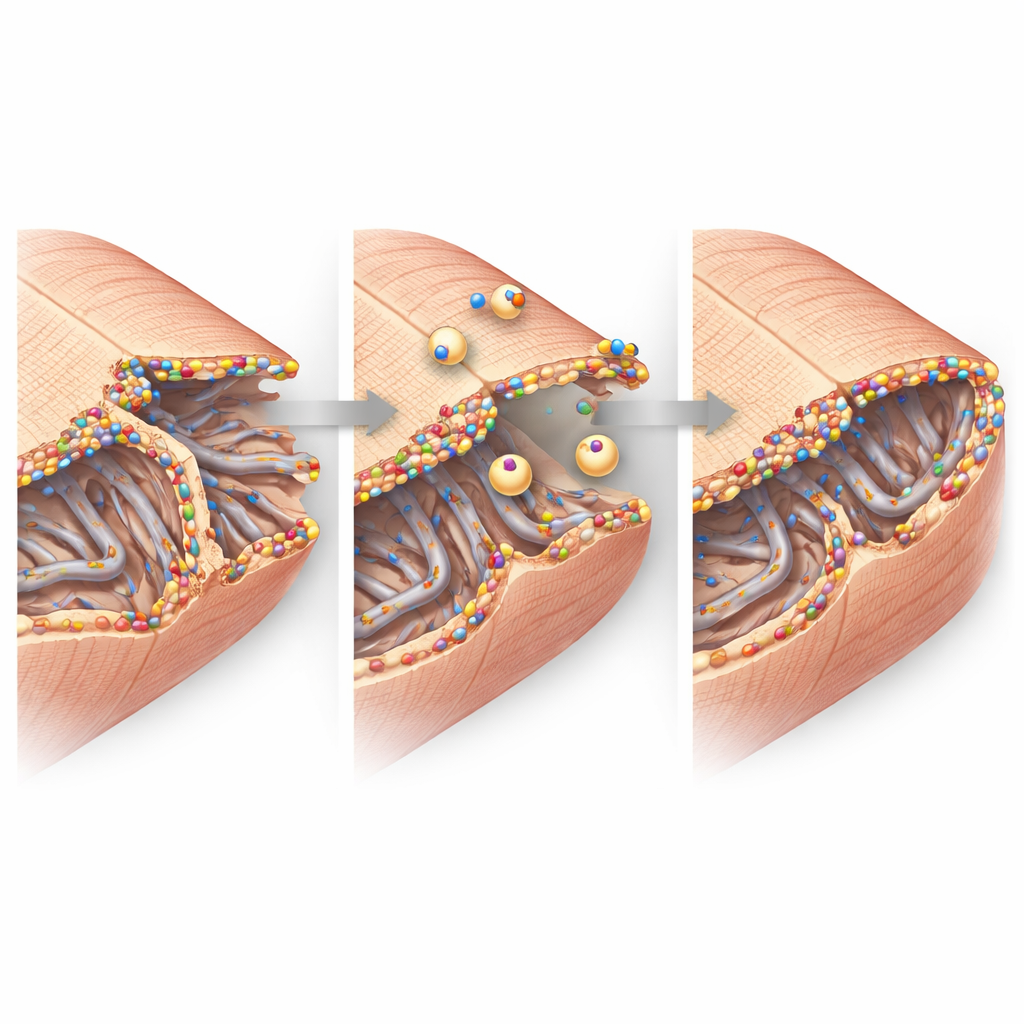
Von Molekülen zur Herzfunktion
Zusammengefasst zeichnet die Studie das Bild von Dysferlin als Wächter der Herzmuskelzellmembran in der verletzlichen Grenzzone nach einem Herzinfarkt. Wenn es vorhanden und hochreguliert ist, konzentriert sich Dysferlin an beschädigten tubulären Netzwerken und Faltungen der Zell‑Zell‑Verbindungen, zieht Reparaturvesikel an und stabilisiert diese winzigen, aber kritischen Strukturen. Fehlt es, bröckeln diese nanoskopischen Stützstrukturen leichter, mehr Zellen gehen verloren oder funktionieren nicht mehr richtig, und die Pumpkraft des Herzens nimmt ab. Für Patientinnen und Patienten deutet diese Arbeit darauf hin, dass eine Verstärkung der Dysferlin‑Aktivität oder das Nachahmen seiner Reparaturfunktion eines Tages eine Strategie sein könnte, um nach einem Herzinfarkt Herzinsuffizienz zu begrenzen, indem die Membranen geschützt werden, die es den Herzzellen ermöglichen, im Gleichklang zu schlagen.
Zitation: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Schlüsselwörter: Myokardinfarkt, Reparatur der Kardiomyozytenmembran, Dysferlin, Prävention von Herzinsuffizienz, Umgestaltung von Nanobereichen