Clear Sky Science · nl
Dysferline stabiliseert membraannanodomeinen van cardiomyocyten na myocardinfarct
Waarom hartcellen noodpleisters nodig hebben
Wanneer iemand een hartaanval overleeft, is de echte strijd vaak pas begonnen. Het beschadigde gebied van het hart geneest niet als een simpele snee; in plaats daarvan moeten de overgebleven hartspiercellen aan de rand van het litteken blijven samentrekken onder intense mechanische spanning. Deze studie laat zien hoe een weinig bekend reparatie-eiwit, dysferline, fungeert als een soort microscopische pleisterset voor deze overbelaste cellen, waardoor hun fragiele membranen bij elkaar blijven en de pompkracht van het hart behouden blijft.
De stressvolle grens tussen leven en litteken
Na een hartaanval wordt de bloedtoevoer naar een deel van het hart geblokkeerd, waardoor veel cellen direct afsterven en een centraal litteken ontstaat. Rondom deze dode kern bevindt zich een smalle “grenszone” van nog levende hartspiercellen die te maken hebben met lage zuurstoftoevoer, ontsteking en krachtige uitrekking bij elke slag. Deze omstandigheden belasten het buitenmembraan van de cellen en zijn ingewikkelde plooien, die cruciale structuren voor elektrische signalen en calciumhuishouding huisvesten. De auteurs vermoedden dat als de kleine architectonische kenmerken van het membraan in deze zone beschermd konden worden, meer hartfunctie behouden zou blijven.
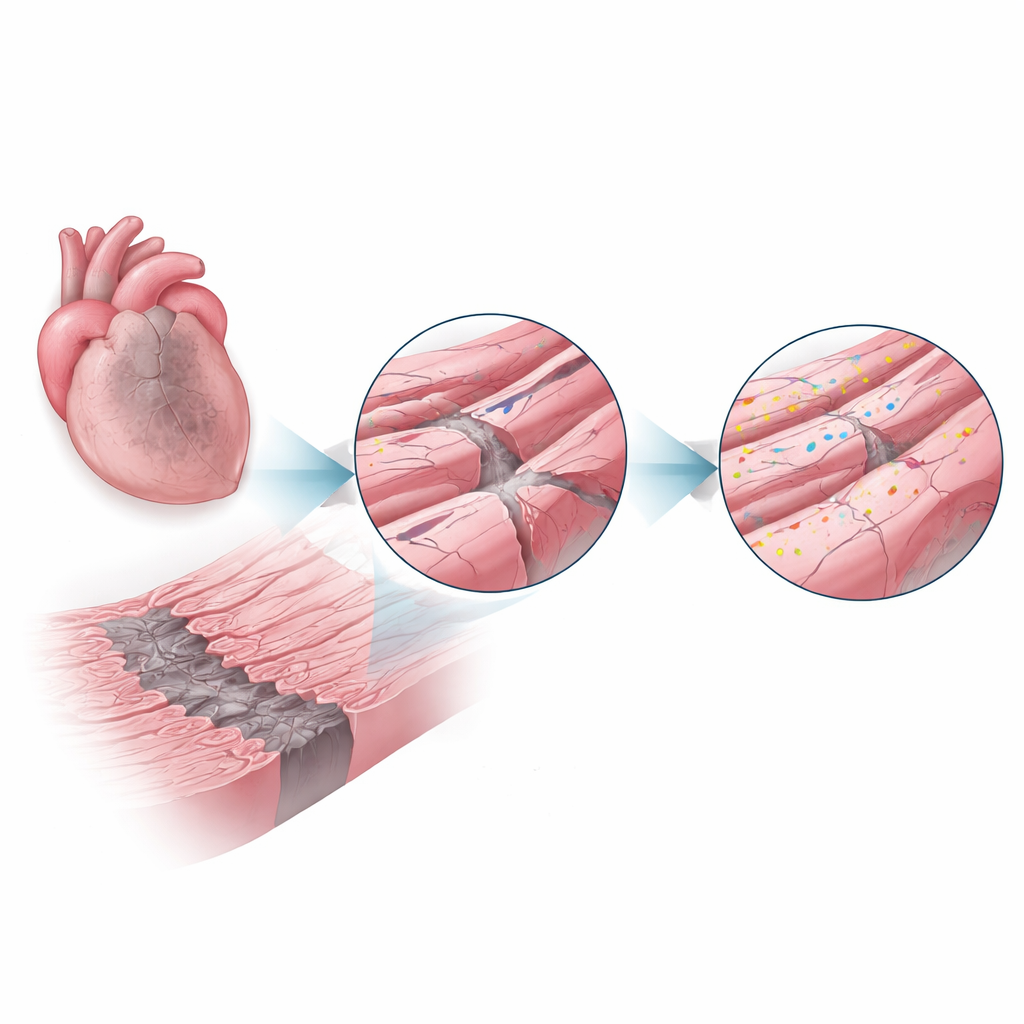
Een reparatie-eiwit treedt in de schijnwerpers
Dysferline is een groot eiwit dat bekend is uit zeldzame spieraandoeningen waarbij het ontbreken ervan leidt tot zwakke skeletspieren, deels omdat beschadigde vezels hun membranen niet efficiënt kunnen herstellen. Hier vroegen onderzoekers of dysferline een vergelijkbare beschermende rol in het hart vervult. Met muizen die ofwel normaal dysferline hadden of er volledig geen van bezaten, veroorzaakten ze hartaanvallen en onderzochten de harten één en vier weken later. Bij normale muizen steeg het dysferlineniveau in de grenszone tot meer dan het dubbele van dat in gezonde harten, wat suggereert dat de cellen dit reparatiesysteem actief inzetten waar de stress het grootst was.
Wat er gebeurt als dysferline ontbreekt
Het team vergeleek vervolgens de uitkomsten bij muizen met en zonder dysferline. Dieren zonder het eiwit ontwikkelden aanzienlijk grotere littekens en meer verwijden en verzwakken van de linker hartkamer. Hun harten persten bij elke slag minder bloed naar buiten, wat aangeeft dat meer van het overgebleven myocardium faalde. Met een krachtige eiwitvangertechniek konden de onderzoekers duizenden eiwitten in verschillende hartregio’s in kaart brengen. Ze ontdekten dat dysferlinegebrek deze eiwitprofielen herschikte, vooral in het infarct- en grensgebied, en routes veranderde die verband houden met celdood, ontsteking en calcium‑signaalering — veranderingen die overeenkomen met fragielere cellen en voortschrijdend falen.
Microscopische architectuur in herstel
Beeldvorming met hoge resolutie zoomde in op de fijne structuur van de hartcellen. In gezond weefsel buigt het celmembraan naar binnen in een regelmatig raster van tunnels, de transversaal–axiale tubulaire netwerken, die elektrische signalen helpen om calcium vrij te maken en contractie te starten. Na een hartaanval raakte dit netwerk in de grenszone gedesorganiseerd en deels verdwenen, vooral de transversale componenten. Toch waren de overgebleven tubuli bedekt met felle clusters van dysferline en omgeven door kleine interne membraanblaasjes, wat wijst op actieve reparatie en remodeling. Bij de cel‑cel verbindingen, waar hartcellen elektrische impulsen uitwisselen en aan elkaar hechten, stapelde dysferline zich ook op naast sleutelproteïnen van die verbindingen. Biochemische experimenten toonden aan dat dysferline fysiek met deze partners samenhangt in grote complexen, wat de gedachte ondersteunt dat het helpt deze contactplaatsen onder stress te behouden en te herbouwen.
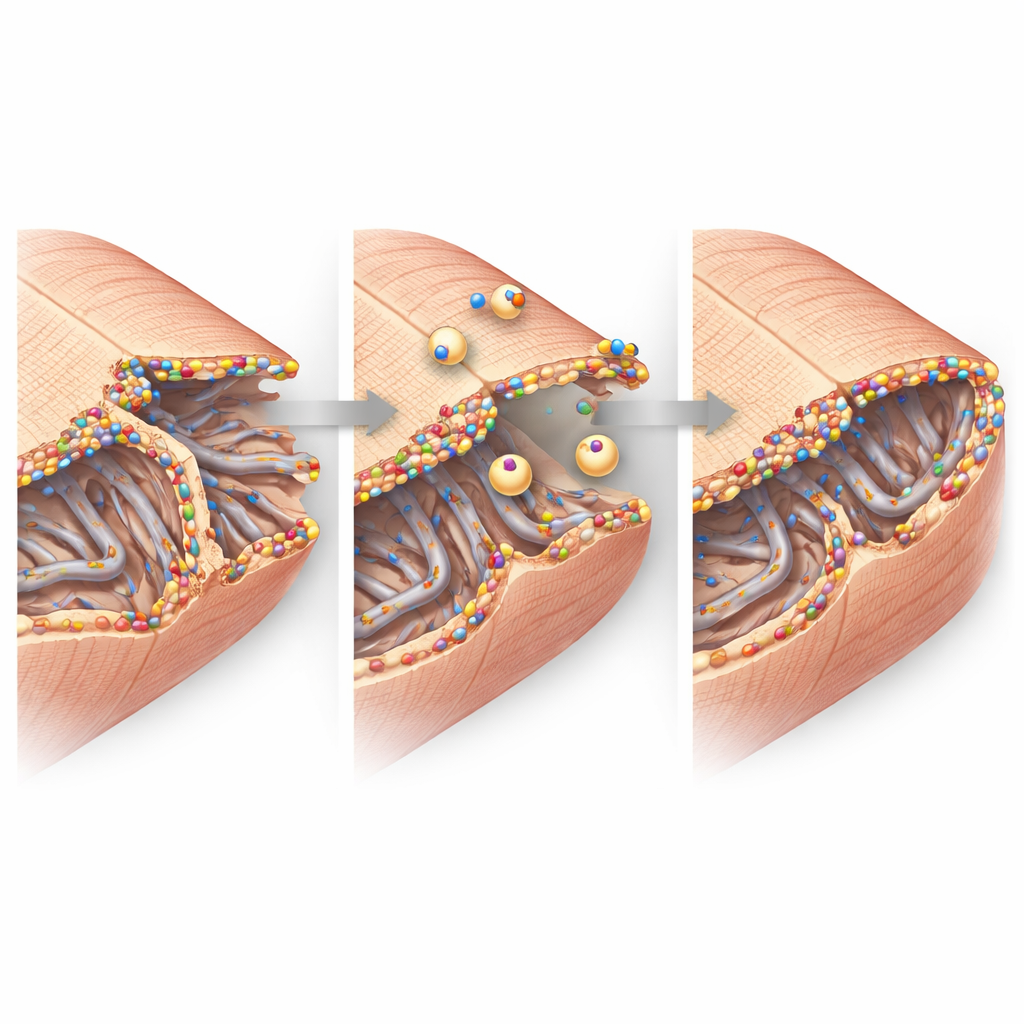
Van moleculen naar hartfunctie
Al deze bevindingen samen schetsen het beeld van dysferline als bewaker van het celmembraan in de kwetsbare grenszone na een hartaanval. Wanneer het aanwezig is en opgeregeld wordt, clustert dysferline bij beschadigde tubulaire netwerken en cel‑cel plooien, trekt het reparatieve vesikels aan en stabiliseert het deze kleine maar kritieke structuren. Wanneer het ontbreekt, bezwijken die nanoscopische steunpunten gemakkelijker, gaan meer cellen verloren of functioneren ze niet goed, en neemt de pompkracht van het hart af. Voor patiënten suggereert dit werk dat het versterken van dysferline‑activiteit of het nabootsen van zijn reparatiefunctie op een dag een strategie zou kunnen worden om hartfalen na een hartaanval te beperken door precies die membranen te beschermen die ervoor zorgen dat hartcellen synchroon blijven kloppen.
Bronvermelding: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Trefwoorden: myocardinfarct, herstel van cardiomyocytenmembraan, dysferline, preventie van hartfalen, nanodomeinhermodellering