Clear Sky Science · fr
La dysférline stabilise les nanodomaines membranaires des cardiomyocytes après un infarctus du myocarde
Pourquoi les cellules cardiaques ont besoin de rustines d’urgence
Quand une personne survit à un infarctus, la véritable lutte ne fait que commencer. La région endommagée du cœur ne cicatrise pas comme une simple coupure ; les cellules musculaires cardiaques survivantes au bord de la cicatrice doivent continuer à se contracter sous un stress mécanique intense. Cette étude révèle comment une protéine de réparation peu connue, la dysférline, agit comme une sorte de trousse de réparation microscopique pour ces cellules sursollicitées, aidant leurs membranes délicates à rester intactes et préservant ainsi la capacité de pompage du cœur.
La frontière stressante entre la vie et la cicatrice
Après un infarctus, le flux sanguin est bloqué vers une partie du cœur, tuant de nombreuses cellules sur le coup et laissant une cicatrice centrale. Autour de ce noyau mort se trouve une « zone de transition » étroite de cellules musculaires cardiaques encore vivantes qui subissent un faible apport en oxygène, une inflammation et des étirements puissants à chaque battement. Ces conditions mettent à l’épreuve la membrane externe des cellules et ses replis complexes, qui abritent des structures cruciales pour la conduction électrique et la gestion du calcium. Les auteurs ont supposé que si les minuscules caractéristiques architecturales de la membrane pouvaient être protégées dans cette zone, une plus grande partie de la fonction cardiaque pourrait être préservée.
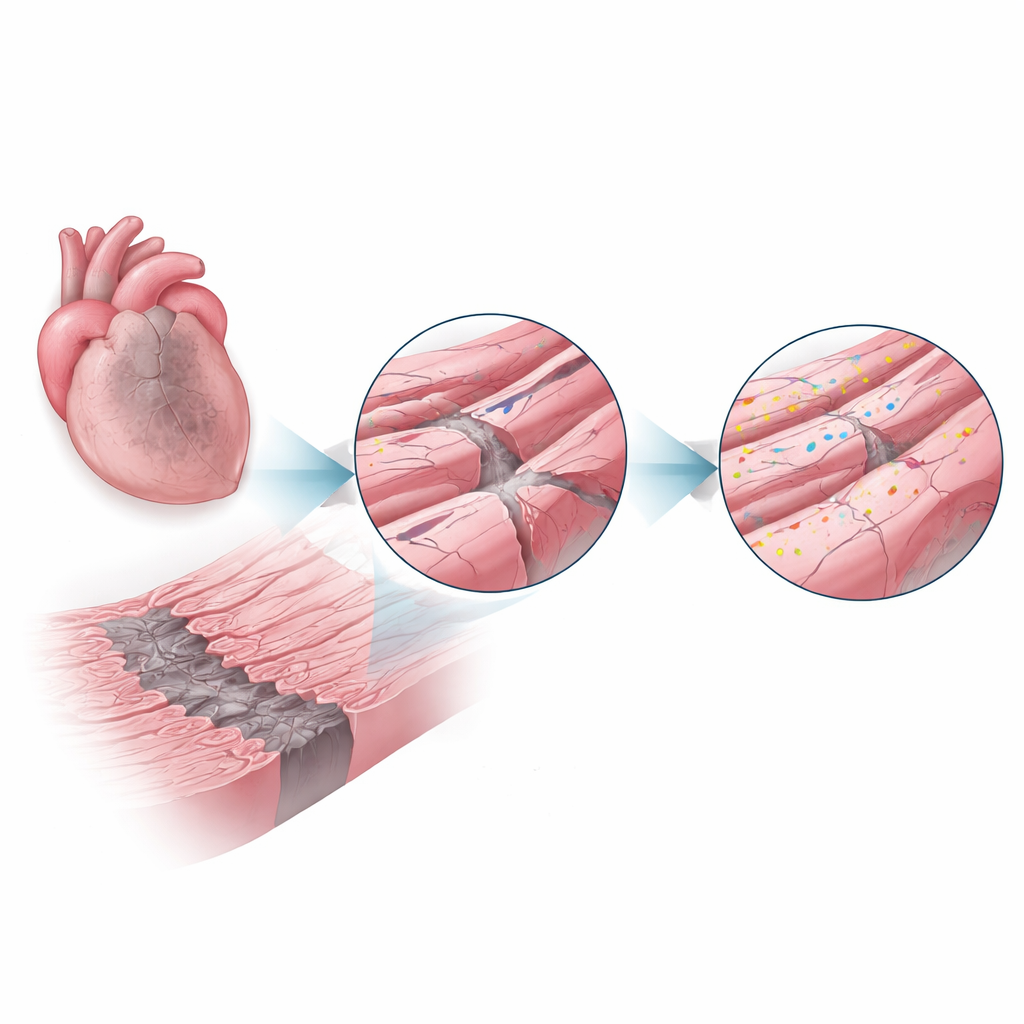
Une protéine de réparation entre en lumière
La dysférline est une grande protéine connue dans des maladies musculaires rares où son absence entraîne une faiblesse des muscles squelettiques, en partie parce que les fibres endommagées ne peuvent pas réparer efficacement leurs membranes. Ici, les chercheurs se sont demandé si la dysférline jouait un rôle protecteur similaire dans le cœur. En utilisant des souris ayant soit une dysférline normale soit une absence totale de celle-ci, ils ont provoqué des infarctus et examiné les cœurs une et quatre semaines plus tard. Chez les souris normales, les niveaux de dysférline dans la zone de transition ont augmenté pour dépasser le double de ceux des cœurs sains, suggérant que les cellules faisaient appel activement à ce système de réparation là où le stress était le plus élevé.
Que se passe-t-il quand la dysférline manque
L’équipe a ensuite comparé les résultats chez les souris avec et sans dysférline. Les animaux dépourvus de la protéine ont développé des cicatrices significativement plus larges et des ventricules gauches plus dilatés et plus faibles. Leurs cœurs ont pompé moins de sang à chaque battement, indiquant qu’une plus grande partie du myocarde survivant avait failli. Une technique puissante d’analyse protéique a permis aux chercheurs de cataloguer des milliers de protéines dans différentes régions cardiaques. Ils ont constaté que l’absence de dysférline remodelait ces profils protéiques, en particulier dans les zones nécrosées et de transition, modifiant des voies liées à la mort cellulaire, à l’inflammation et à la signalisation calcique — des changements cohérents avec des cellules plus fragiles et une défaillance progressive.
Architecture microscopique en cours de réparation
Des images à haute résolution ont zoomé sur la structure fine des cellules cardiaques. Dans les tissus sains, la membrane cellulaire s’enfonce en un réseau régulier de tunnels appelés réseau transverse–axial de tubules, qui aide les signaux électriques à déclencher la libération de calcium et la contraction. Après un infarctus, ce réseau dans la zone de transition est devenu désorganisé et partiellement perdu, en particulier ses éléments transverses. Pourtant, les tubules restants étaient recouverts d’amas lumineux de dysférline et entourés de petites vésicules internes de membrane, suggérant une réparation et un remodelage actifs. Aux jonctions cellule–cellule, où les cellules cardiaques échangent des impulsions électriques et restent attachées les unes aux autres, la dysférline s’est également accumulée aux côtés de protéines de jonction clés. Des expériences biochimiques ont montré que la dysférline s’associe physiquement à ces partenaires au sein de grands complexes, soutenant l’idée qu’elle aide à maintenir et à reconstruire ces sites de contact sous stress.
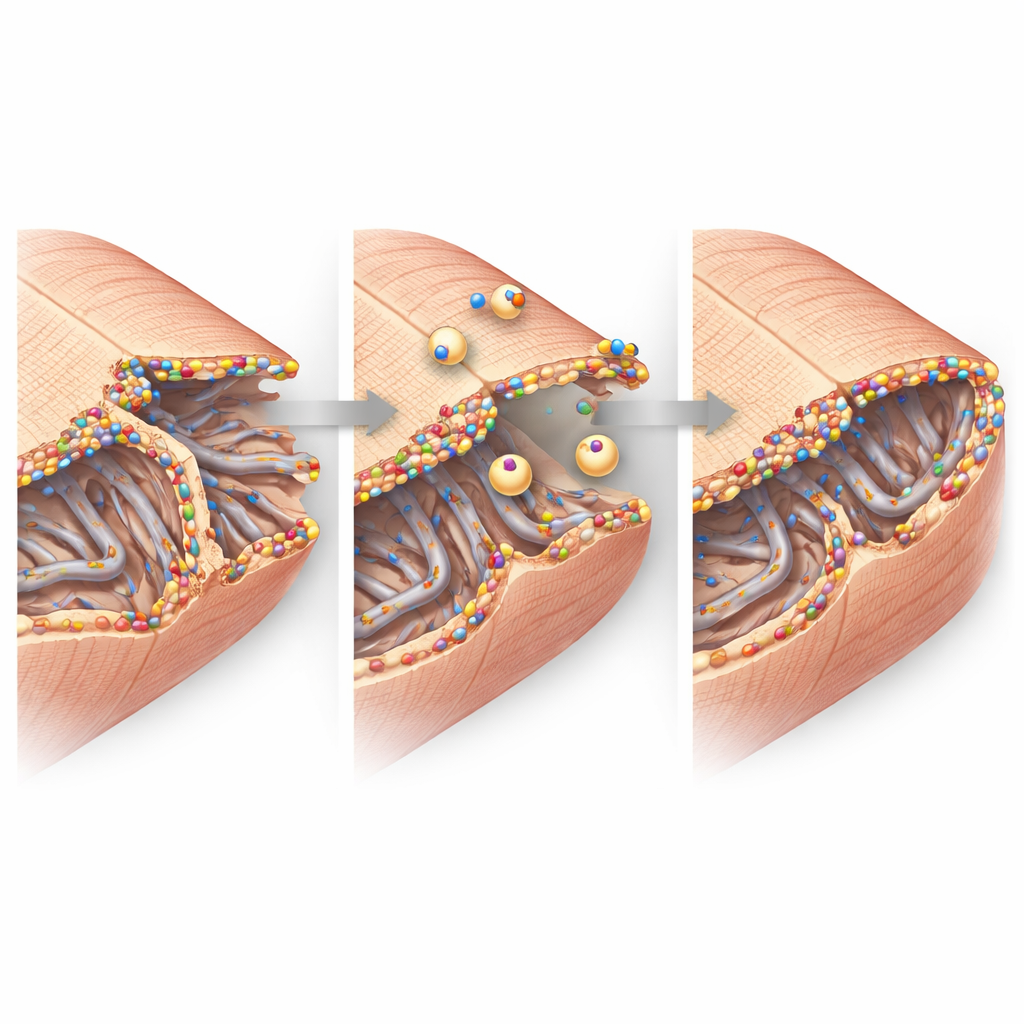
Des molécules à la fonction cardiaque
En réunissant ces observations, l’étude dresse le portrait de la dysférline comme gardienne de la membrane des cellules cardiaques dans la zone de transition vulnérable après un infarctus. Lorsqu’elle est présente et régulée à la hausse, la dysférline se regroupe au niveau des réseaux tubulaires endommagés et des replis des jonctions cellule–cellule, attirant des vésicules de réparation et stabilisant ces structures minuscules mais critiques. En son absence, ces soutiens nanoscopiques s’effondrent plus facilement, davantage de cellules sont perdues ou dysfonctionnent, et la capacité de pompage du cœur décline. Pour les patients, ce travail suggère qu’augmenter l’activité de la dysférline ou imiter sa fonction de réparation pourrait un jour devenir une stratégie pour limiter l’insuffisance cardiaque après un infarctus en protégeant les membranes mêmes qui permettent aux cellules cardiaques de battre à l’unisson.
Citation: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Mots-clés: infarctus du myocarde, réparation de la membrane du cardiomyocyte, dysférline, prévention de l’insuffisance cardiaque, remodelage des nanodomaines