Clear Sky Science · es
La disferlina estabiliza nanodominios de membrana de los cardiomiocitos tras el infarto de miocardio
Por qué las células cardíacas necesitan parches de emergencia
Cuando una persona sobrevive a un infarto, la verdadera batalla apenas comienza. La zona dañada del corazón no cicatriza como un corte sencillo; en su lugar, las células musculares cardíacas supervivientes en el borde de la cicatriz deben seguir contrayéndose bajo un estrés mecánico intenso. Este estudio revela cómo una proteína de reparación poco conocida, la disferlina, actúa como una suerte de kit de parches microscópico para estas células sobrecargadas, ayudando a que sus membranas delicadas se mantengan intactas y preservando la capacidad de bombeo del corazón.
La frontera estresante entre la vida y la cicatriz
Tras un infarto, el flujo sanguíneo queda bloqueado en una parte del corazón, lo que mata a muchas células y deja una cicatriz central. Alrededor de ese núcleo muerto existe una estrecha «zona limítrofe» de células musculares cardiacas todavía vivas que soportan bajo oxígeno, inflamación y potentes estiramientos con cada latido. Estas condiciones tensionan la membrana externa de las células y sus repliegues intrincados, que albergan estructuras cruciales para las señales eléctricas y el manejo del calcio. Los autores sospecharon que si las pequeñas características arquitectónicas de la membrana pudieran protegerse en esta zona, se podría salvar más función cardíaca.
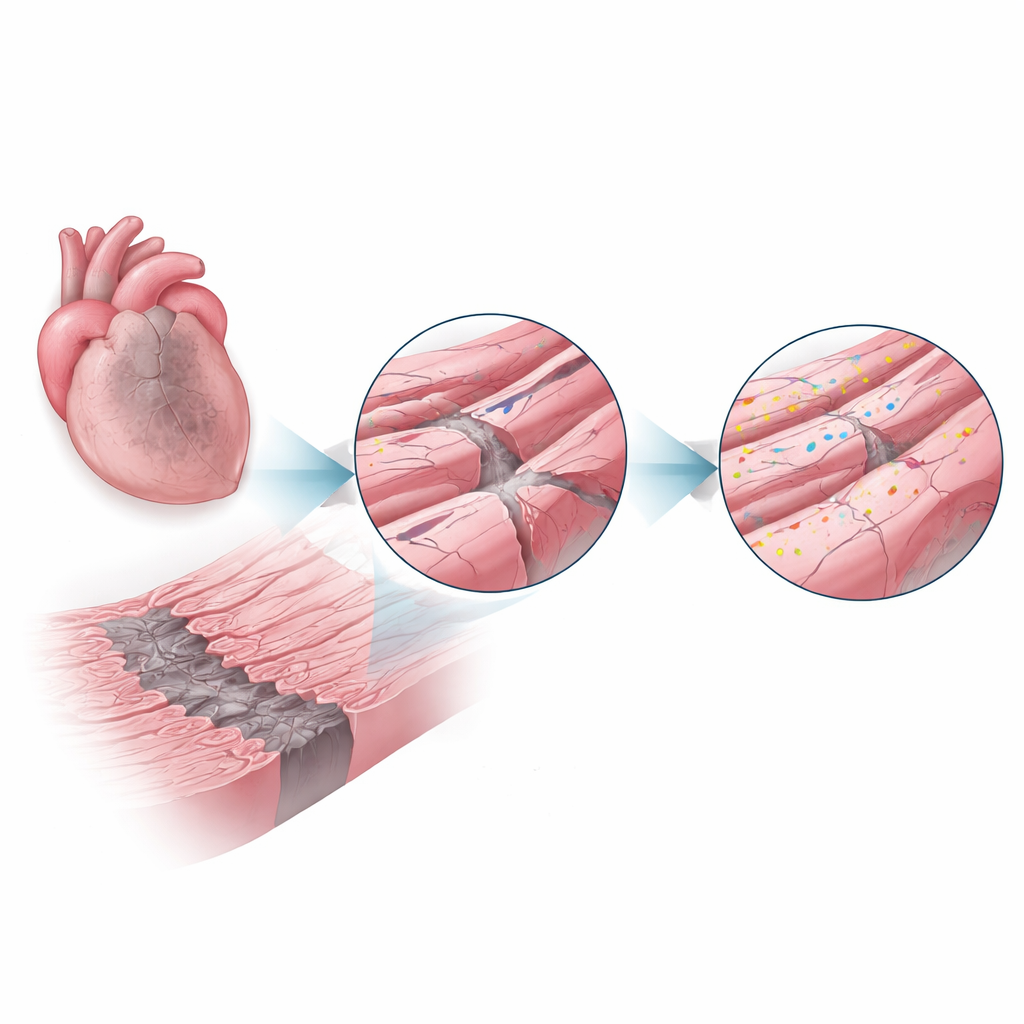
Una proteína reparadora toma el protagonismo
La disferlina es una proteína grande conocida por enfermedades musculares raras en las que su ausencia conduce a debilidad del músculo esquelético, en parte porque las fibras dañadas no pueden reparar sus membranas con eficacia. Aquí, los investigadores se preguntaron si la disferlina desempeña un papel protector similar en el corazón. Usando ratones que tenían disferlina normal o carecían totalmente de ella, inducieron infartos y examinaron los corazones una y cuatro semanas después. En los ratones normales, los niveles de disferlina en la zona limítrofe se dispararon a más del doble que en corazones sanos, lo que sugiere que las células estaban reclutando activamente este sistema de reparación donde el estrés era mayor.
Qué ocurre cuando falta la disferlina
El equipo comparó entonces los resultados en ratones con y sin disferlina. Los animales carentes de la proteína desarrollaron cicatrices significativamente mayores y ventrículos izquierdos más dilatados y debilitados. Sus corazones bombeaban menos sangre en cada latido, lo que indica que más del miocardio superviviente había fallado. Una potente técnica de cribado proteico permitió a los investigadores catalogar miles de proteínas en diferentes regiones del corazón. Encontraron que la deficiencia de disferlina reconfiguró estos perfiles proteicos, especialmente en las zonas de infarto y limítrofe, alterando vías vinculadas a la muerte celular, la inflamación y la señalización del calcio: cambios coherentes con células más frágiles y una progresiva insuficiencia.
Arquitectura microscópica bajo reparación
Imágenes de alta resolución se acercaron a la estructura fina de las células cardíacas. En tejido sano, la membrana celular se hunde hacia el interior en una red regular de túneles llamada red transversa–axial de túbulos, que ayuda a que las señales eléctricas desencadenen la liberación de calcio y la contracción. Tras un infarto, esta red en la zona limítrofe se volvió desorganizada y se perdió parcialmente, en particular sus elementos transversales. Sin embargo, los túbulos restantes estaban recubiertos por racimos brillantes de disferlina y rodeados por pequeñas vesículas internas de membrana, lo que sugiere reparación y remodelado activos. En las uniones célula–célula, donde las células cardíacas intercambian impulsos eléctricos y se adhieren entre sí, la disferlina también se acumuló junto a proteínas clave de unión. Experimentos bioquímicos mostraron que la disferlina se asocia físicamente con estos socios en complejos grandes, apoyando la idea de que ayuda a mantener y reconstruir estos sitios de contacto bajo estrés.
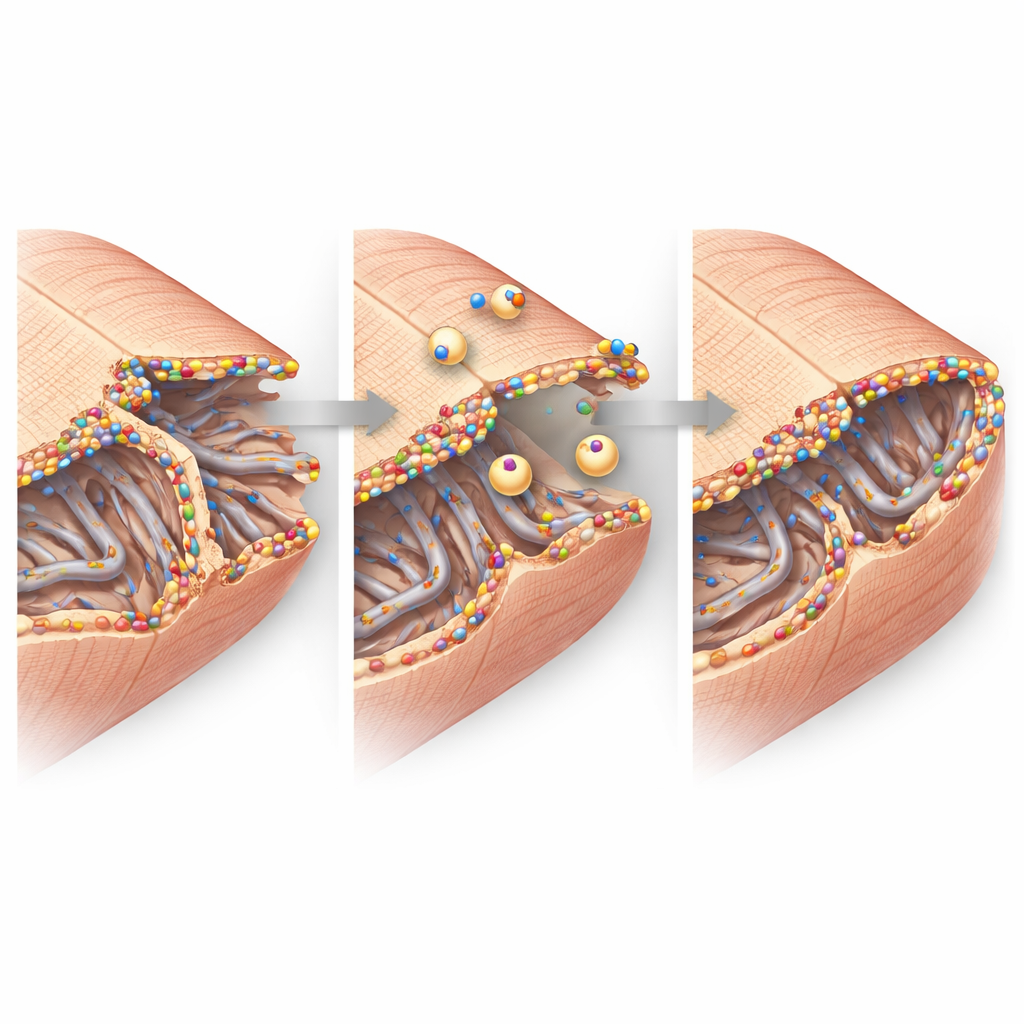
De las moléculas a la función cardíaca
Al reunir estos hallazgos, el estudio dibuja el retrato de la disferlina como guardiana de la membrana de las células cardíacas en la vulnerable zona limítrofe tras un infarto. Cuando está presente y sobreexpresada, la disferlina se agrupa en redes tubulares dañadas y pliegues de las uniones célula–célula, atrayendo vesículas de reparación y estabilizando estas estructuras diminutas pero críticas. Cuando falta, esos soportes nanoscópicos se desmoronan más fácilmente, se pierden o disfuncionan más células y la capacidad de bombeo del corazón disminuye. Para los pacientes, este trabajo sugiere que potenciar la actividad de la disferlina o imitar su función reparadora podría algún día convertirse en una estrategia para limitar la insuficiencia cardíaca tras un infarto al proteger las mismas membranas que permiten que las células cardíacas latan al unísono.
Cita: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Palabras clave: infarto de miocardio, reparación de la membrana del cardiomiocito, disferlina, prevención de insuficiencia cardíaca, remodelado de nanodominios