Clear Sky Science · it
La disferlina stabilizza i nanodomini di membrana dei cardiomiociti dopo l'infarto miocardico
Perché le cellule cardiache hanno bisogno di rattoppi d'emergenza
Quando una persona sopravvive a un attacco cardiaco, la vera battaglia è appena iniziata. La regione danneggiata del cuore non guarisce come un semplice taglio; le cellule muscolari cardiache sopravvissute al margine della cicatrice devono continuare a contrarsi sotto intenso stress meccanico. Questo studio rivela come una proteina di riparazione poco conosciuta, la disferlina, agisca come una sorta di kit microscopico di rattoppi per queste cellule sovraccaricate, aiutando le loro membrane delicate a rimanere integre e preservando la capacità di pompaggio del cuore.
Il confine stressante tra vita e cicatrice
Dopo un infarto, il flusso sanguigno viene interrotto in una parte del cuore, uccidendo molte cellule e lasciando una cicatrice centrale. Intorno a questo nucleo morto c'è una stretta «zona di confine» di cellule muscolari ancora vive che subiscono ipossia, infiammazione e potenti stiramenti a ogni battito. Queste condizioni sollecitano la membrana esterna delle cellule e i suoi pieghetti intricati, che ospitano strutture cruciali per i segnali elettrici e la gestione del calcio. Gli autori hanno ipotizzato che se le minuscole caratteristiche architettoniche della membrana potessero essere protette in questa zona, si potrebbe salvare una maggiore funzione cardiaca.
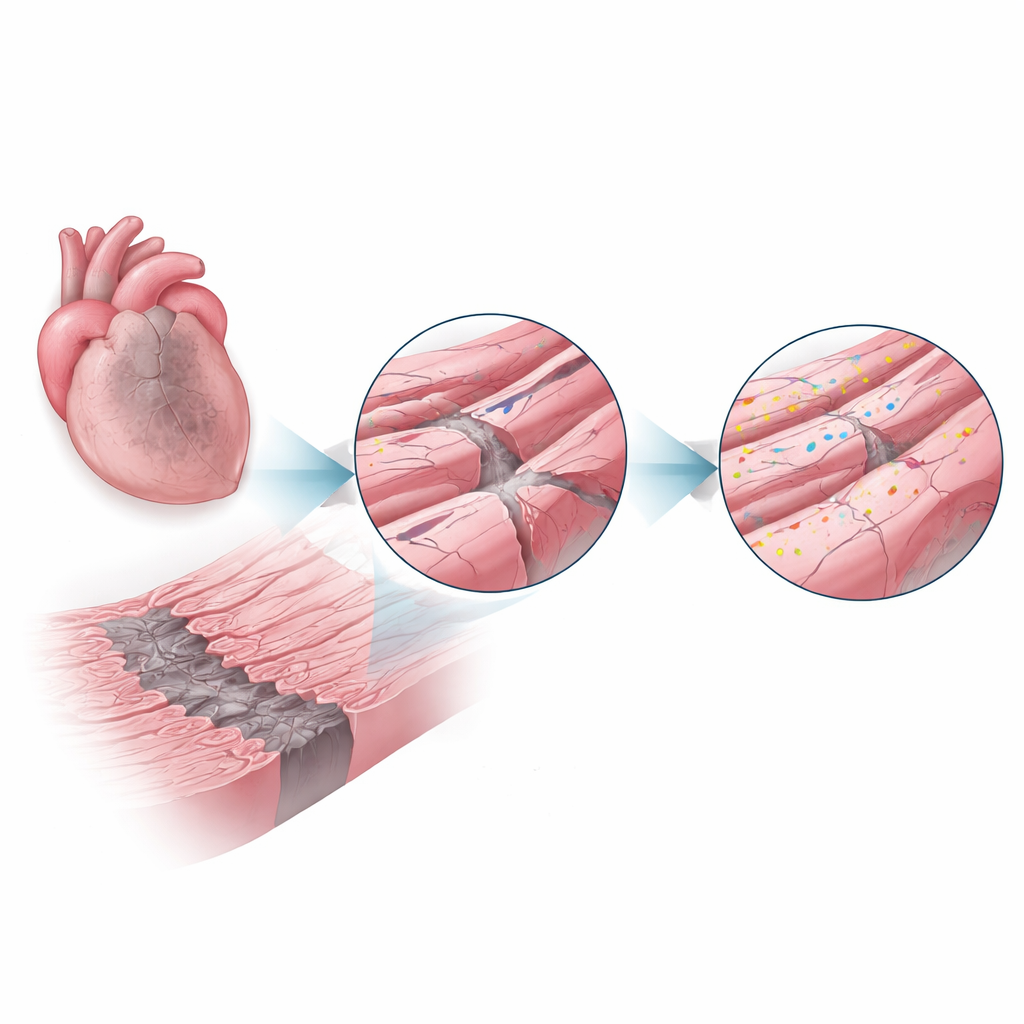
Una proteina di riparazione entra sotto i riflettori
La disferlina è una proteina di grandi dimensioni nota per malattie muscolari rare in cui la sua assenza porta a muscoli scheletrici deboli, in parte perché le fibre danneggiate non riescono a riparare efficacemente le membrane. Qui i ricercatori si sono chiesti se la disferlina svolga un ruolo protettivo simile nel cuore. Utilizzando topi con livelli normali di disferlina o privi completamente della proteina, hanno indotto infarti e analizzato i cuori dopo una e quattro settimane. Nei topi normali i livelli di disferlina nella zona di confine sono aumentati a più del doppio rispetto ai cuori sani, suggerendo che le cellule richiamassero attivamente questo sistema di riparazione dove lo stress era maggiore.
Cosa succede quando la disferlina manca
Il gruppo ha poi confrontato gli esiti in topi con e senza disferlina. Gli animali privi della proteina hanno sviluppato cicatrici significativamente più ampie e ventricoli sinistri più dilatati e deboli. I loro cuori pompavano meno sangue a ogni battito, indicando che una maggiore porzione del miocardio sopravvissuto aveva ceduto. Una potente tecnica di indagine proteica ha permesso ai ricercatori di catalogare migliaia di proteine in diverse regioni cardiache. Hanno rilevato che la carenza di disferlina rimodellava questi profili proteici, soprattutto nelle zone di infarto e di confine, alterando percorsi legati alla morte cellulare, all'infiammazione e alla segnalazione del calcio — cambiamenti coerenti con cellule più fragili e un progressivo deterioramento.
Architettura microscopica in riparazione
Immagini ad alta risoluzione hanno ingrandito la struttura fine delle cellule cardiache. Nel tessuto sano, la membrana cellulare si infossa in una griglia regolare di tunnel chiamata rete dei tubuli trasverso-assiali, che aiuta i segnali elettrici a innescare il rilascio di calcio e la contrazione. Dopo un infarto, questa rete nella zona di confine è diventata disorganizzata e in parte perduta, in particolare i suoi elementi trasversali. Tuttavia i tubuli rimasti erano rivestiti da brillanti aggregati di disferlina e circondati da piccole bolle interne di membrana, suggerendo un'attività di riparazione e rimodellamento. Alle giunzioni cellula-cellula, dove le cellule cardiache scambiano impulsi elettrici e si ancorano reciprocamente, la disferlina si accumulava insieme a proteine chiave delle giunzioni. Esperimenti biochimici hanno mostrato che la disferlina si associa fisicamente con questi partner in complessi di grandi dimensioni, sostenendo l'idea che aiuti a mantenere e ricostruire questi siti di contatto sotto stress.
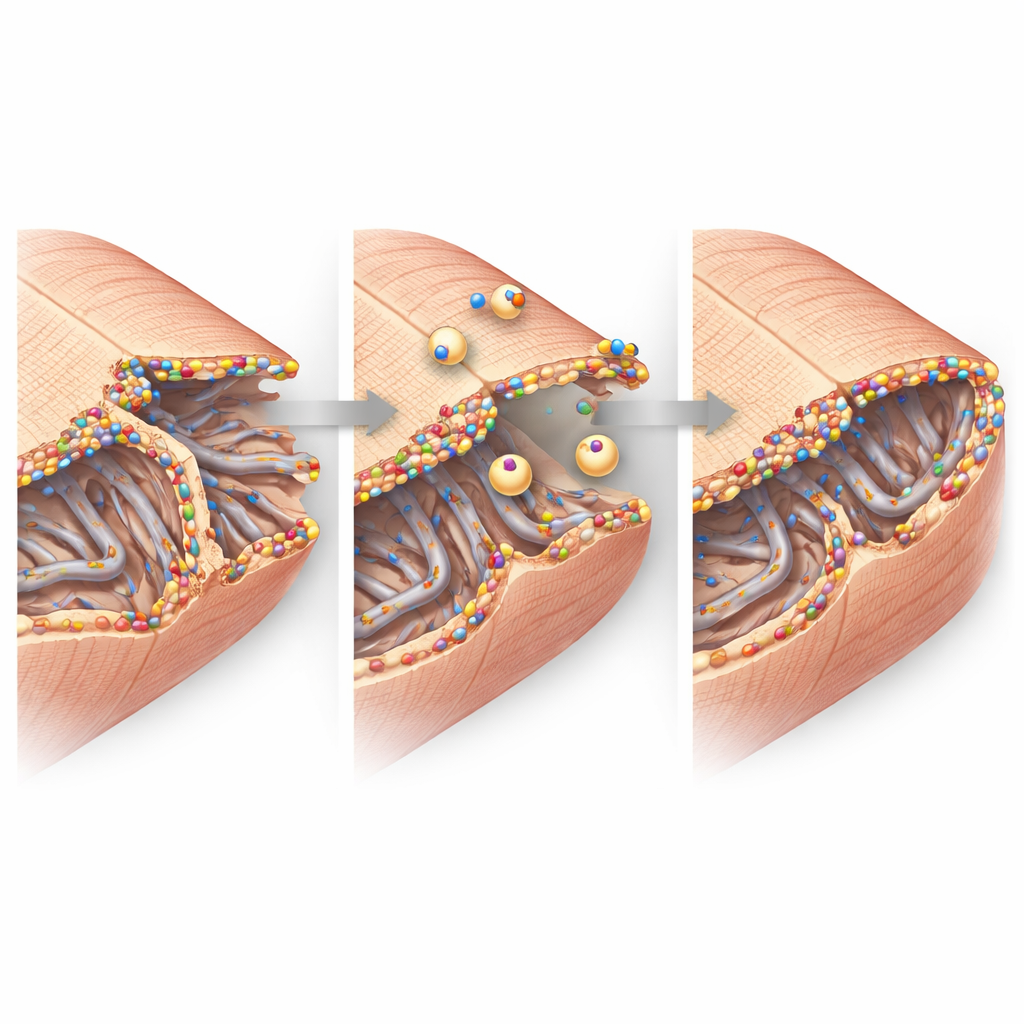
Dalle molecole alla funzione cardiaca
Mettere insieme questi risultati disegna il ritratto della disferlina come guardiano della membrana delle cellule cardiache nella vulnerabile zona di confine dopo un infarto. Quando è presente e sovraregolata, la disferlina si concentra nelle reti tubulari danneggiate e nelle pieghe delle giunzioni cellula-cellula, attirando vescicole di riparazione e stabilizzando queste strutture minuscole ma critiche. Quando manca, quei supporti nanoscopici crollano più facilmente, più cellule vengono perse o funzionano male e la capacità di pompaggio del cuore diminuisce. Per i pazienti, questo lavoro suggerisce che potenziare l'attività della disferlina o imitare la sua funzione di riparazione potrebbe un giorno diventare una strategia per limitare l'insufficienza cardiaca dopo un infarto proteggendo le membrane che permettono alle cellule cardiache di battere all'unisono.
Citazione: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Parole chiave: infarto miocardico, riparazione della membrana del cardiomiocita, disferlina, prevenzione dell'insufficienza cardiaca, rimodellamento dei nanodomini