Clear Sky Science · ru
Дисферлин стабилизирует мембранные нанообласти кардиомиоцитов после инфаркта миокарда
Почему сердечным клеткам нужна экстренная заплатка
Когда человек переживает сердечный приступ, настоящая борьба только начинается. Поврежденный участок сердца не заживает как простая рана; выжившие сердечные мышечные клетки по краю рубца продолжают сокращаться при сильной механической нагрузке. В этом исследовании показано, как малоизвестный белок ремонта, дисферлин, действует как крошечный набор для починки для этих перегруженных клеток, помогая их тонким мембранам сохранять целостность и поддерживая насосную функцию сердца.
Напряженная граница между жизнью и рубцом
После инфаркта кровоток перекрывается в части сердца, что приводит к гибели многих клеток и образованию центрального рубца. Вокруг этой мертвой зоны располагается узкая «пограничная зона» из еще живых кардиомиоцитов, которые терпят дефицит кислорода, воспаление и сильное растяжение при каждом сокращении. Эти условия нагружают наружную мембрану клеток и ее сложные складки, где расположены ключевые структуры для электрической проводимости и обращения кальция. Авторы предположили, что если в этой зоне удастся защитить микроскопические архитектурные элементы мембраны, можно сохранить больше сердечной функции.
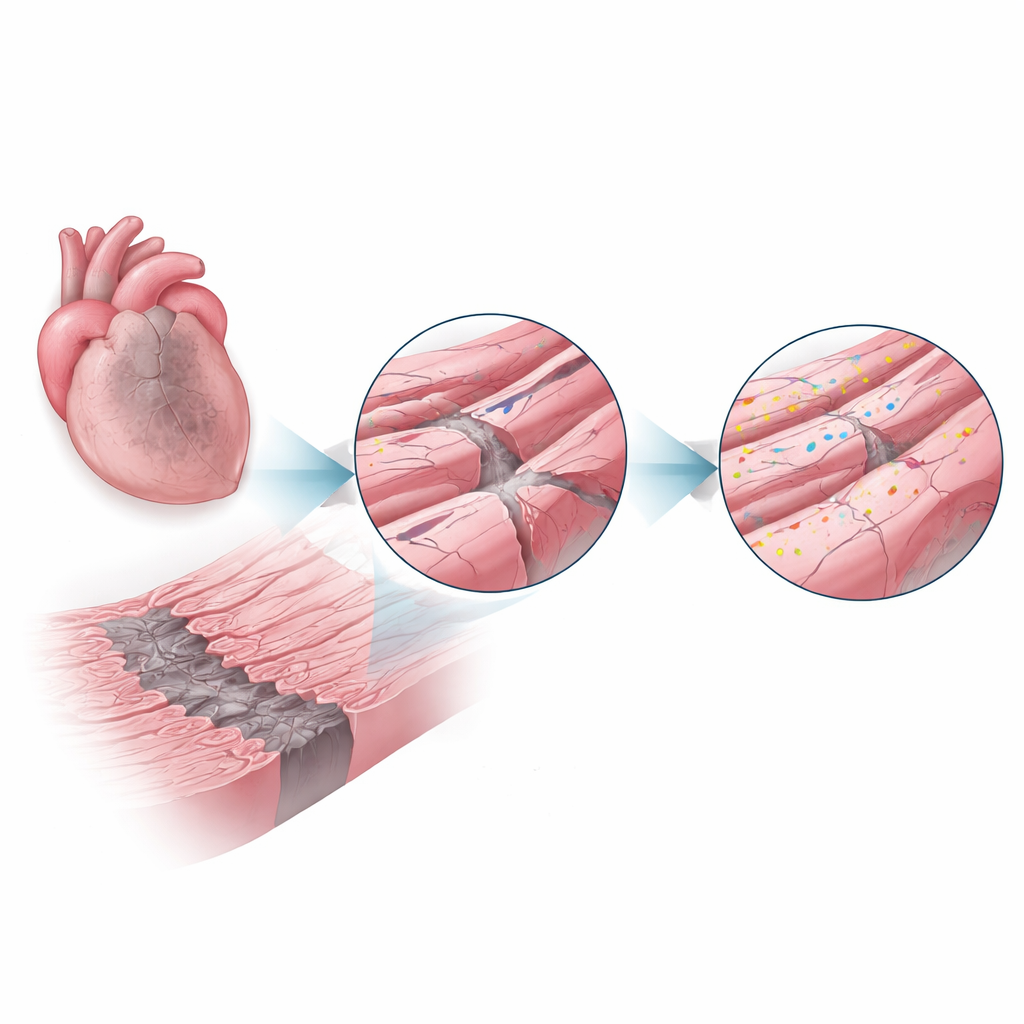
Белок ремонта выходит на передний план
Дисферлин — крупный белок, известный по редким мышечным заболеваниям, при которых его отсутствие приводит к ослаблению скелетной мускулатуры, отчасти потому, что поврежденные волокна не могут эффективно восстанавливать свои мембраны. В этой работе исследователи проверили, выполняет ли дисферлин похожую защитную роль в сердце. На мышах с нормальным дисферлином и без него индуцировали инфаркты и изучали сердце через одну и четыре недели. У нормальных животных уровень дисферлина в пограничной зоне резко вырос — более чем вдвое по сравнению со здоровым сердцем, что указывает на активный набор этого механизма ремонта именно там, где стресс был наибольшим.
Что происходит при отсутствии дисферлина
Затем команда сравнила исходы у мышей с дисферлином и без него. Животные, лишенные белка, развивали значительно большие рубцы и более дилатированные, ослабленные левовентрикулярные камеры. Их сердца выбрасывали меньше крови за одно сокращение, что свидетельствует о том, что большая часть выжившего миокарда утратила функцию. Мощный протеомный анализ позволил исследователям каталогизировать тысячи белков в разных областях сердца. Они обнаружили, что дефицит дисферлина изменяет эти белковые профили, особенно в зоне инфаркта и пограничной области, затрагивая пути, связанные со смертью клеток, воспалением и сигнальной передачей кальция — изменения, согласующиеся с большей хрупкостью клеток и прогрессированием сердечной недостаточности.
Микроскопическая архитектура под восстановлением
Высокое разрешение изображений позволило приблизиться к тонкой структуре кардиомиоцитов. В здоровой ткани мембрана клетки впячивается внутрь в регулярную сетку тоннелей — поперечно-осевую трубчатую сеть, которая помогает электрическим сигналам вызывать выброс кальция и сокращение. После инфаркта эта сеть в пограничной зоне становилась дезорганизованной и частично утраченной, особенно поперечные элементы. Однако оставшиеся трубочки были покрыты яркими кластерами дисферлина и окружены небольшими внутренними пузырьками мембраны, что указывает на активный ремонт и ремоделирование. В местах контакта клетка—клетка, где кардиомиоциты обмениваются электрическими импульсами и крепятся друг к другу, дисферлин также накапливался рядом с ключевыми белками контактов. Биохимические эксперименты показали, что дисферлин физически ассоциирован с этими партнерами в крупных комплексах, поддерживая идею о том, что он помогает сохранять и восстанавливать эти контактные участки под стрессом.
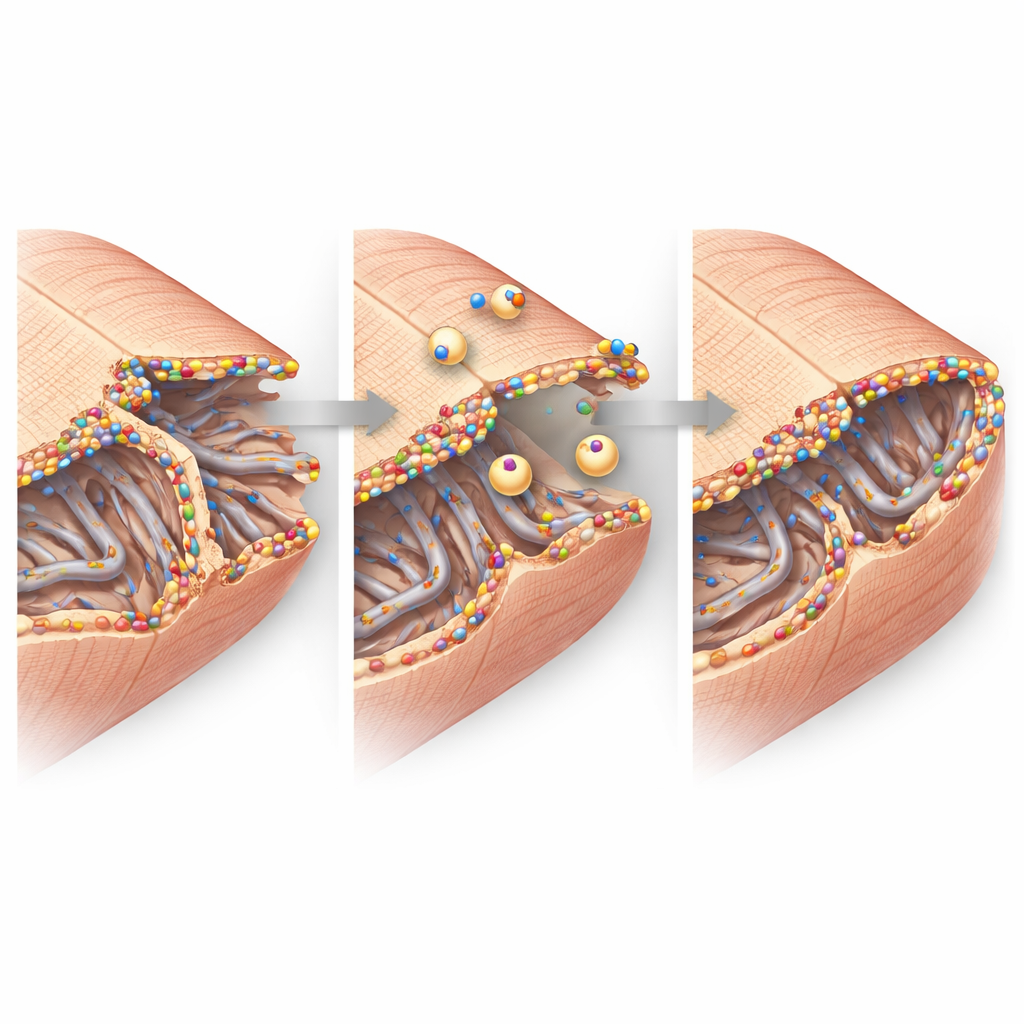
От молекул до функции сердца
Собрав все данные вместе, исследование рисует образ дисферлина как стража мембраны кардиомиоцита в уязвимой пограничной зоне после инфаркта. Когда он присутствует и увеличен в экспрессии, дисферлин образует кластеры на поврежденных трубчатых сетях и складках контактов клетка—клетка, привлекая везикулы ремонта и стабилизируя эти мельчайшие, но критически важные структуры. При его отсутствии эти наноопоры разрушаются легче, больше клеток теряется или функционирует неправильно, и сократительная способность сердца уменьшается. Для пациентов эта работа указывает на то, что усиление активности дисферлина или имитация его ремонтной функции в будущем может стать стратегией ограничения сердечной недостаточности после инфаркта за счет защиты тех самых мембран, которые позволяют сердечным клеткам биться согласованно.
Цитирование: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Ключевые слова: инфаркт миокарда, ремонт мембраны кардиомиоцита, дисферлин, профилактика сердечной недостаточности, ремоделирование нанообластей