Clear Sky Science · tr
Dysferlin miyokard enfarktüsünden sonra kardiyomiyositlerin membran nanodomainlerini stabilize eder
Kalp Hücrelerinin Acil Yama İhtiyacı Neden Var
Bir kişi kalp krizinden kurtulduğunda, asıl mücadele yeni başlar. Kalbin hasarlı bölgesi basit bir yara gibi iyileşmez; bunun yerine yaranın kenarındaki hayatta kalan kalp kası hücreleri yoğun mekanik stres altında kasılmaya devam etmelidir. Bu çalışma, az bilinen bir onarım proteini olan dysferlin’in, bu aşırı yüke maruz kalan hücreler için mikroskobik bir yama kiti gibi davranarak zarlarının bütünlüğünü korumasına ve kalbin pompalama gücünü sürdürmesine nasıl yardımcı olduğunu ortaya koyuyor.
Yaşam ile Skar Arasındaki Stresli Sınır
Kalp krizi sonrası, kalbin bir kısmına kan akışı engellenir, birçok hücre doğrudan ölür ve merkezi bir skar kalır. Bu ölü çekirdeği çevreleyen dar “sınır bölgesi” hâlâ yaşayan kalp kası hücrelerinden oluşur; bu hücreler düşük oksijen, iltihap ve her atışta güçlü gerilmeye maruz kalır. Bu koşullar hücrelerin dış zarını ve elektrik sinyalleri ile kalsiyum yönetimi için kritik yapıları barındıran karmaşık kıvrımlarını zorlar. Yazarlar, bu bölgedeki zarın küçük mimari özellikleri korunabilirse daha fazla kalp fonksiyonunun kurtarılabileceğini düşündüler.
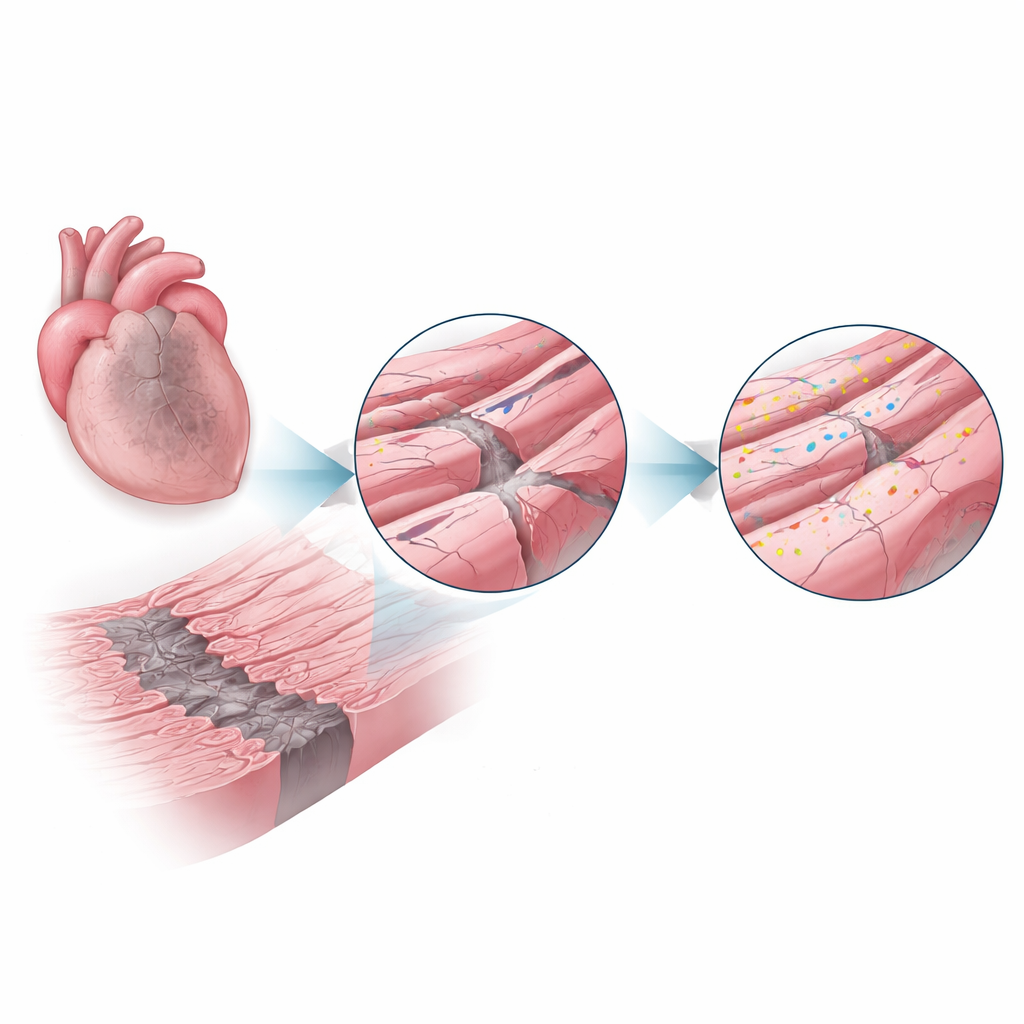
Onarım Proteini Sahneye Çıkıyor
Dysferlin, yokluğunda nadir kas hastalıklarına yol açan büyük bir proteindir; eksik olduğu durumlarda hasarlı kas lifleri membranlarını etkili şekilde onaramaz ve iskelet kası zayıflığı görülür. Bu çalışmada araştırmacılar dysferlin’in kalpte benzer bir koruyucu rol oynayıp oynamadığını sordular. Normal dysferlin’e sahip veya tamamen eksik olan farelerde kalp krizleri indükleyip kalpleri bir ve dört hafta sonra incelediler. Normal farelerde sınır bölgesindeki dysferlin düzeyleri sağlıklı kalplere göre iki kattan fazla arttı; bu da hücrelerin en yüksek stresin olduğu yerde bu onarım sistemini aktif halde çağırdığını gösteriyordu.
Dysferlin Eksik Olunca Ne Oluyor
Grup daha sonra dysferlinli ve dysferlini olmayan farelerdeki sonuçları karşılaştırdı. Proteini eksik olan hayvanlarda anlamlı şekilde daha büyük skarlar ve daha genişlemiş, zayıf sol ventriküller gelişti. Kalpleri her atımda daha az kan pompalıyordu; bu da hayatta kalan miyokardın daha fazlasının başarısız olduğunu gösteriyordu. Güçlü bir protein tarama tekniği araştırmacıların farklı kalp bölgelerindeki binlerce proteini kataloglamasına olanak tanıdı. Dysferlin eksikliğinin özellikle infarktüs ve sınır bölgelerinde bu protein profillerini yeniden şekillendirdiğini; hücre ölümü, iltihap ve kalsiyum sinyalleşmesi ile ilişkili yolakları değiştirdiğini buldular — bu değişiklikler daha kırılgan hücreler ve ilerleyici yetmezlikle uyumluydu.
Onarım Altındaki Mikroskobik Mimari
Yüksek çözünürlüklü görüntüleme kalp hücrelerinin ince yapısına yakından baktı. Sağlıklı dokuda hücre zarı, iletim sinyallerinin kalsiyum salınımını ve kasılmayı tetiklemesine yardımcı olan transvers–aksiyel tübül ağı adı verilen düzenli bir tünel ızgarası şeklinde içeri doğru çöküntüler oluşturur. Kalp krizi sonrası, sınır bölgesindeki bu ağ düzensizleşti ve özellikle transvers elemanları kısmen kayboldu. Buna rağmen kalan tübüller parlak dysferlin kümeleriyle kaplıydı ve çevrelerinde küçük iç membran kabarcıkları vardı; bu durum aktif onarım ve yeniden şekillenmeye işaret ediyordu. Hücre–hücre bağlantılarında, yani kalp hücrelerinin elektriksel impuls alışverişi yaptığı ve birbirine tuttuğu bölgelerde de dysferlin, ana bağlantı proteinlerinin yanında birikti. Biyokimyasal deneyler dysferlin’in bu ortaklarla büyük kompleksler halinde fiziksel olarak ilişki kurduğunu gösterdi; bu da stres altında bu temas noktalarını korumaya ve yeniden inşa etmeye yardımcı olduğu fikrini destekliyor.
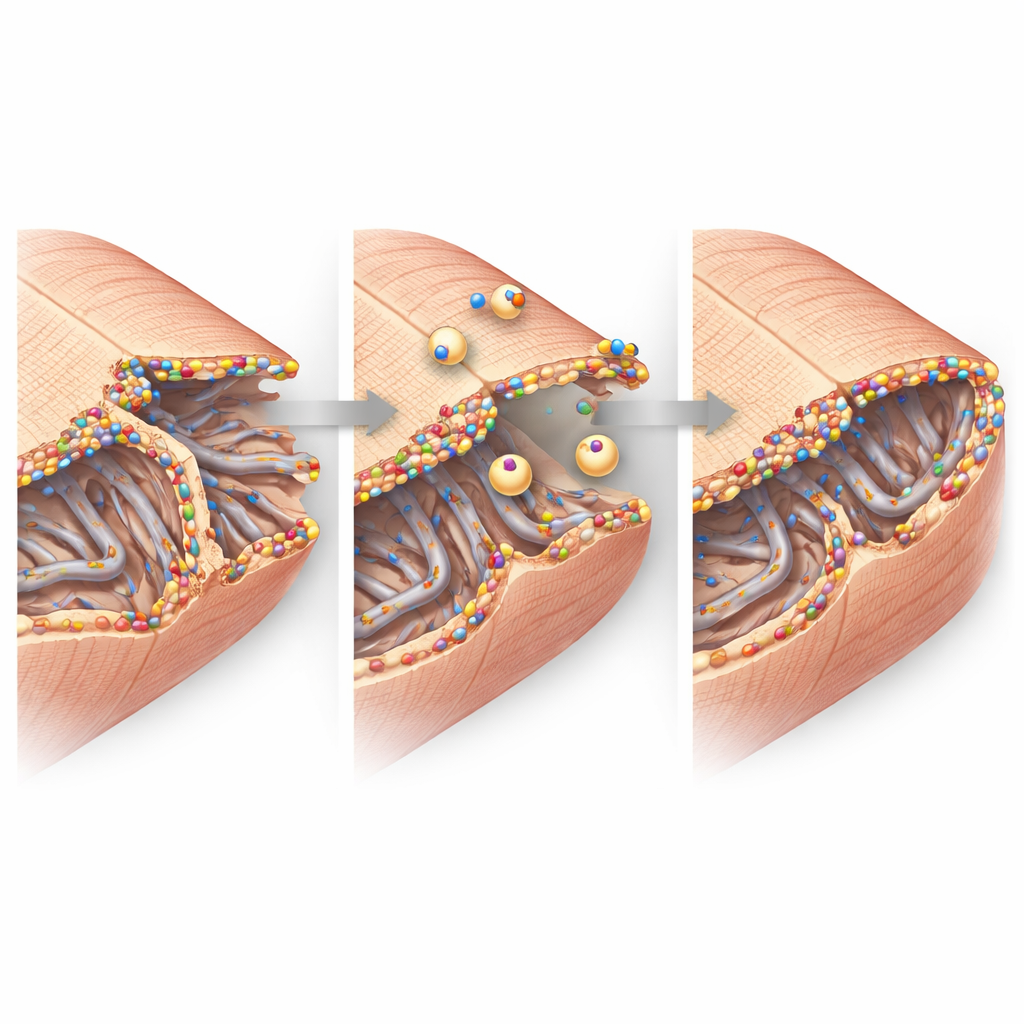
Moleküllerden Kalp Fonksiyonuna
Bu bulguları birleştirdiğinizde, çalışma dysferlin’i kalp krizinden sonra savunmasız sınır bölgesinde kalp hücresi zarının bir bekçisi olarak resmediyor. Bulunduğunda ve yukarı regüle edildiğinde dysferlin hasarlı tübüler ağlarda ve hücre–hücre bağlantılarının kıvrımlarında kümelenir, onarım veziküllerini çeker ve bu küçük ama kritik yapıları stabilize eder. Yokluğunda ise bu nanoskopik destekler daha kolay çöküyor, daha fazla hücre kaybediliyor veya işlevini yitiriyor ve kalbin pompalama gücü azalıyor. Hastalar için bu çalışma, dysferlin aktivitesinin artırılmasının veya onun onarım işlevini taklit etmenin bir gün kalp krizi sonrası kalp yetmezliğini sınırlama stratejisi haline gelebileceğini; kalp hücrelerinin uyum içinde atmasını sağlayan zarları koruyarak öne sürüyor.
Atıf: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Anahtar kelimeler: miyokard enfarktüsü, kardiyomiyosit membran onarımı, dysferlin, kalp yetmezliğinin önlenmesi, nanodomain yeniden şekillenmesi