Clear Sky Science · pt
Dysferlin estabiliza nanodomínios da membrana de cardiomiócitos após infarto do miocárdio
Por que as células cardíacas precisam de remendos de emergência
Quando alguém sobrevive a um ataque cardíaco, a verdadeira batalha está apenas começando. A região danificada do coração não cicatriza como um corte simples; em vez disso, as células musculares cardíacas sobreviventes na borda da cicatriz precisam continuar se contraindo sob intenso estresse mecânico. Este estudo revela como uma proteína de reparo pouco conhecida, a dysferlin, atua como um tipo de kit de remendo microscópico para essas células sobrecarregadas, ajudando suas membranas delicadas a se manterem unidas e preservando a capacidade de bombeamento do coração.
A fronteira estressante entre vida e cicatriz
Após um ataque cardíaco, o fluxo sanguíneo é bloqueado em parte do coração, matando muitas células diretamente e deixando uma cicatriz central. Ao redor desse núcleo morto existe uma estreita “zona de borda” de células musculares cardíacas ainda vivas que suportam baixo oxigênio, inflamação e poderosas distensões a cada batimento. Essas condições sobrecarregam a membrana externa das células e suas dobras intrincadas, que abrigam estruturas cruciais para sinais elétricos e controle do cálcio. Os autores suspeitaram que, se as pequenas características arquitetônicas da membrana pudessem ser protegidas nessa zona, mais função cardíaca poderia ser preservada.
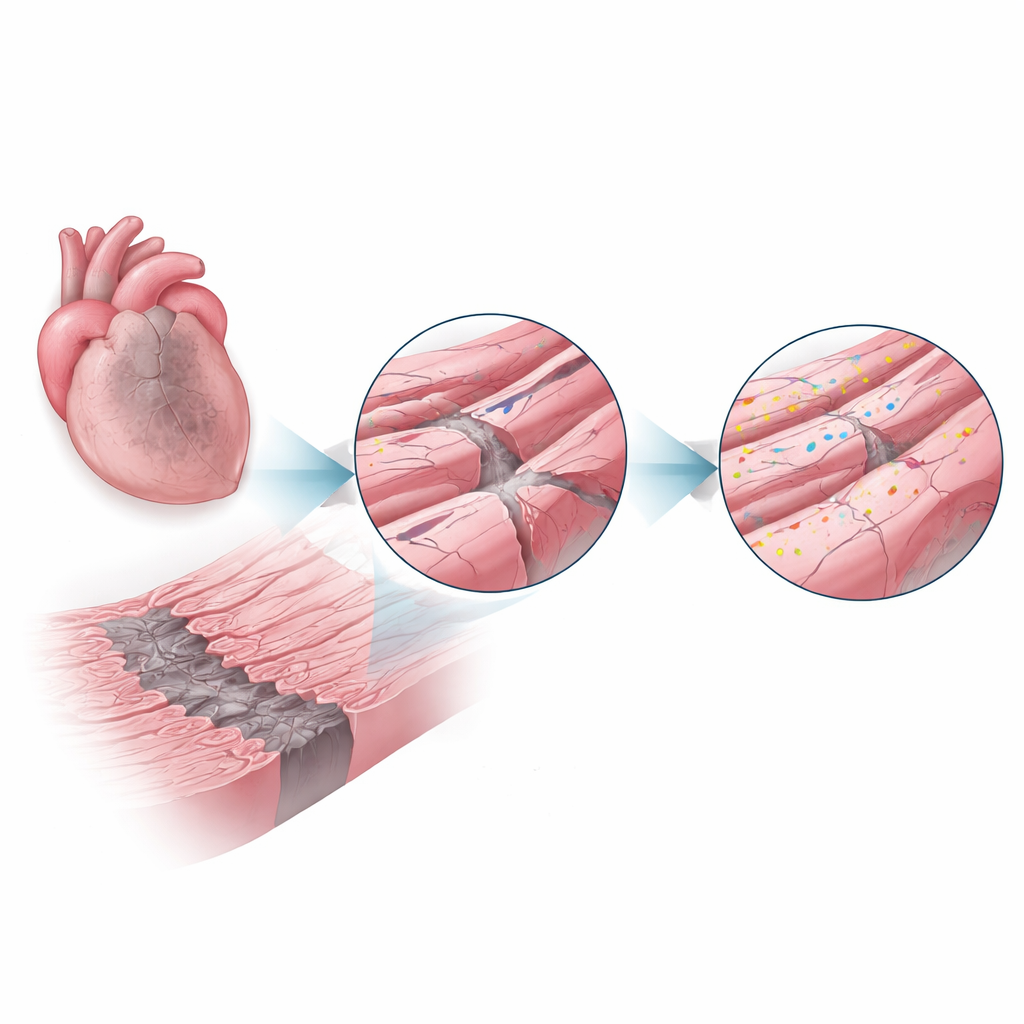
Uma proteína de reparo assume o centro do palco
A dysferlin é uma proteína grande conhecida por doenças musculares raras em que sua ausência leva ao enfraquecimento dos músculos esqueléticos, em parte porque fibras danificadas não conseguem reparar suas membranas de forma eficiente. Aqui, os pesquisadores perguntaram se a dysferlin desempenha um papel protetor semelhante no coração. Usando camundongos que tinham dysferlin normal ou a ausência completa dela, eles induziram ataques cardíacos e examinaram os corações uma e quatro semanas depois. Em camundongos normais, os níveis de dysferlin na zona de borda aumentaram para mais do que o dobro dos observados em corações saudáveis, sugerindo que as células estavam ativamente recrutando esse sistema de reparo onde o estresse era maior.
O que acontece quando a dysferlin está ausente
A equipe então comparou os desfechos em camundongos com e sem dysferlin. Animais sem a proteína desenvolveram cicatrizes significativamente maiores e ventrículos esquerdos mais dilatados e fracos. Seus corações bombeavam menos sangue a cada batida, indicando que mais do miocárdio sobrevivente havia falhado. Uma técnica poderosa de levantamento proteico permitiu aos pesquisadores catalogar milhares de proteínas em diferentes regiões do coração. Eles descobriram que a deficiência de dysferlin remodelou esses perfis proteicos, especialmente nas zonas de infarto e de borda, alterando vias ligadas à morte celular, inflamação e sinalização do cálcio — mudanças consistentes com células mais frágeis e falha progressiva.
Arquitetura microscópica em reparo
Imagens de alta resolução ampliaram a estrutura fina das células cardíacas. Em tecido saudável, a membrana celular se projeta para dentro em uma grade regular de túneis chamada rede transversa–axial de túbulos, que ajuda os sinais elétricos a desencadear liberação de cálcio e a contração. Após um ataque cardíaco, essa rede na zona de borda tornou-se desorganizada e parcialmente perdida, particularmente seus elementos transversais. Ainda assim, os túbulos remanescentes estavam revestidos por aglomerados brilhantes de dysferlin e circundados por pequenas bolsas internas de membrana, sugerindo reparo e remodelamento ativos. Nas junções célula–célula, onde as células cardíacas trocam impulsos elétricos e se aderem umas às outras, a dysferlin também se acumulou ao lado de proteínas de junção chave. Experimentos bioquímicos mostraram que a dysferlin se associa fisicamente a esses parceiros em complexos grandes, sustentando a ideia de que ela ajuda a manter e reconstruir esses locais de contato sob estresse.
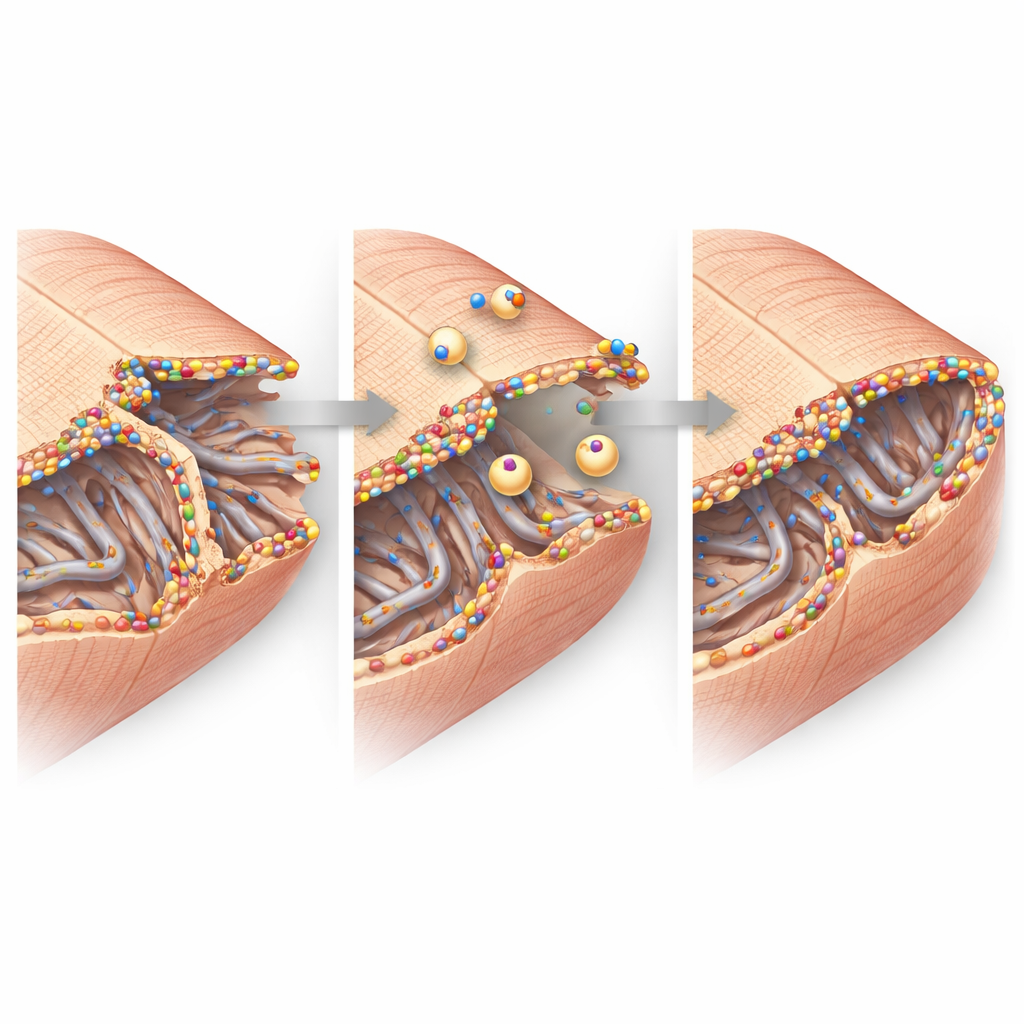
Das moléculas à função cardíaca
Ao reunir essas descobertas, o estudo desenha o retrato da dysferlin como guardiã da membrana das células cardíacas na vulnerável zona de borda após um ataque cardíaco. Quando presente e regulada para cima, a dysferlin se agrupa nas redes tubulares danificadas e nas dobras das junções célula–célula, atraindo vesículas de reparo e estabilizando essas estruturas minúsculas, porém críticas. Quando ausente, esses suportes nanoscópicos desmoronam mais facilmente, mais células são perdidas ou funcionam mal, e a potência de bombeamento do coração declina. Para pacientes, este trabalho sugere que aumentar a atividade da dysferlin ou imitar sua função de reparo pode, um dia, tornar-se uma estratégia para limitar a insuficiência cardíaca após um ataque cardíaco, protegendo as próprias membranas que permitem às células cardíacas baterem em uníssono.
Citação: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
Palavras-chave: infarto do miocárdio, reparo da membrana do cardiomiócito, dysferlin, prevenção da insuficiência cardíaca, remodelamento de nanodomínios