Clear Sky Science · he
דיספרלין מייצב ננו-דומיינים בממברנות תאי הלב לאחר אוטם שריר הלב
למה תאי הלב זקוקים לתפירה חירום
כאשר אדם שורד התקף לב, המאבק האמיתי רק מתחיל. האזור הפגוע בלב אינו נרפא כמו חתך פשוט; במקום זאת, תאי שריר הלב הניצולים בקצה הצלקת חייבים להמשיך להתכווץ תחת עומס מכני אינטנסיבי. המחקר הזה מגלה כיצד חלבון תיקון פחות מוכר, דיספרלין, פועל כסוג של ערכת תקון מיקרוסקופית לתאים המותשים הללו, מסייע לממברנות העדינות שלהם להחזיק מעמד ושומר על יכולת המשאבה של הלב.
הגבול המלחיץ בין חיים וצלקת
לאחר התקף לב, זרימת הדם נחסמת לחלק מהלב, מה שממית ישירות תאים רבים ומשאיר גרעין צלקתי מרכזי. מסביב לגרעין המת נמצאת "אזור הגבול" צר של תאי שריר לב שעדיין חיים ושחווים חוסר חמצן, דלקת ומתיחה עזה בכל פעימה. תנאים אלה מתישים את הממברנה החיצונית של התאים ואת הקיפולים המורכבים שלה, המארח מבנים חיוניים לאיתותים חשמליים ולנשיאת סידן. המחברים חשדו שאם ניתן יהיה להגן על התכונות האדריכליות הזעירות של הממברנה באזור זה, ניתן להציל יותר מפונקציית הלב.
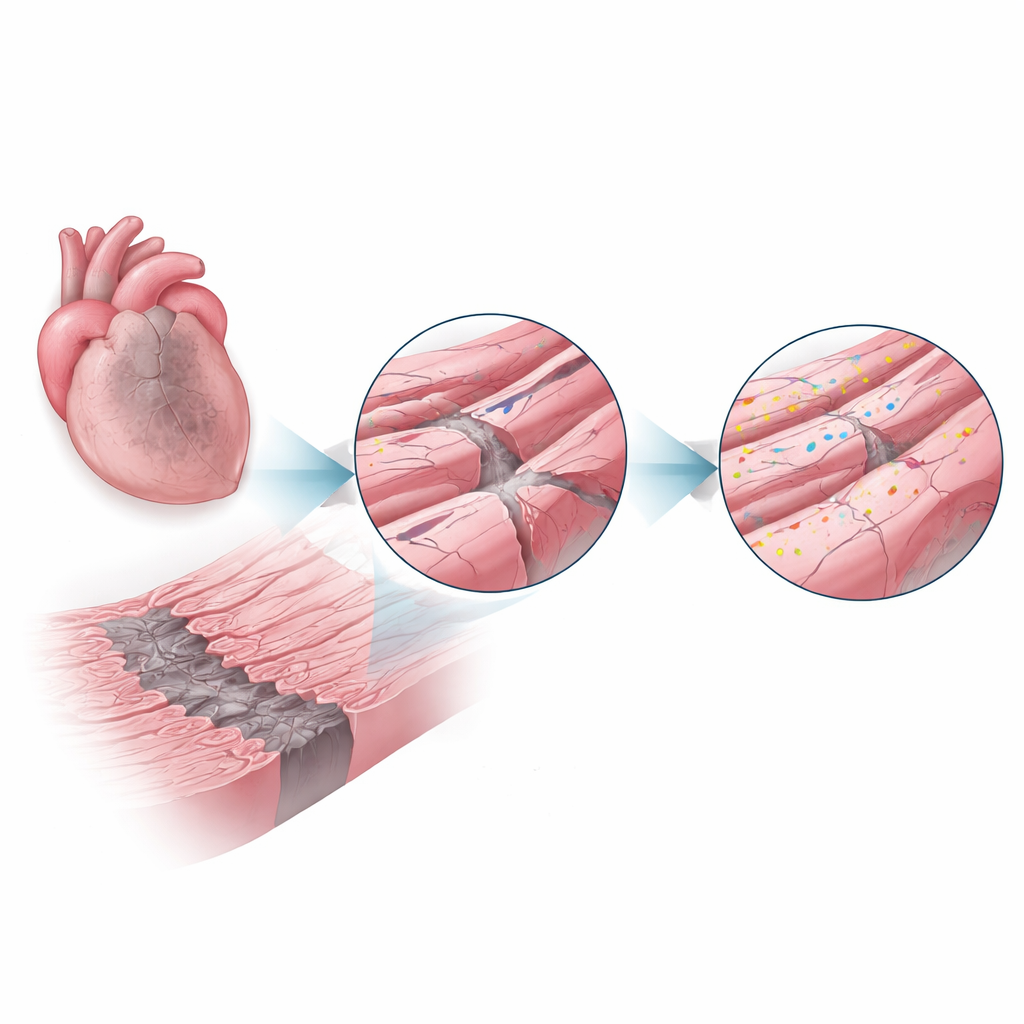
חלבון תיקון נכנס לתמונה
דיספרלין הוא חלבון גדול המוכר ממחלות שריר נדירות שבהן היעדרו מוביל לחולשה בשרירי השלד, חלקית כי סיבים פגועים אינם יכולים לתקן את ממברנותיהם ביעילות. כאן שאלו החוקרים האם דיספרלין ממלא תפקיד מגן דומה בלב. באמצעות עכברים שהחזיקו בדיספרלין תקין או שחסר לחלוטין, הם עוררו התקפי לב ובחנו את הלבבות שבוע ואחד וארבעה שבועות לאחר מכן. בעכברים התקינים רמת הדיספרלין באזור הגבול זינקה ליותר מפי שניים לעומת לבבות בריאים, מה שמרמז שהתאים קראו באופן פעיל למערכת התיקון הזו איפה שהעומס היה הגבוה ביותר.
מה קורה כשדיספרלין חסר
הצוות השווה לאחר מכן תוצאות בעכברים עם וללא דיספרלין. בעלי החיים שחסרו את החלבון פיתחו צלקות משמעותית גדולות יותר וחדר שמאל מורחב וחלש יותר. לבבותיהם שאבו פחות דם בכל פעימה, מה שמעיד שיותר מן המיוקרדיום הניצול נכשל. טכניקת סקר חלבונים עוצמתית אפשרה לחוקרים לרשום אלפי חלבונים באזורים שונים של הלב. הם מצאו שחסרון דיספרלין שינה את פרופילי החלבונים האלה, במיוחד באזורי האינפקט ואזור הגבול, ושינה מסלולים הקשורים למוות תאי, דלקת ואיתות סידן — שינויים התואמים לתאים שבריריים יותר ולכישלון מתקדם.
אדריכלות מיקרוסקופית תחת תיקון
הדמיה ברזולוציה גבוהה זום-אין למבנה העדין של תאי הלב. ברקמה בריאה, ממברנת התא שוקעת פנימה ברשת סדירה של מנהרות הנקראת רשת הצינורות הרוחבית–אקסיאלית, שמסייעת לאיתותים חשמליים לגרום לשחרור סידן ולהתכווצות. לאחר התקף לב, רשת זו באזור הגבול הפכה לאי-סדירה ואבד חלקית, במיוחד את האלמנטים הרוחביים שלה. ובכל זאת, הצינורות הנותרים היו מצופים באשכולות זוהרות של דיספרלין וסביבם בועיות פנימיות קטנות של ממברנה, מרמזות על תיקון ורמונטלינג פעיל. בצמתים בין-תאיים, שבהם תאי הלב מחליפים דחפים חשמליים ומתחברים זה לזה, דיספרלין גם הצטבר לצד חלבוני צורה מרכזיים. ניסויים ביוכימיים הראו שדיספרלין קשור פיזית לשותפים אלה במורכבים גדולים, תומך ברעיון שהוא מסייע לשמר ולבנות מחדש את אתרי המגע האלה תחת לחץ.
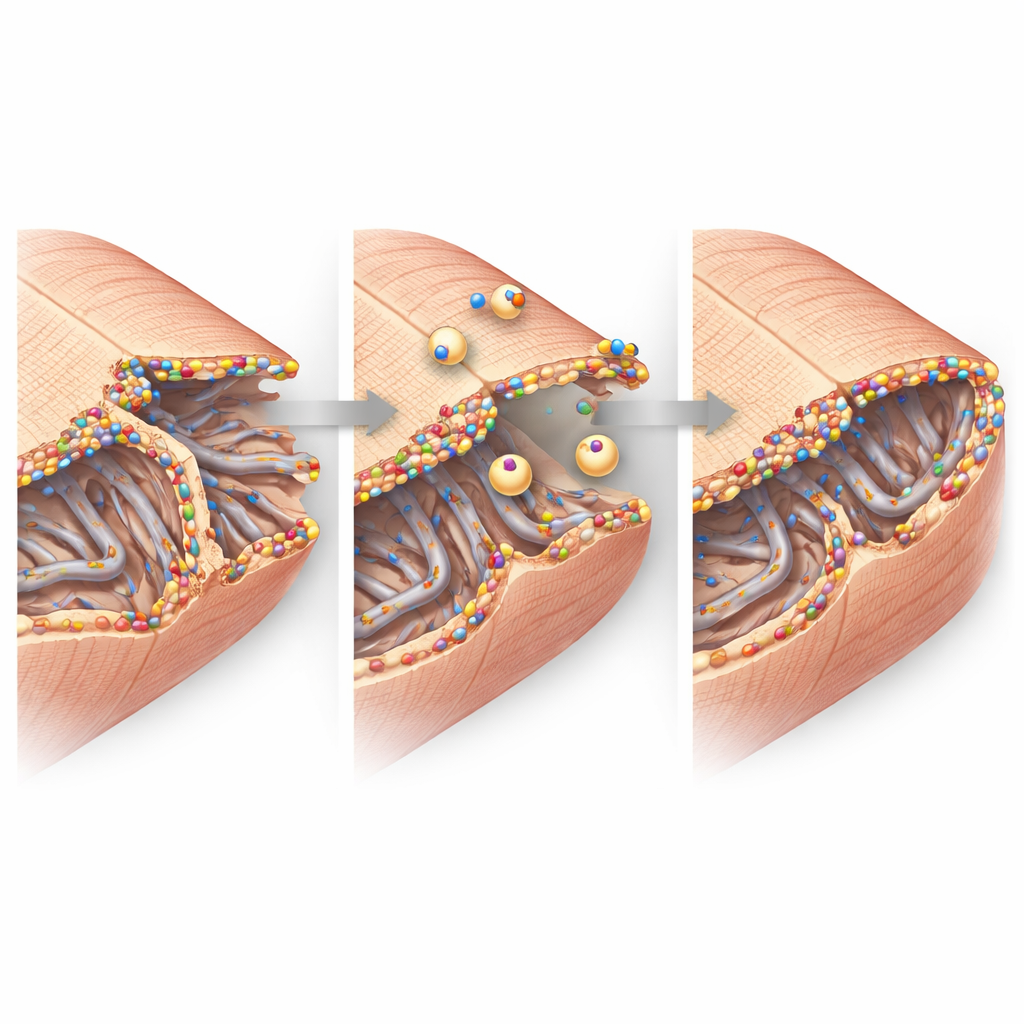
מותקנים מהמולקולות לתפקוד הלב
בהצמדת הממצאים הללו יחד, המחקר מצייר תמונה של דיספרלין כמגן של ממברנת תא הלב באזור הגבול הפגיע לאחר התקף לב. כשהוא נוכח ומוגבר, דיספרלין מצטבר ברשתות צינוריות פגועות ובקיפולי הצמתים בין תאים, מושך וזיקיות תיקון ומייצב את המבנים הקטנים אך הקריטיים האלה. כשהוא חסר, התמיכות הננומטריות האלה מתמוטטות ביתר קלות, יותר תאים הולכים לאיבוד או מתקלקלים, וכוח המשאבה של הלב פוחת. עבור מטופלים, עבודה זו מרמזת כי חיזוק פעילות הדיספרלין או חיקוי פונקציית התיקון שלו עשוי יום אחד להפוך לאסטרטגיה להגבלת אי־ספיקת לב לאחר התקף על ידי הגנה על הממברנות שמאפשרות לתאי הלב לפעום בסנכרון.
ציטוט: Wegener, J.B., Zühlke, Y., Fleischhacker, C. et al. Dysferlin stabilizes membrane nanodomains of cardiomyocytes after myocardial infarction. Sci Rep 16, 10488 (2026). https://doi.org/10.1038/s41598-026-42800-9
מילות מפתח: אוטם שריר הלב, תיקון ממברנת קרדיומיוציטים, דיספרלין, מניעת אי-ספיקת לב, רמונטלינג של ננו-דומיינים