Clear Sky Science · zh
使用抗生素抗性生长平板探索大肠埃希氏菌 MG1655 中氨基糖苷类耐药性的分子机制
为什么快速变化的病原体关系到每个人
抗生素拯救了无数生命,但细菌正在稳步学会如何躲避它们。本文探讨了普通肠道细菌大肠埃希氏菌如何在短短几天内进化出对常用抗生素庆大霉素的耐药性。研究者通过在一种专门设计的生长平板上观察耐药性的出现,然后解析细菌的 DNA 和分子结构,揭示了这些微生物如何智胜药物的新细节。他们的发现有助于解释耐药为何能如此迅速地出现,并指向可用于预测哪些治疗可能失效的工具。
用于实时观察进化的新型平板
为了让耐药性在出现时可见,团队构建了所谓的抗生素抗性生长平板(ARGP)。想象一个彼得里皿被分成三个同心圆带:中心无药物、中间带为中等剂量、最外圈为非常高的剂量。研究者在中心播种一种标准的对药物敏感的大肠埃希氏菌株,让细菌在一层薄的半固体介质中向外游动。随着微生物扩散,它们遇到的庆大霉素浓度越来越高。大多数在区域之间的边界被阻止,但偶尔会有微小的侧芽设法穿过并继续生长。仅在两到三天内,某些谱系就能在比抑制原始菌株所需最低浓度高十倍的抗生素浓度下繁衍生存。 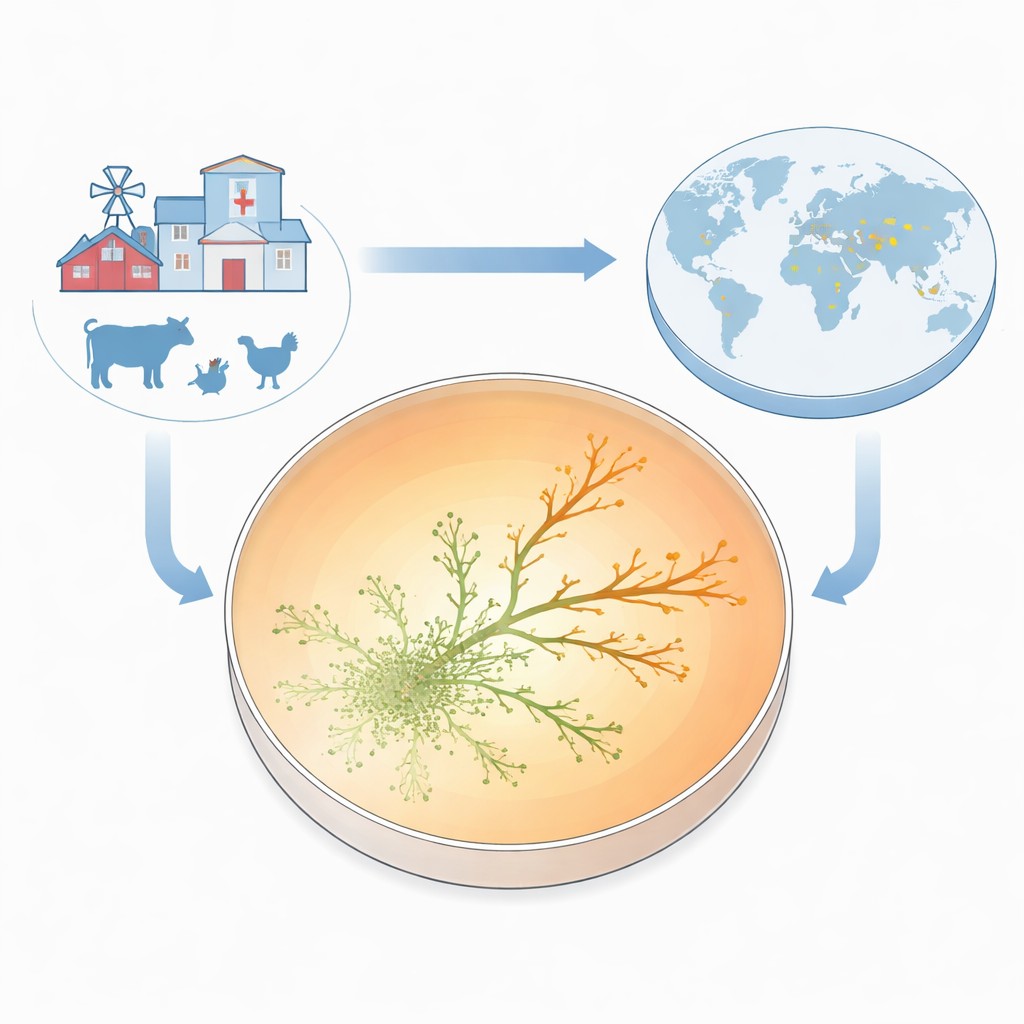
追踪幸存者背后的遗传改变
看到耐药菌落出现只是开始。科学家们收集了这些顽强外生长体的细胞,并将它们的完整 DNA 序列与原始菌株进行比较。在仔细过滤掉伪影和污染片段后,他们将注意力集中在已知参与细胞内蛋白质合成的基因变化上。研究发现有些突变出现在构建细胞蛋白质合成机器的基因部分:多拷贝的 16S 核糖体 RNA 基因以及名为 fusA 的基因,该基因编码一个关键的辅助蛋白 EF-G。这两个靶点的出现合情合理,因为庆大霉素通过结合细菌核糖体起作用,核糖体负责读取遗传指令并缝合新的蛋白质。任何在不完全破坏该机器的前提下改变其功能的微小调整,都有可能削弱药物的效果。
单一铰链变化如何削弱药效
最显著的改变是 fusA 基因中的一个单字母变化,使 EF-G 蛋白第 610 位的氨基酸由脯氨酸被置换为苏氨酸。EF-G 像一只可移动的臂,帮助移动转运 RNA 和信使 RNA 通过核糖体,使每个新蛋白得以合成。借助 EF-G 三维结构的计算模型,研究团队显示该位置位于 EF-G 两个结构域之间的铰链处,蛋白在推动核糖体前进时在此弯曲和旋转。该铰链处的脯氨酸在许多相关细菌中高度保守,提示其重要性。被替换后,EF-G 的整体柔韧性和紧凑性发生变化,微妙地重塑了该蛋白与核糖体的配合方式。将庆大霉素作用于核糖体–EF-G 复合体的对接模拟表明,这种微小的结构移动改变了药物结合区的几何形态。在突变形式中,庆大霉素不再能将核糖体困在通常被阻断运动的脆弱阶段。
RNA 结构的小变动带来大后果
突变还出现在构成核糖体小亚基的多个 16S rRNA 基因拷贝中的两个拷贝上。通过将这些改变映射到已知的 RNA 结构上,作者发现所有突变都聚集在“5′ 体”区域,靠近庆大霉素和附近核糖体蛋白通常结合的位置。详细的计算预测显示总体 RNA 折叠大体保留,但突变碱基附近的局部环和茎发生了微妙重排。这些小的结构调整足以改变 RNA 与核糖体蛋白和药物的相互作用,可能将关键碱基轻微移开,使庆大霉素难以实现紧密结合。与 EF-G 铰链突变共同作用时,结果是即便在高药物浓度下,核糖体仍能继续读取遗传指令。 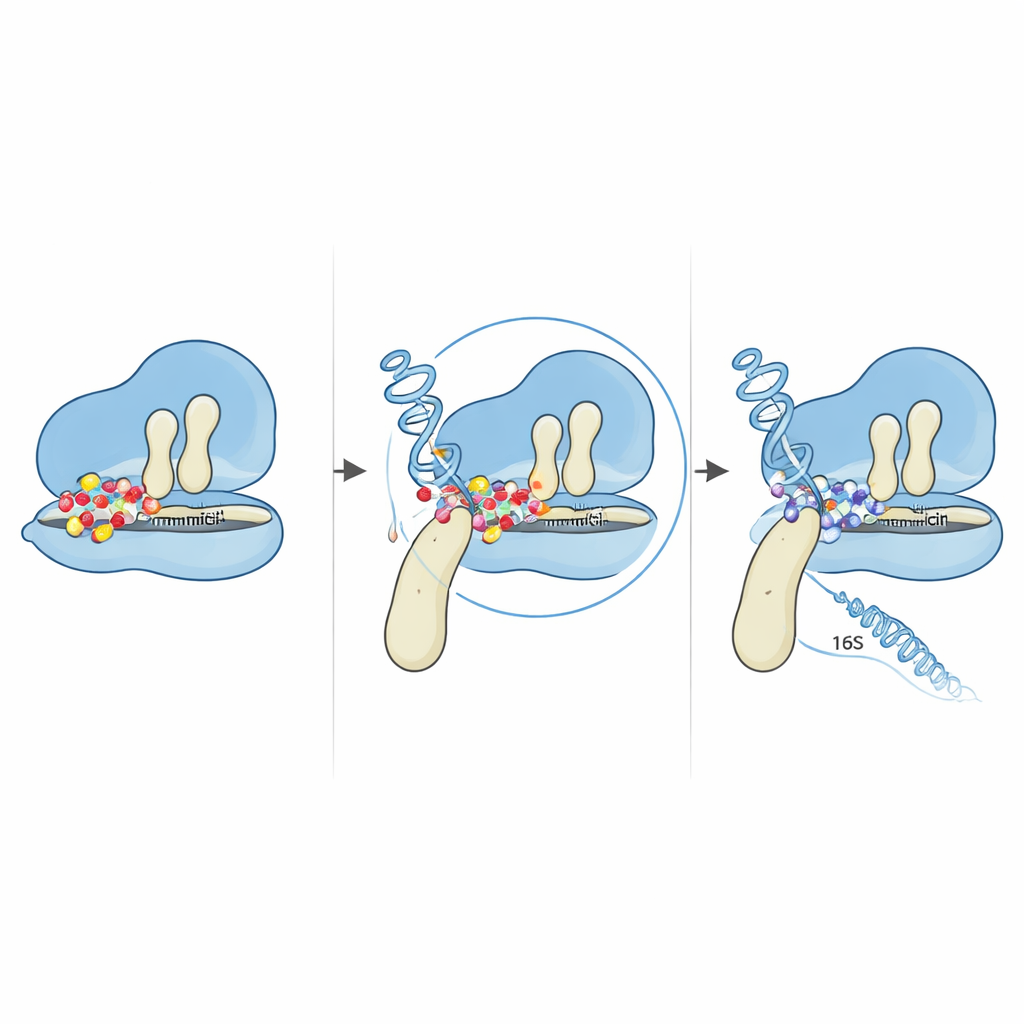
这对应对耐药性意味着什么
综合来看,这项工作表明,大肠埃希氏菌能够通过同时修改核糖体 RNA 上的药物停靠位点和驱动翻译的蛋白引擎的活动部件,迅速组装起对庆大霉素的高度特异性防御。这些改变并未摧毁蛋白质合成工厂;它们对其进行微调,足以使抗生素无法再卡住机器。ARGP 系统提供了一种简单、可视化的方式,在可控条件下产生并研究此类耐药路径,并可适配到其他药物和病原体。对非专业读者而言,关键讯息是耐药并非模糊、缓慢的趋势——它可以通过精确的分子修改迅速出现。详细理解这些修改对我们设计新抗生素和治疗策略、保持领先于进化中的细菌至关重要。
引用: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
关键词: 抗生素耐药性, 庆大霉素, 大肠埃希氏菌, 核糖体, 实验进化