Clear Sky Science · pl
Badanie molekularnych mechanizmów oporności na aminoglikozydy w Escherichia coli MG1655 za pomocą płytki wzrostu do badania oporności na antybiotyki
Dlaczego szybko zmieniające się drobnoustroje dotyczą nas wszystkich
Antybiotyki uratowały niezliczone życie, ale bakterie stopniowo uczą się ich unikać. W artykule zbadano, jak zwykła bakteria jelitowa Escherichia coli może w ciągu zaledwie kilku dni wyewoluować oporność na powszechnie stosowany antybiotyk gentamycynę. Obserwując pojawianie się oporności na specjalnie zaprojektowanej płytce wzrostu, a następnie analizując DNA i struktury molekularne bakterii, badacze odkrywają nowe szczegóły dotyczące sposobów, w jakie te mikroby przechytrzają lek. Wyniki pomagają wyjaśnić, dlaczego oporność może pojawiać się tak szybko i wskazują narzędzia, które mogłyby przewidywać, które terapie prawdopodobnie zawiodą.
Nowa płytka do obserwowania ewolucji w działaniu
Aby uczynić oporność widoczną w momencie jej pojawiania się, zespół zbudował to, co nazwał Płytką Wzrostu Oporności na Antybiotyk (ARGP). Wyobraź sobie płytkę Petriego podzieloną na trzy koncentryczne pasy: bez leku w centrum, umiarkowana dawka w środkowym pierścieniu i bardzo wysoka dawka na krawędzi. W centrum zaszczepiono standardowy, wrażliwy szczep E. coli i pozwolono bakteriom rozpraszać się na zewnątrz przez cienką, półstałą warstwę. W miarę rozprzestrzeniania się mikroby napotykały coraz wyższe stężenia gentamycyny. Większość zatrzymywała się na granicach między strefami, ale od czasu do czasu drobne odgałęzienia przechodziły do następnego pierścienia i nadal rosły. W ciągu zaledwie dwóch‑trzech dni niektóre linie rozwijały się w stężeniach antybiotyku dziesięć razy wyższych niż minimalne stężenie hamujące pierwotny szczep. 
Śledzenie zmian genetycznych stojących za przetrwaniem
Pojawienie się kolonii odpornych było dopiero początkiem. Naukowcy pobrali komórki z tych odpornych odrostów i porównali ich pełne sekwencje DNA z sekwencją szczepu wyjściowego. Po starannym odfiltrowaniu artefaktów i fragmentów zanieczyszczających skupili się na zmianach w genach znanych z udziału w produkcji białek w komórce. Odkryli mutacje w częściach kodu genetycznego budujących maszynerię do wytwarzania białek: w kilku kopiach genu 16S rRNA oraz w genie fusA, który koduje kluczowe białko pomocnicze znane jako EF‑G. Oba cele są logiczne, ponieważ gentamycyna działa, przyczepiając się do bakteryjnego rybosomu — kompleksu odczytującego instrukcje genetyczne i łączącego nowe białka. Każda zmiana, która modyfikuje tę maszynerię bez jej całkowitego rozbicia, może osłabić działanie leku.
Jak pojedyncza zmiana „zawiasu" osłabia lek
Najbardziej znacząca zmiana to jednopunktowa zamiana w genie fusA, która wymienia jedną aminokwas — prolinę — na inną — treoninę — w pozycji 610 białka EF‑G. EF‑G działa jak ruchome ramię pomagające przesuwać tRNA i mRNA przez rybosom w trakcie syntezy białka. Korzystając z komputerowych modeli trójwymiarowej struktury EF‑G, zespół wykazał, że ta pozycja znajduje się w zawiasie między dwoma domenami EF‑G, gdzie białko zgina się i obraca, popychając rybosom do przodu. Prolina w tym miejscu wydaje się być wyjątkowo konserwowana wśród wielu spokrewnionych bakterii, co sugeruje jej istotną rolę. Gdy zostaje zastąpiona, zmienia się ogólna elastyczność i zwartość EF‑G, subtelnie przekształcając dopasowanie białka do rybosomu. Symulacje dokowania, w których wirtualnie umieszczono gentamycynę na kompleksach rybosom–EF‑G, sugerują, że ta drobna zmiana strukturalna modyfikuje geometrię miejsca wiązania leku. W zmutowanej formie gentamycyna nie jest już w stanie unieruchomić rybosomu w podatnym etapie, gdzie normalnie blokuje ruch.
Małe przesunięcia w strukturze RNA o dużych konsekwencjach
Pojawiły się także mutacje w dwóch z wielu kopii genu 16S rRNA, które tworzą mniejszą podjednostkę rybosomu. Mapując te zmiany na znanych strukturach RNA, autorzy stwierdzili, że wszystkie skupiają się w regionie „5′ body”, blisko miejsca, gdzie zwykle przyczepiają się gentamycyna i sąsiednie białko rybosomalne. Szczegółowe przewidywania komputerowe wykazały, że ogólne składanie RNA zostało w dużej mierze zachowane, ale lokalne pętle i stabilne pary zasad w pobliżu zmutowanych nukleotydów zostały subtelnie przekształcone. Te drobne korekty strukturalne wystarczają, by zmienić interakcje RNA zarówno z białkami rybosomalnymi, jak i z lekiem, potencjalnie przesuwając krytyczne zasady z precyzyjnych pozycji, których gentamycyna potrzebuje do silnego wiązania. W połączeniu z mutacją zawiasu w EF‑G daje to rybosom, który nadal odczytuje instrukcje genetyczne nawet w obecności wysokich stężeń leku. 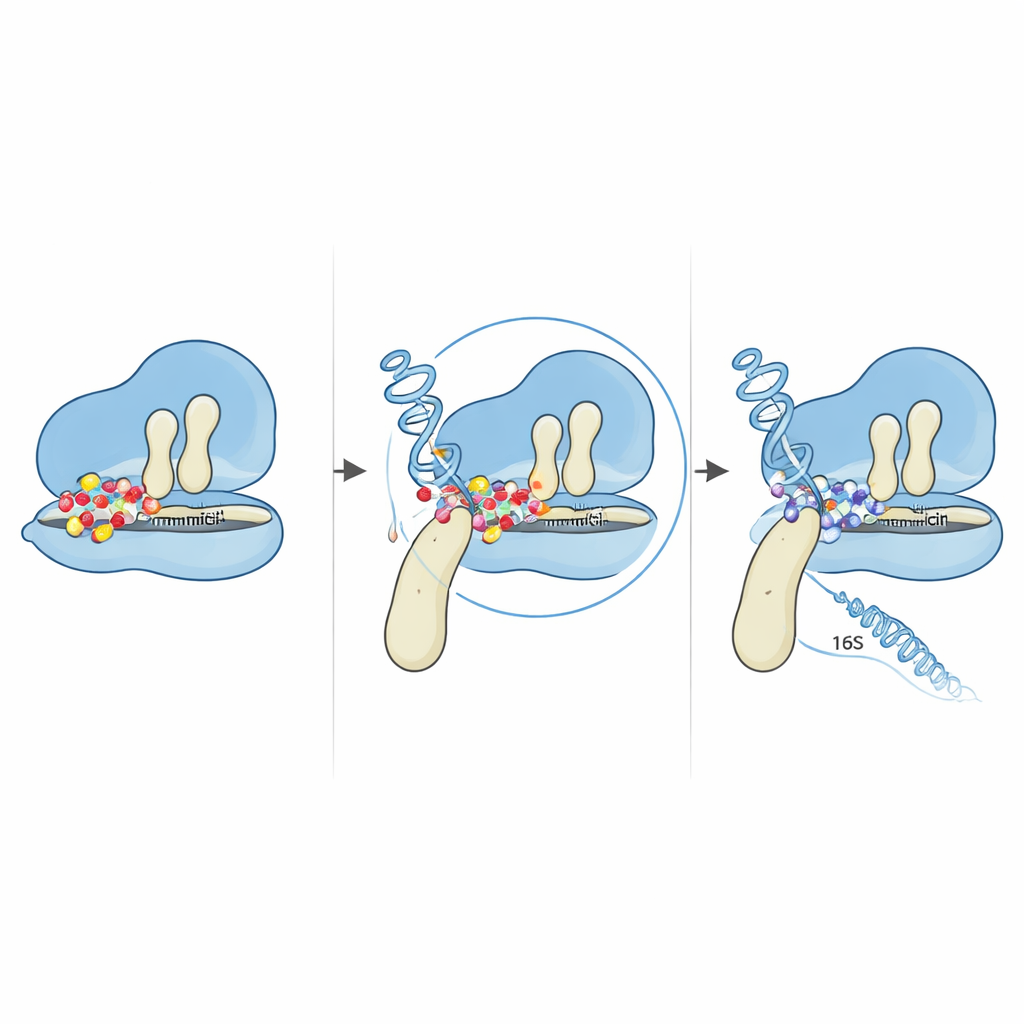
Co to oznacza dla walki z opornością
W całości badanie pokazuje, że E. coli może szybko złożyć wysoce specyficzną obronę przeciwko gentamycynie, modyfikując zarówno miejsce dokowania leku na rybosomalnym RNA, jak i ruchomy element białkowego mechanizmu napędzającego translację. Zmiany te nie niszczą fabryki białek; dostrajają ją na tyle, by antybiotyk nie mógł już zablokować jej pracy. System ARGP dostarcza prostego, wizualnego sposobu generowania i badania takich ścieżek oporności w kontrolowanych warunkach i można go dostosować do innych leków i patogenów. Dla osób niebędących specjalistami kluczowy przekaz jest taki, że oporność nie jest mglistym, powolnym trendem — może pojawić się szybko dzięki precyzyjnym edycjom molekularnym. Zrozumienie tych zmian szczegółowo jest niezbędne, jeśli chcemy projektować nowe antybiotyki i strategie leczenia, które pozostaną krok przed ewoluującymi bakteriami.
Cytowanie: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Słowa kluczowe: oporność na antybiotyki, gentamycyna, Escherichia coli, rybosom, ewolucja eksperymentalna