Clear Sky Science · pt
Explorando mecanismos moleculares de resistência a aminoglicosídeos em Escherichia coli MG1655 usando a placa de crescimento para resistência a antibióticos
Por que germes que mudam rápido importam para todos
Antibióticos salvaram inúmeras vidas, mas as bactérias vêm aprendendo, de forma contínua, a escapar deles. Este artigo investiga como uma bactéria comum do intestino, Escherichia coli, pode evoluir resistência a um antibiótico amplamente usado, a gentamicina, em apenas alguns dias. Ao observar o surgimento da resistência em uma placa de crescimento especialmente projetada e, em seguida, sondar o DNA e as estruturas moleculares das bactérias, os pesquisadores revelam novos detalhes sobre como esses micróbios driblam o medicamento. Seus achados ajudam a explicar por que a resistência pode surgir tão rapidamente e apontam para ferramentas que poderiam prever quais tratamentos têm maior probabilidade de falhar.
Uma nova placa para ver a evolução em ação
Para tornar a resistência visível à medida que surgia, a equipe construiu o que chama de Placa de Crescimento para Resistência a Antibióticos (ARGP). Imagine uma placa de Petri dividida em três faixas circulares: sem droga no centro, uma dose moderada no anel do meio e uma dose muito alta na borda externa. Eles semearam o centro com uma cepa padrão sensível ao medicamento e permitiram que as bactérias se movessem para fora através de uma camada fina e semi‑sólida. À medida que os micróbios se espalhavam, encontravam níveis cada vez maiores de gentamicina. A maioria foi detida nas fronteiras entre as zonas, mas ocasionalmente pequenos brotos conseguiram cruzar para o anel seguinte e continuar crescendo. Em apenas dois a três dias, algumas linhagens prosperavam em concentrações de antibiótico dez vezes maiores do que a mínima necessária para impedir a cepa original. 
Acompanhando as mudanças genéticas por trás da sobrevivência
Ver colônias resistentes aparecer foi apenas o começo. Os cientistas coletaram células desses brotos resistentes e compararam seu genoma completo com o da cepa original. Após filtrar cuidadosamente artefatos e fragmentos contaminantes, concentraram‑se em alterações em genes conhecidos por participarem da produção de proteínas dentro da célula. Encontraram mutações em partes do código genético que constroem a maquinaria de fabricação de proteínas: várias cópias do gene do RNA ribossômico 16S e um gene chamado fusA, que codifica uma proteína auxiliar-chave conhecida como EF‑G. Ambos os alvos fazem sentido porque a gentamicina atua ligando‑se ao ribossomo bacteriano, o complexo que lê instruções genéticas e monta novas proteínas. Qualquer alteração que modifique essa maquinaria sem destruí‑la por completo tem potencial para atenuar o efeito do medicamento.
Como uma única mudança na dobradiça enfraquece o medicamento
A alteração mais marcante foi uma mudança de uma letra no gene fusA que troca um aminoácido — prolina — por outro — treonina — na posição 610 da proteína EF‑G. A EF‑G atua como um braço móvel que ajuda a deslocar RNAs de transferência e o RNA mensageiro através do ribossomo enquanto cada nova proteína é sintetizada. Usando modelos computacionais da estrutura tridimensional da EF‑G, a equipe mostrou que essa posição fica em uma dobradiça entre dois domínios da EF‑G, local em que a proteína se dobra e gira ao empurrar o ribossomo. A prolina nessa dobradiça parece ser incomumente conservada entre muitas bactérias relacionadas, sugerindo sua importância. Quando é substituída, a flexibilidade e a compacidade gerais da EF‑G mudam, remodelando sutilmente como a proteína se acomoda no ribossomo. Simulações de encaixe que posicionam virtualmente a gentamicina nos complexos ribossomo–EF‑G sugerem que esse pequeno deslocamento estrutural altera a geometria da região de ligação do medicamento. Na forma mutada, a gentamicina não consegue mais prender o ribossomo no estágio vulnerável onde normalmente bloqueia o movimento.
Pequenas alterações na estrutura do RNA com grandes consequências
Também surgiram mutações em duas das múltiplas cópias do gene 16S rRNA que ajudam a formar a metade menor do ribossomo. Ao mapear essas alterações em estruturas de RNA conhecidas, os autores descobriram que todas se concentraram na região do “corpo 5′”, perto de onde a gentamicina e uma proteína ribossomal adjacente normalmente se ligam. Previsões computacionais detalhadas mostraram que a dobra geral do RNA foi em grande parte preservada, mas laços e hastes locais próximos às bases mutadas foram sutilmente rearranjados. Esses pequenos ajustes estruturais são suficientes para alterar como o RNA interage tanto com proteínas ribossomais quanto com o medicamento, potencialmente deslocando bases críticas das posições precisas que a gentamicina precisa para uma ligação firme. Quando combinadas com a mutação na dobradiça da EF‑G, o resultado é um ribossomo que continua a ler instruções genéticas mesmo na presença de altos níveis do antibiótico. 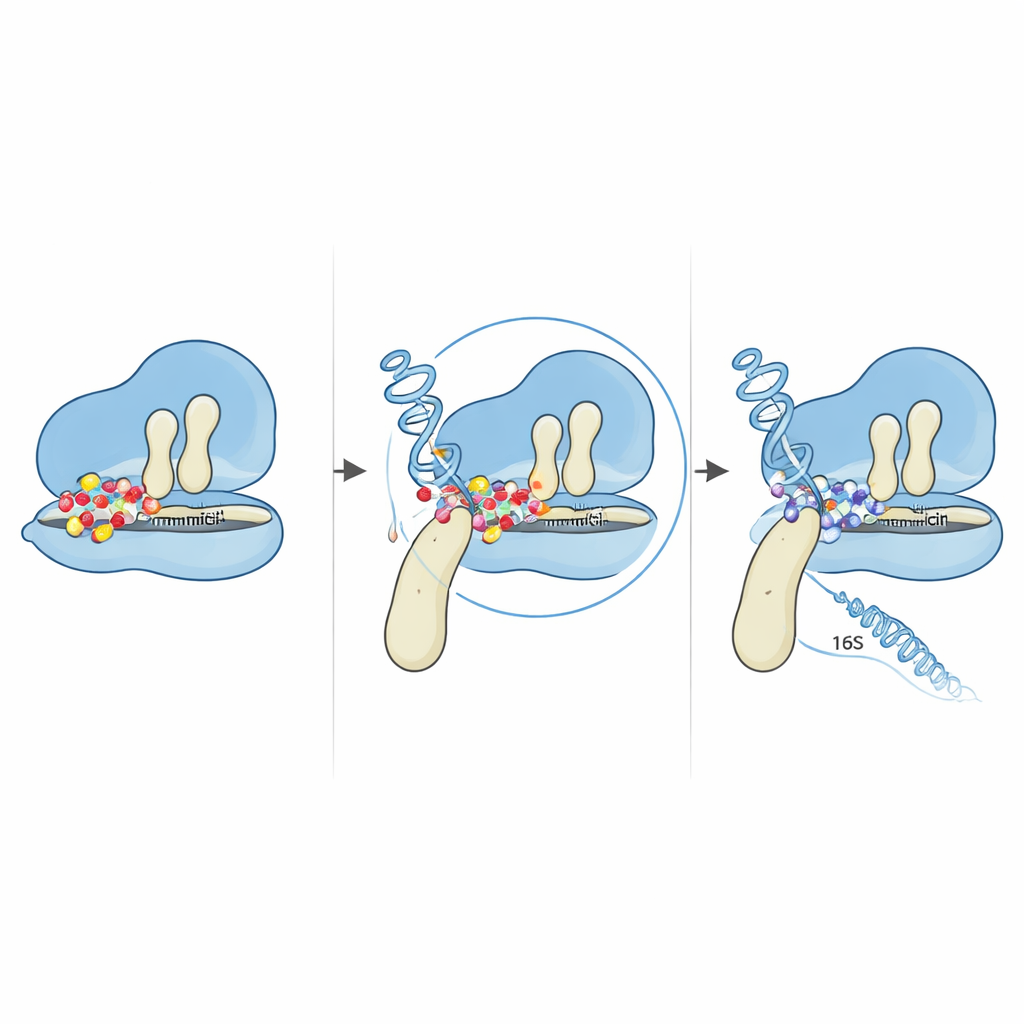
O que isso significa para enfrentar a resistência
De forma conjunta, o trabalho mostra que E. coli pode montar rapidamente uma defesa altamente específica contra a gentamicina ao modificar tanto o sítio de ancoragem da droga no RNA ribossomal quanto uma parte móvel do motor proteico que conduz a tradução. Essas mudanças não destroem a fábrica de proteínas; elas a ajustam o suficiente para que o antibiótico não consiga mais emperrar o funcionamento. O sistema ARGP fornece uma forma simples e visual de gerar e estudar tais caminhos de resistência em condições controladas, e pode ser adaptado para outros medicamentos e patógenos. Para não especialistas, a mensagem-chave é que a resistência não é uma tendência vaga e lenta — ela pode surgir rapidamente por meio de edições moleculares precisas. Compreender essas edições em detalhe é essencial se quisermos projetar novos antibióticos e estratégias de tratamento que fiquem um passo à frente das bactérias em evolução.
Citação: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Palavras-chave: resistência a antibióticos, gentamicina, Escherichia coli, ribossomo, evolução experimental