Clear Sky Science · it
Esplorare i meccanismi molecolari della resistenza agli aminoglicosidi in Escherichia coli MG1655 usando la piastra di crescita per resistenza agli antibiotici
Perché i germi che cambiano rapidamente contano per tutti
Gli antibiotici hanno salvato innumerevoli vite, ma i batteri imparano costantemente a sfuggirvi. Questo studio esplora come batteri intestinali comuni, Escherichia coli, possano evolvere resistenza a un antibiotico ampiamente usato, la gentamicina, in appena pochi giorni. Monitorando l’emergere della resistenza su una piastra di crescita appositamente progettata e analizzando poi il DNA e le strutture molecolari dei batteri, i ricercatori rivelano nuovi dettagli su come questi microrganismi aggirino il farmaco. I risultati aiutano a spiegare perché la resistenza può comparire così rapidamente e indicano strumenti che potrebbero prevedere quali terapie sono destinate a fallire.
Una nuova piastra per osservare l’evoluzione in azione
Per rendere visibile la resistenza mentre emergeva, il gruppo ha costruito quella che chiamano Piastra di Crescita per Resistenza agli Antibiotici (ARGP). Immaginate una petri divisa in tre anelli circolari: nessun farmaco al centro, una dose moderata nell’anello medio e una dose molto alta lungo il bordo esterno. Hanno inoculato il centro con un ceppo standard sensibile al farmaco e lasciato che i batteri migrassero verso l’esterno attraverso uno strato sottile semi-solido. Mentre i microrganismi si diffondevano incontravano concentrazioni di gentamicina via via maggiori. La maggior parte si arrestava ai confini tra le zone, ma di tanto in tanto minuscole propaggini riuscivano a oltrepassare l’anello successivo e a continuare a crescere. In appena due‑tre giorni, alcune linee erano fiorenti a concentrazioni di antibiotico dieci volte superiori alla minima necessaria per fermare il ceppo originale. 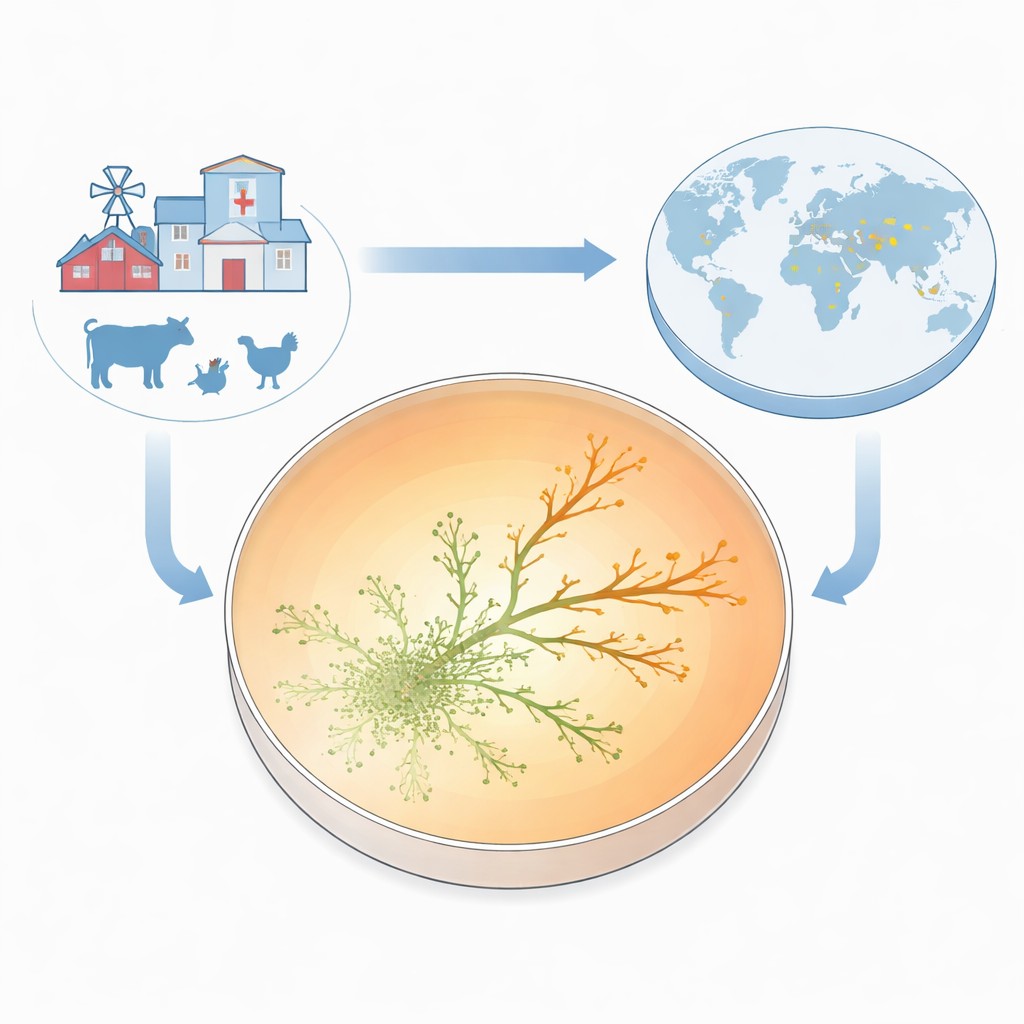
Tracciare i cambiamenti genetici alla base della sopravvivenza
Vedere apparire colonie resistenti è stato solo l’inizio. Gli scienziati hanno raccolto cellule da questi rigogliosi germogli e confrontato la loro sequenza completa del DNA con quella del ceppo originale. Dopo aver accuratamente filtrato artefatti e frammenti contaminanti, si sono concentrati su cambiamenti in geni noti per essere coinvolti nella produzione proteica all’interno della cellula. Hanno riscontrato mutazioni in parti del codice genetico che costruiscono la macchina di sintesi proteica: diverse copie del gene 16S rRNA e un gene chiamato fusA, che codifica per una proteina ausiliaria chiave nota come EF‑G. Entrambi i bersagli sono coerenti con il meccanismo d’azione della gentamicina, che si lega al ribosoma batterico — il complesso che legge le istruzioni genetiche e concatena le nuove proteine. Qualsiasi modifica che alteri questa macchina senza comprometterla completamente ha il potenziale di attenuare l’effetto del farmaco.
Come un singolo cambiamento nella cerniera indebolisce il farmaco
La variazione più sorprendente è stata un cambiamento di una singola lettera nel gene fusA che sostituisce un amminoacido — prolina — con un altro — treonina — nella posizione 610 della proteina EF‑G. EF‑G funzione come un braccio mobile che aiuta a spostare gli RNA di trasferimento e l’RNA messaggero attraverso il ribosoma durante la sintesi proteica. Utilizzando modelli al computer della struttura tridimensionale di EF‑G, il team ha mostrato che quella posizione si trova su una cerniera tra due domini di EF‑G, dove la proteina si piega e ruota mentre spinge il ribosoma. La prolina in questa cerniera sembra essere particolarmente conservata tra molti batteri correlati, suggerendo la sua importanza. Quando viene sostituita, la flessibilità e la compattezza complessive di EF‑G cambiano, rimodellando sottilmente il modo in cui la proteina si adatta al ribosoma. Simulazioni di docking che posizionano virtualmente la gentamicina sui complessi ribosoma–EF‑G suggeriscono che questo piccolo spostamento strutturale altera la geometria della regione di legame del farmaco. Nella forma mutata, la gentamicina non è più in grado di intrappolare il ribosoma nello stadio vulnerabile in cui normalmente blocca il movimento.
Piccoli spostamenti nella struttura dell’RNA con grandi conseguenze
Sono emerse anche mutazioni in due delle multiple copie del gene 16S rRNA che contribuiscono a formare la subunità minore del ribosoma. Mappando questi cambiamenti sulle strutture dell’RNA note, gli autori hanno rilevato che tutte le mutazioni si addensavano nella regione detta “corpo 5′”, vicino al punto dove la gentamicina e una proteina ribosomiale adiacente si legano normalmente. Predizioni dettagliate al computer hanno mostrato che il ripiegamento complessivo dell’RNA era per lo più preservato, ma che anse e steli locali vicini alle basi mutate risultavano sottilmente riorganizzati. Questi piccoli aggiustamenti strutturali sono sufficienti a modificare le interazioni dell’RNA sia con le proteine ribosomiali sia con il farmaco, potenzialmente spostando basi critiche fuori dalle posizioni precise di cui la gentamicina ha bisogno per un legame stretto. In combinazione con la mutazione della cerniera di EF‑G, il risultato è un ribosoma che continua a leggere le istruzioni genetiche anche in presenza di alte concentrazioni del farmaco. 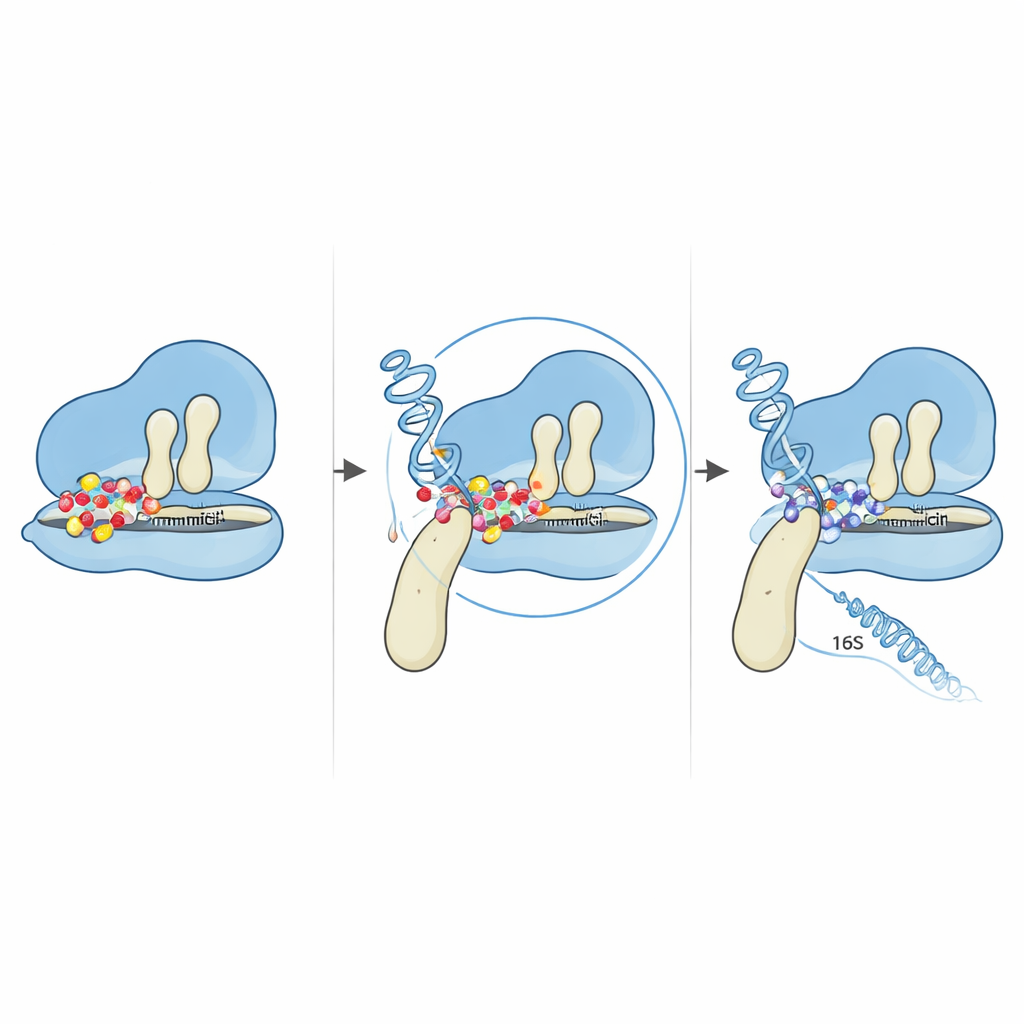
Cosa significa per contrastare la resistenza
Considerato nel suo insieme, il lavoro mostra che E. coli può assemblare rapidamente una difesa altamente specifica contro la gentamicina modificando sia il sito di aggancio del farmaco sull’RNA ribosomiale sia una parte mobile del motore proteico che guida la traduzione. Questi cambiamenti non distruggono la fabbrica proteica; la sintonizzano quel tanto che basta perché l’antibiotico non riesca più a incepparne il funzionamento. Il sistema ARGP fornisce un modo semplice e visivo per generare e studiare tali percorsi di resistenza in condizioni controllate e potrebbe essere adattato ad altri farmaci e patogeni. Per i non specialisti, il messaggio chiave è che la resistenza non è una tendenza vaga e lenta: può emergere rapidamente tramite modifiche molecolari molto precise. Capire questi cambiamenti nei dettagli è essenziale se vogliamo progettare nuovi antibiotici e strategie terapeutiche che restino un passo avanti rispetto ai batteri in evoluzione.
Citazione: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Parole chiave: resistenza agli antibiotici, gentamicina, Escherichia coli, ribosoma, evoluzione sperimentale