Clear Sky Science · ru
Изучение молекулярных механизмов устойчивости к аминогликозидам у Escherichia coli MG1655 с помощью планшета для роста при антибиотике
Почему быстро меняющиеся микробы важны для всех
Антибиотики спасли бесчисленное количество жизней, но бактерии постепенно учатся избегать их действия. В этой работе исследуют, как обычная кишечная бактерия Escherichia coli может выработать устойчивость к широко применяемому антибиотику гентамицину всего за пару дней. Наблюдая за развитием устойчивости на специально спроектированном планшете для роста и затем изучая ДНК и молекулярные структуры бактерий, исследователи раскрывают новые детали того, как эти микробы перехитривают препарат. Их выводы помогают объяснить, почему устойчивость может возникать так быстро, и указывают на инструменты, которые могли бы прогнозировать, какие терапии, вероятно, потерпят неудачу.
Новый планшет для наблюдения эволюции в действии
Чтобы сделать появление устойчивости хорошо заметным, команда создала то, что они называют Планшетом роста при антибиотике (ARGP). Представьте чашку Петри, разделённую на три концентрических кольца: в центре нет препарата, в среднем кольце — умеренная доза, а по краю — очень высокая концентрация. В центр высадили стандартный, чувствительный к лекарству штамм E. coli и позволили бактериям продвигаться наружу через тонкий полутвердый слой. По мере распространения микробы встречали всё более высокие концентрации гентамицина. Большинство останавливалось на границах между зонами, но иногда маленькие ответвления преодолевали барьер и продолжали рост. Всего за два–три дня некоторые линии процветали при концентрациях антибиотика, в десять раз превышающих минимальную ингибирующую концентрацию для исходного штамма. 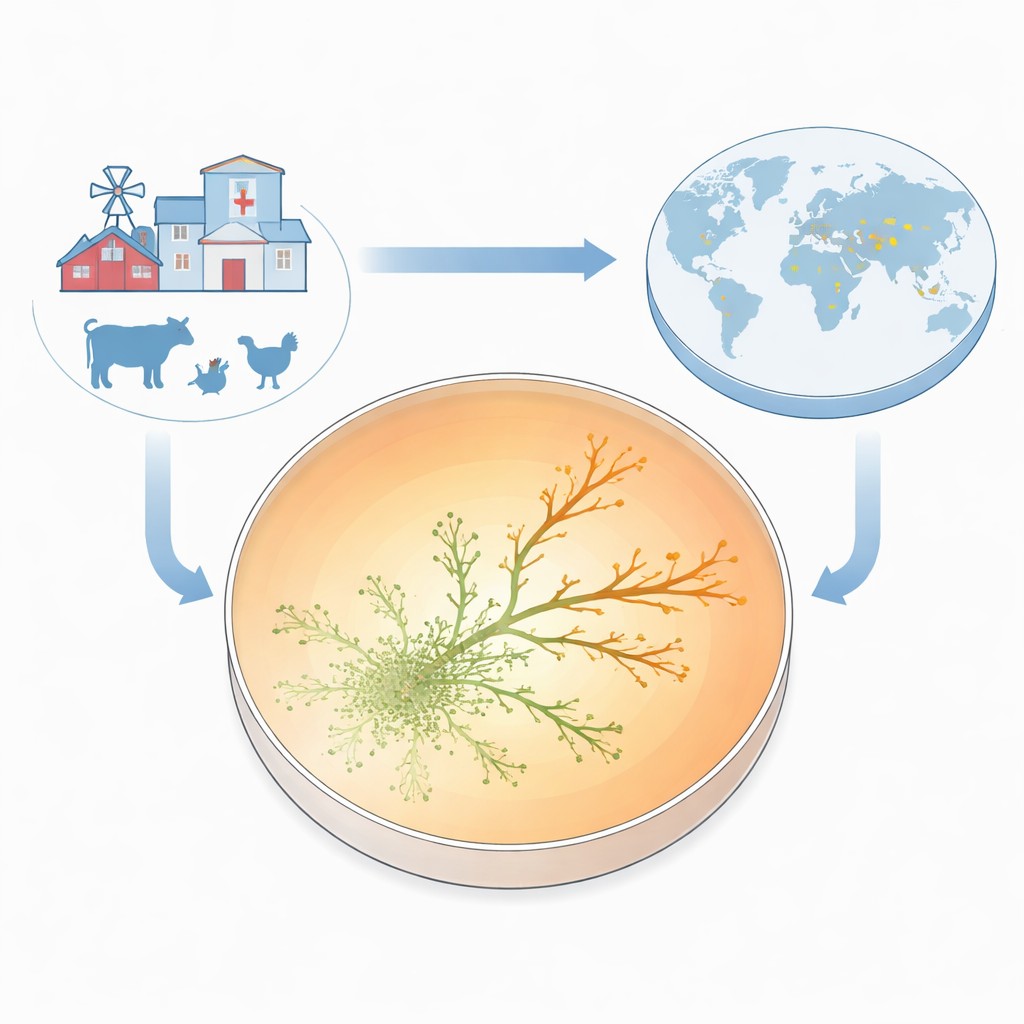
Отслеживание генетических изменений, лежащих в основе выживания
Появление устойчивых колоний — это было только начало. Учёные собрали клетки из этих стойких отростков и сравнили их полный последовательности ДНК с последовательностью исходного штамма. Тщательно отфильтровав артефакты и фрагменты контаминантов, они сосредоточились на изменениях в генах, известных своей ролью в синтезе белка внутри клетки. Были обнаружены мутации в участках генетического кода, формирующих белковый аппарат клетки: в нескольких копиях гена 16S рРНК и в гене fusA, который кодирует ключевой фактор сопряжения — белок EF-G. Оба мишени логичны, поскольку гентамицин действует, связываясь с бактериальной рибосомой — комплексом, который читает генетические инструкции и собирает новые белки. Любая модификация, меняющая этот аппарат, но не разрушающая его полностью, может ослабить действие препарата.
Как одиночная «шарнирная» замена ослабляет действие препарата
Наиболее заметной была одиночная замена нуклеотида в гене fusA, которая приводит к замене одной аминокислоты — пролина на треонин — в положении 610 белка EF-G. EF-G действует как подвижная рука, помогающая перемещать тРНК и матричную РНК через рибосому по мере сборки каждого нового белка. С помощью компьютерного моделирования трехмерной структуры EF-G команда показала, что эта позиция находится в «шарнире» между двумя доменами EF-G, где белок сгибается и поворачивается в процессе продвижения рибосомы. Пролин в этой точке оказался особенно консервативным у многих родственных бактерий, что указывает на его важность. При его замене изменяются общая гибкость и компактность EF-G, что тонко перестраивает его сопряжение с рибосомой. Моделирование докинга, в котором виртуально размещали гентамицин на комплексах рибосома–EF-G, показывает, что это небольшое структурное смещение меняет геометрию участка связывания препарата. В мутированной форме гентамицин больше не может «запереть» рибосому в уязвимом состоянии, в котором он обычно блокирует движение.
Небольшие сдвиги в структуре РНК с большими последствиями
Мутации также возникли в двух из нескольких копий гена 16S рРНК, которые формируют малую субчастицу рибосомы. Нанесение этих изменений на известные структуры РНК показало, что все они сосредоточены в области «5′ тела», рядом с участком, где обычно закрепляются гентамицин и соседний рибосомный белок. Детальные компьютерные прогнозы показали, что общая укладка РНК в целом сохраняется, но локальные петли и стебли рядом с мутированными основаниями тонко перестраиваются. Эти небольшие структурные корректировки достаточны, чтобы изменить взаимодействие РНК как с рибосомными белками, так и с препаратом, потенциально отводя ключевые основания от точных позиций, необходимых гентамицину для плотного связывания. В сочетании с «шарнирной» мутацией EF-G это даёт рибосому, которая продолжает считывать генетические инструкции даже при высоких концентрациях лекарства. 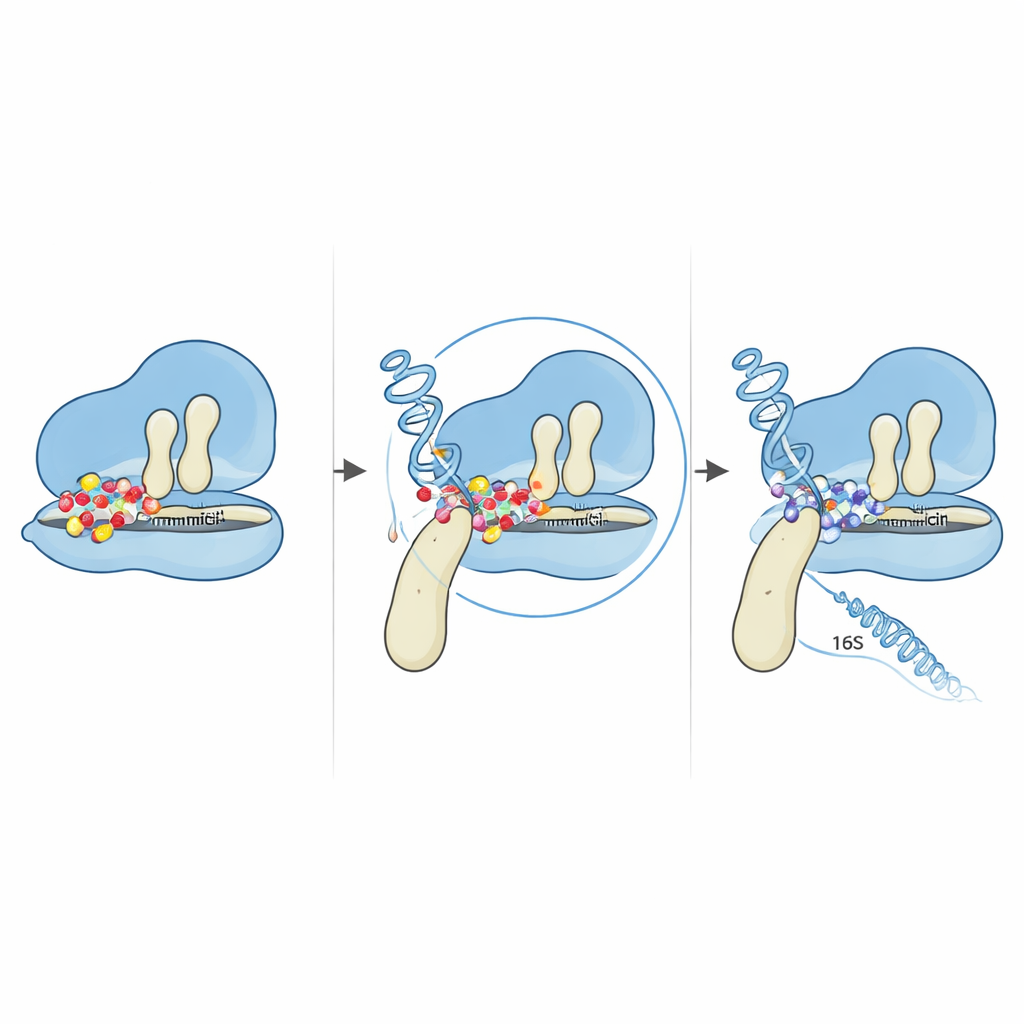
Что это значит для борьбы с устойчивостью
В совокупности работа показывает, что E. coli способна быстро собрать высокоспецифичную защиту против гентамицина, изменив и посадочное место препарата на рибосомной РНК, и подвижную часть белкового механизма трансляции. Эти изменения не разрушают белковую фабрику; они тонко её настраивают так, что антибиотик уже не может застрять в механизме. Система ARGP предоставляет простой визуальный способ генерировать и изучать такие пути устойчивости в контролируемых условиях и может быть адаптирована для других препаратов и патогенов. Для неспециалистов ключевое сообщение таково: устойчивость — это не размытая медленная тенденция, она может возникать быстро посредством точечных молекулярных правок. Понимание этих правок в деталях необходимо, если мы хотим разработать новые антибиотики и стратегии лечения, которые будут на шаг впереди эволюционирующих бактерий.
Цитирование: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Ключевые слова: устойчивость к антибиотикам, гентамицин, Escherichia coli, рибосома, экспериментальная эволюция