Clear Sky Science · sv
Utforskning av molekylära mekanismer för aminoglykosidresistens i Escherichia coli MG1655 med hjälp av Antibiotic Resistance Growth Plate
Varför snabbt föränderliga mikrober berör oss alla
Antibiotika har räddat otaliga liv, men bakterier lär sig stegvis att undvika dem. Denna artikel undersöker hur vanliga tarmbakterier, Escherichia coli, kan utveckla resistens mot ett mycket använt läkemedel, gentamicin, på bara ett par dagar. Genom att följa resistens som uppstår på en specialkonstruerad tillväxtplatta och sedan granska bakteriernas DNA och molekylära strukturer avslöjar forskarna nya detaljer om hur dessa mikrober överlistar läkemedlet. Deras fynd hjälper till att förklara varför resistens kan uppkomma så snabbt och pekar på verktyg som kan förutsäga vilka behandlingar som riskerar att misslyckas.
En ny platta för att se evolution i arbete
För att göra resistens synlig i det ögonblick den uppstod byggde teamet det de kallar Antibiotic Resistance Growth Plate (ARGP). Föreställ dig en petriskål indelad i tre cirkulära band: inget läkemedel i mitten, en måttlig dos i mittzonen och en mycket hög dos längst ut. De sådde mitten med en standardstam av E. coli som är känslig för läkemedlet och lät bakterierna röra sig utåt genom ett tunt, halvt fast medium. När mikroberna spred sig mötte de successivt högre gentamicinnivåer. De flesta stoppades vid gränserna mellan zonerna, men då och då lyckades små utskott korsa in i nästa ring och fortsätta växa. Redan efter två till tre dagar frodades vissa linjer i antibiotikakoncentrationer som var tio gånger högre än den minsta koncentration som hämmade den ursprungliga stammen. 
Spåra de genetiska förändringarna bakom överlevnaden
Att se resistenta kolonier dyka upp var bara början. Forskarna samlade celler från dessa härdiga utväxter och jämförde deras hela DNA-sekvenser med den ursprungliga stammen. Efter noggrann filtrering av artefakter och kontaminerande fragment fokuserade de på förändringar i gener som är kända för att vara involverade i proteinproduktionen inne i cellen. De fann mutationer i delar av den genetiska koden som bygger cellens proteinmaskineri: flera kopior av 16S ribosomalt RNA-genen och en gen kallad fusA, som kodar för en viktig hjälpprotein känd som EF-G. Båda målen är logiska eftersom gentamicin verkar genom att binda till bakteriens ribosom, komplexet som läser genetiska instruktioner och sätter ihop nya proteiner. Varje justering som förändrar detta maskineri utan att förstöra det helt kan dämpa läkemedlets effekt.
Hur en enda gångjärnsförändring försvagar läkemedlet
Den mest iögonfallande förändringen var en enkelbokstavsförändring i fusA-genen som byter ut en aminosyra—prolin—mot en annan—treonin—på position 610 i EF-G-proteinet. EF-G fungerar som en rörlig arm som hjälper till att förflytta tRNA och mRNA genom ribosomen medan varje nytt protein byggs. Med hjälp av datoriserade modeller av EF-G:s tredimensionella struktur visade teamet att denna position sitter vid ett gångjärn mellan två av EF-G:s domäner, där proteinet böjer och svänger när det driver ribosomen framåt. Prolinet vid detta gångjärn verkar vara ovanligt väl bevarat hos många närbesläktade bakterier, vilket antyder dess betydelse. När det ersätts förändras EF-G:s övergripande flexibilitet och kompakthet, vilket subtilt omformar hur proteinet passar mot ribosomen. Dockningssimuleringar som i princip placerar gentamicin på ribosom–EF-G-komplex föreslår att denna lilla strukturella förändring ändrar geometrin i läkemedlets bindningsregion. I den muterade formen kan gentamicin inte längre fånga ribosomen i den sårbara fas där det normalt blockerar rörelse.
Små skift i RNA-struktur med stora konsekvenser
Mutationer uppstod också i två av de flera kopiorna av 16S rRNA-genen som hjälper till att bilda ribosomens mindre subenhet. Genom att kartlägga dessa förändringar på kända RNA-strukturer fann författarna att alla klustrade i "5′ body"-regionen, nära där gentamicin och ett närliggande ribosomalt protein normalt fäster. Detaljerade datorprognoser visade att RNA:s övergripande veckning till stor del bevarades, men lokala slingor och stammar i närheten av de muterade nukleotiderna var subtilt omarrangerade. Dessa små strukturella justeringar räcker för att förändra hur RNA interagerar med både ribosomala proteiner och läkemedlet, och kan skjuta kritiska baser ur de precisa positioner som gentamicin behöver för stark bindning. I kombination med EF-G-gångjärnsmutationen blir resultatet en ribosom som fortsätter läsa genetiska instruktioner även i närvaro av höga läkemedelsnivåer. 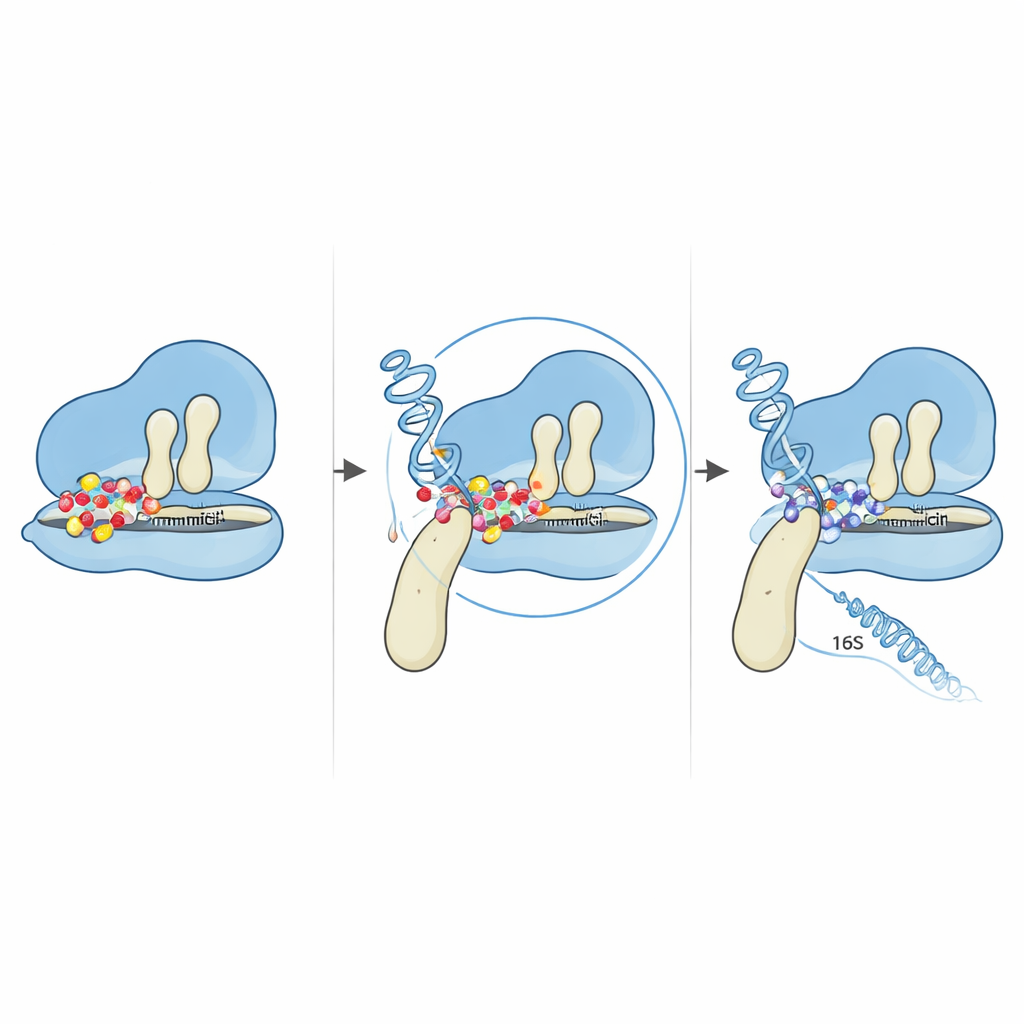
Vad detta betyder för att bekämpa resistens
Tillsammans visar arbetet att E. coli snabbt kan montera ett mycket specifikt försvar mot gentamicin genom att modifiera både läkemedlets fästpunkt på ribosomalt RNA och en rörlig del av det proteinmotor som driver translationen. Dessa förändringar förstör inte proteinfabriken; de finslipar den precis så mycket att antibiotikan inte längre kan blockera mekaniken. ARGP-systemet ger ett enkelt, visuellt sätt att framkalla och studera sådana resistensvägar under kontrollerade förhållanden och kan anpassas till andra läkemedel och patogener. För icke-specialister är huvudbudskapet att resistens inte är en vag, långsam trend—den kan uppstå snabbt genom precisa molekylära ändringar. Att förstå dessa ändringar i detalj är avgörande om vi ska kunna designa nya antibiotika och behandlingsstrategier som ligger steget före de utvecklande bakterierna.
Citering: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Nyckelord: antibiotikaresistens, gentamicin, Escherichia coli, ribosom, experimentell evolution