Clear Sky Science · tr
Aminoglikozid direncinin Escherichia coli MG1655’teki moleküler mekanizmalarını Antibiotik Direnci Büyüme Plakası kullanarak keşfetmek
Neden hızla değişen mikroplar herkes için önemli
Antibiyotikler sayısız hayat kurtardı, ama bakteriler bunlardan kaçınmayı giderek öğreniyor. Bu makale, sıradan bağırsak bakterisi Escherichia coli’nin yaygın kullanılan bir antibiyotik olan gentamisine yalnızca birkaç gün içinde nasıl direnç geliştirebildiğini inceliyor. Direncin özel olarak tasarlanmış bir büyüme plakası üzerinde nasıl ortaya çıktığını izleyip ardından bakterilerin DNA’sını ve moleküler yapısını inceleyerek araştırmacılar, bu mikropların ilacı nasıl etkisiz hâle getirdiğine dair yeni ayrıntılar ortaya koyuyor. Bulgular, direncin neden bu kadar çabuk ortaya çıkabildiğini açıklamaya yardımcı olurken hangi tedavilerin başarısız olabileceğini öngörmeye yarayabilecek araçlara işaret ediyor.
Evrimi gözlemlemek için yeni bir plaka
Direnç ortaya çıkarken görünür kılmak için ekip, Antibiotik Direnci Büyüme Plakası (ARGP) adını verdikleri yapıyı oluşturdu. Merkezinde ilaç olmayan, orta halkasında orta doz, dış kenarında çok yüksek doz bulunan üç dairesel bölmeye ayrılmış bir petri kabını düşünün. Ortaya hassas, standart bir E. coli suşu ektiler ve bakterilerin ince, yarı katı bir tabaka boyunca dışa doğru yayılmasına izin verdiler. Mikroplar yayılırken gittikçe artan gentamisin konsantrasyonlarıyla karşılaştı. Çoğu bölge sınırlarında durdu, ama bazen küçük çıkıntılar bir sonraki halkanın ötesine geçmeyi başararak büyümeye devam etti. Sadece iki-üç gün içinde bazı soylar, orijinal suşu durdurmak için gereken minimumun on katı ilaç konsantrasyonunda bile gelişiyordu. 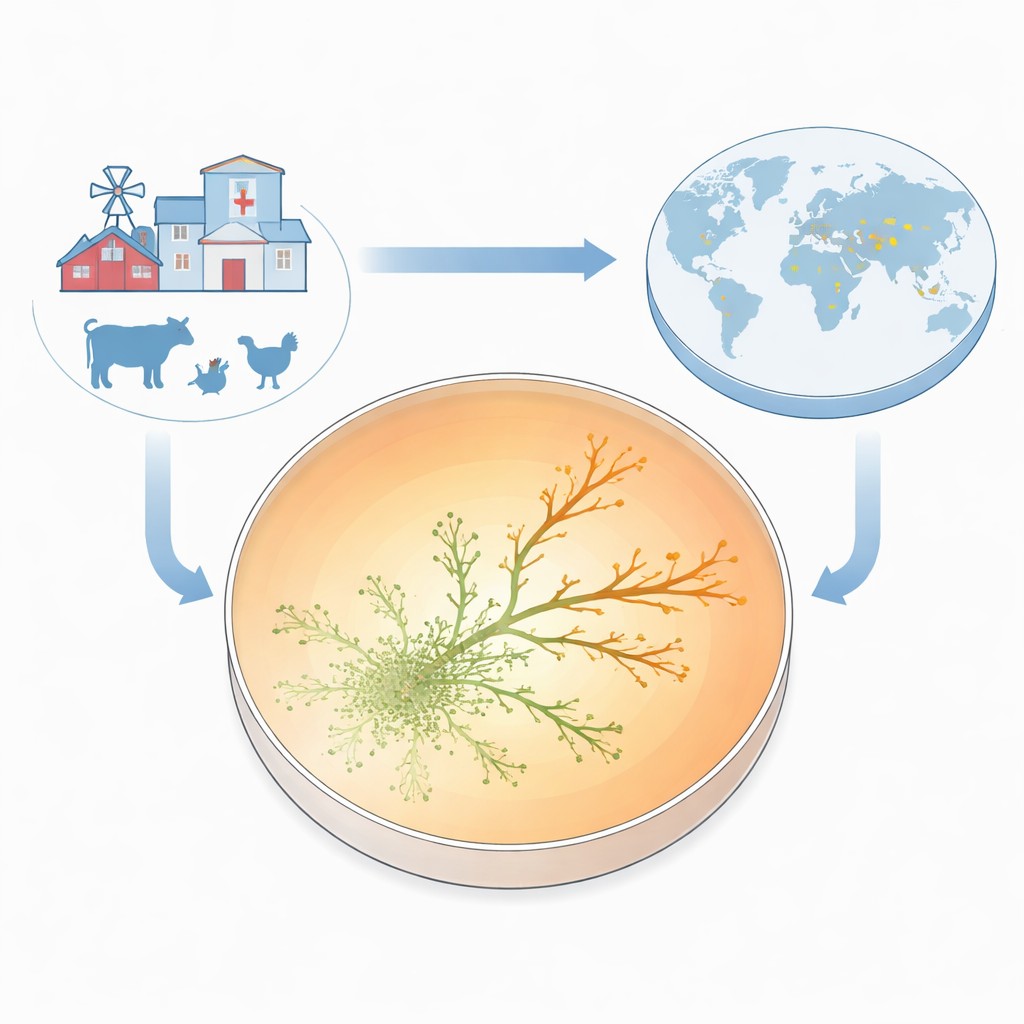
Hayatta kalmanın arkasındaki genetik değişiklikleri izlemek
Dirençli koloni görünümlerini gözlemlemek yalnızca başlangıçtı. Bilim insanları bu dayanıklı çıkıntılardan hücreleri topladı ve tüm DNA dizilerini orijinal suşunkilerle karşılaştırdı. Artefaktları ve kontaminant parçacıkları dikkatle filtreledikten sonra, hücre içindeki protein üretiminde rolü olduğu bilinen genlerdeki değişikliklere odaklandılar. Hücrenin protein yapım makinesini oluşturan genetik kodun parçalarında mutasyonlar buldular: birden çok 16S ribozomal RNA geni kopyasında ve EF‑G adlı önemli bir yardımcı proteini kodlayan fusA geninde değişiklikler. Her iki hedef de mantıklı çünkü gentamisin, genetik talimatları okuyan ve yeni proteinleri birleştiren ribozoma tutunarak etki eder. Bu makinayı tamamen bozmayacak şekilde yapılan herhangi bir ince ayar, ilacın etkisini azaltma potansiyeline sahiptir.
Tek bir menteşe değişikliğinin ilacı zayıflatması
En çarpıcı değişiklik, fusA geninde tek harfli bir değişiklikti; EF‑G proteininde 610. pozisyonda bir aminoasid—prolin—başka bir aminoasidle—treonin—yer değiştiriyordu. EF‑G, her yeni protein oluşurken transfer RNA’larını ve haberci RNA’yı ribozom boyunca kaydırmaya yardım eden hareketli bir kol gibi davranır. EF‑G’nin üç boyutlu yapısının bilgisayar modellerini kullanarak ekip, bu pozisyonun protein içinde iki alan arasında bir menteşede yer aldığını, protein bükülüp dönerek ribozomu ilerletirken burada kıvrıldığını gösterdi. Bu menteşedeki prolin birçok ilişkili bakteride alışılmadık derecede korunmuş görünüyor; bu da önemine işaret ediyor. Yer değiştirdiğinde EF‑G’nin genel esnekliği ve kompaktlığı değişiyor ve böylece proteinin ribozoma nasıl oturduğu ince bir şekilde yeniden şekilleniyor. Ribozom–EF‑G komplekslerine gentamisini sanal olarak yerleştiren yerleştirme simülasyonları, bu küçük yapısal değişikliğin ilacın bağlanma bölgesinin geometrisini değiştirdiğini öne sürüyor. Mutasyona uğramış formda gentamisin artık ribozomu normalde hareketi engellediği savunmasız aşamada tutamıyor.
RNA yapısındaki küçük değişikliklerin büyük sonuçları
Mutasyonlar ayrıca ribozomun küçük yarısını oluşturmaya yardımcı olan birden çok 16S rRNA geni kopyasından ikisinde de ortaya çıktı. Bu değişiklikleri bilinen RNA yapıları üzerine haritalarken, hepsinin gentamisin ve yakınındaki bir ribozomal proteinin normalde bağlandığı yere yakın olan “5′ gövde” bölgesinde kümelendiğini buldular. Ayrıntılı bilgisayar tahminleri, genel RNA kıvrımının büyük ölçüde korunduğunu, ancak mutasyona uğrayan bazların yakınındaki yerel döngü ve sapların ince olarak yeniden düzenlendiğini gösterdi. Bu küçük yapısal ayarlamalar, RNA’nın hem ribozomal proteinlerle hem de ilaçla etkileşimini değiştirebilecek kadar etkilidir; kritik bazları gentamisinin sıkı bağlanması için gerekli kesin konumlardan uzaklaştırabilir. EF‑G menteşe mutasyonuyla birleştiğinde sonuç, yüksek ilaç seviyelerine rağmen genetik talimatları okumaya devam eden bir ribozomdur. 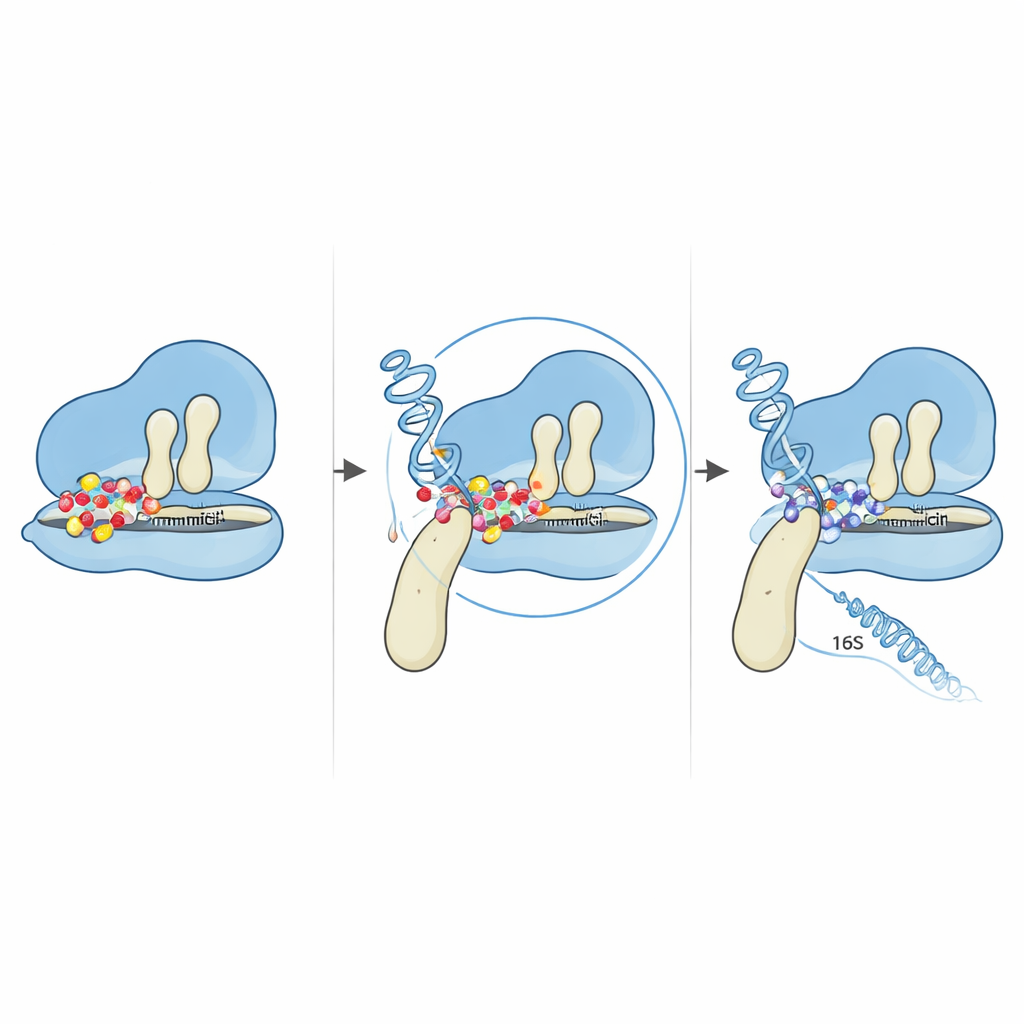
Dirençle mücadele için bunun anlamı
Bir araya getirildiğinde çalışma, E. coli’nin hem ribozomal RNA üzerindeki ilacın bağlanma bölgesini hem de çeviriyi sağlayan protein motorunun hareketli bir parçasını değiştirerek gentamisine karşı hızla son derece spesifik bir savunma inşa edebildiğini gösteriyor. Bu değişiklikler protein fabrikasını yok etmiyor; ilacın işleyişini engelleyecek şekilde ince ayar yapıyor. ARGP sistemi, kontrollü koşullar altında bu tür direnç yollarını üretmek ve incelemek için basit, görsel bir yol sağlıyor ve diğer ilaçlar ile patojenlere uyarlanabilir. Uzman olmayanlar için ana mesaj şudur: direnç belirsiz veya yavaş bir eğilim değil—hassas moleküler değişikliklerle hızla ortaya çıkabilir. Bu değişiklikleri ayrıntılı biçimde anlamak, evrimleşen bakterilerin bir adım önünde kalacak yeni antibiyotikler ve tedavi stratejileri tasarlamak için elzemdir.
Atıf: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Anahtar kelimeler: antibiyotik direnci, gentamisin, Escherichia coli, ribozom, deneysel evrim