Clear Sky Science · fr
Exploration des mécanismes moléculaires de la résistance aux aminosides chez Escherichia coli MG1655 à l’aide d’une plaque de croissance pour la résistance aux antibiotiques
Pourquoi des microbes qui évoluent vite concernent tout le monde
Les antibiotiques ont sauvé d’innombrables vies, mais les bactéries apprennent progressivement à les contourner. Cet article examine comment des bactéries intestinales ordinaires, Escherichia coli, peuvent évoluer vers la résistance à un antibiotique largement utilisé, la gentamicine, en seulement quelques jours. En observant l’émergence de la résistance sur une plaque de croissance spécialement conçue puis en sondant l’ADN et les structures moléculaires des bactéries, les chercheurs révèlent de nouveaux détails sur la façon dont ces microbes déjouent le médicament. Leurs résultats aident à expliquer pourquoi la résistance peut apparaître si rapidement et indiquent des outils susceptibles de prédire quels traitements risquent d’échouer.
Une nouvelle plaque pour regarder l’évolution en action
Pour rendre la résistance visible au fur et à mesure de son apparition, l’équipe a construit ce qu’elle appelle la Plaque de Croissance pour la Résistance aux Antibiotiques (ARGP). Imaginez une boîte de Petri divisée en trois anneaux circulaires : pas de médicament au centre, une dose modérée dans l’anneau intermédiaire et une dose très élevée en périphérie. Ils ont ensemencé le centre avec une souche standard d’E. coli sensible au médicament et laissé les bactéries se déplacer vers l’extérieur à travers une couche semi‑solide fine. En s’étendant, les microbes rencontraient des concentrations de gentamicine de plus en plus élevées. La plupart étaient arrêtés aux frontières entre les zones, mais de temps à autre de petits bourgeons réussissaient à franchir l’anneau suivant et continuaient de croître. En seulement deux à trois jours, certaines lignées prospéraient à des concentrations d’antibiotique dix fois plus élevées que la concentration minimale nécessaire pour stopper la souche initiale. 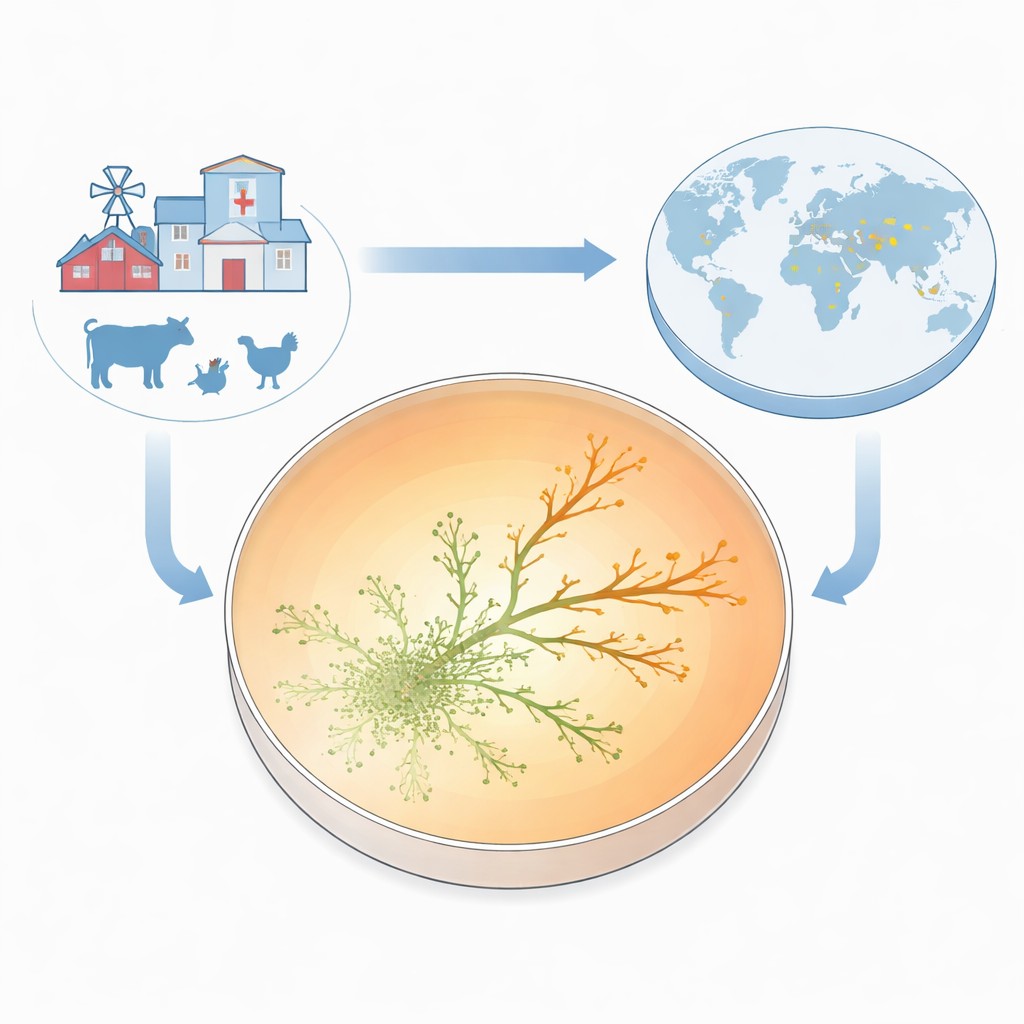
Suivre les changements génétiques derrière la survie
Voir apparaître des colonies résistantes n’était que le début. Les scientifiques ont prélevé des cellules de ces pousses robustes et comparé leur séquence d’ADN complète à celle de la souche d’origine. Après avoir soigneusement écarté artefacts et fragments contaminants, ils se sont concentrés sur les modifications dans des gènes connus pour intervenir dans la production de protéines à l’intérieur de la cellule. Ils ont trouvé des mutations dans des parties du code génétique qui forment la machinerie de synthèse des protéines : plusieurs copies du gène de l’ARN ribosomique 16S, et un gène appelé fusA, qui code pour une protéine auxiliaire clé connue sous le nom d’EF‑G. Ces deux cibles ont du sens car la gentamicine agit en se fixant au ribosome bactérien, le complexe qui lit les instructions génétiques et assemble les nouvelles protéines. Toute modification qui altère cette machinerie sans la détruire complètement peut atténuer l’effet du médicament.
Comment un seul changement d’articulation affaiblit le médicament
La modification la plus marquante était un changement d’une seule lettre dans le gène fusA, qui remplace un acide aminé — la proline — par un autre — la thréonine — à la position 610 de la protéine EF‑G. EF‑G agit comme un bras mobile qui aide à faire glisser les ARN de transfert et l’ARN messager à travers le ribosome lors de la synthèse protéique. À l’aide de modèles informatiques de la structure tridimensionnelle d’EF‑G, l’équipe a montré que cette position se trouve à une charnière entre deux domaines d’EF‑G, là où la protéine se plie et pivote en poussant le ribosome. La proline à cette charnière semble être exceptionnellement conservée chez de nombreuses bactéries apparentées, ce qui suggère son importance. Lorsqu’elle est remplacée, la flexibilité et la compacité globales d’EF‑G changent, remodelant subtilement la manière dont la protéine s’ajuste contre le ribosome. Des simulations d’amarrage virtuel qui placent la gentamicine sur les complexes ribosome–EF‑G suggèrent que ce minuscule déplacement structurel modifie la géométrie de la région de fixation du médicament. Dans la forme mutée, la gentamicine ne peut plus piéger le ribosome dans l’état vulnérable où elle bloque normalement le mouvement.
Petits réajustements de la structure ARN aux grandes conséquences
Des mutations sont également apparues dans deux des copies multiples du gène 16S rRNA qui contribuent à former la petite sous‑unité du ribosome. En cartographiant ces changements sur des structures ARN connues, les auteurs ont constaté qu’ils se regroupaient tous dans la région dite « corps 5′ », près de l’endroit où la gentamicine et une protéine ribosomale voisine se fixent habituellement. Des prédictions informatiques détaillées ont montré que le repliement global de l’ARN était largement préservé, mais que des boucles et des tiges locales proches des bases mutées étaient subtilement réarrangées. Ces petits ajustements structurels suffisent à modifier les interactions de l’ARN avec les protéines ribosomales et le médicament, pouvant repousser des bases critiques hors des positions précises dont la gentamicine a besoin pour une fixation serrée. Lorsqu’ils s’ajoutent à la mutation de la charnière d’EF‑G, le résultat est un ribosome qui continue de lire les instructions génétiques même en présence de fortes concentrations de médicament. 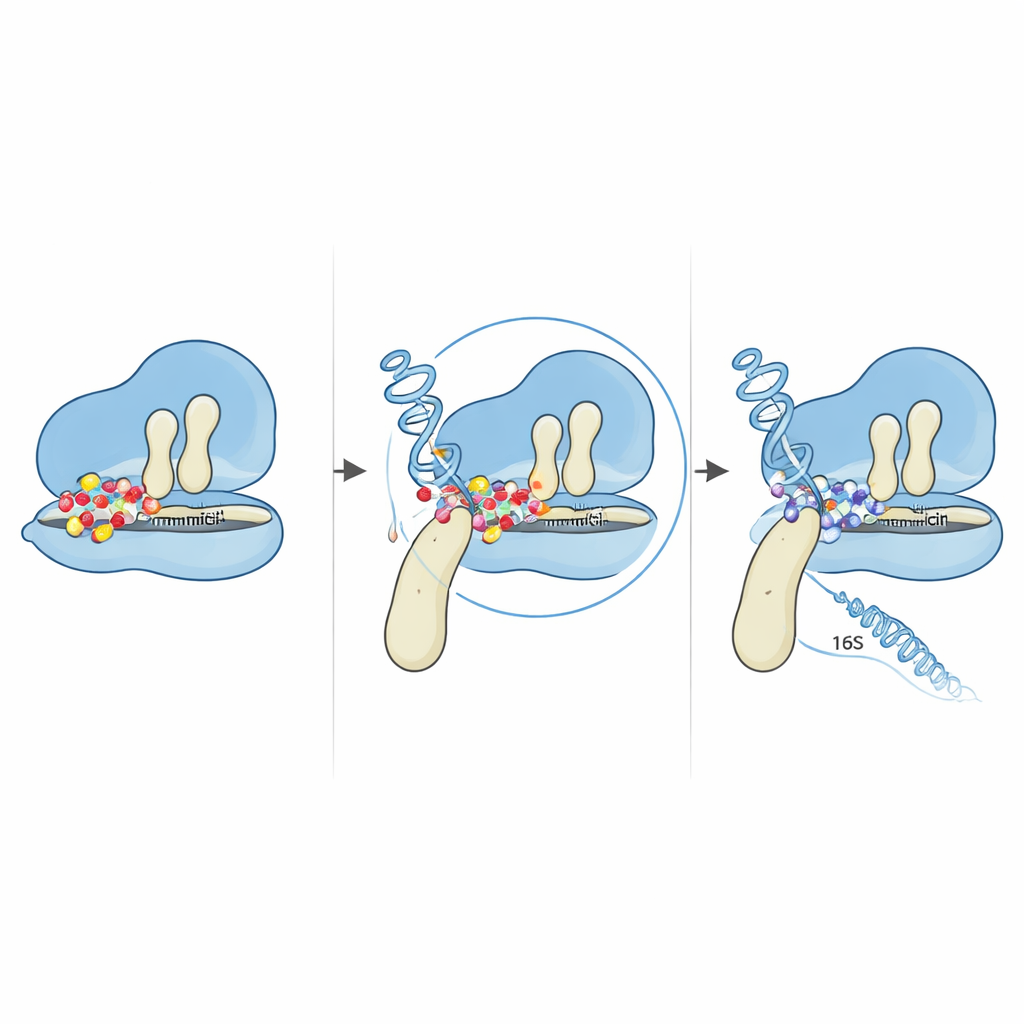
Ce que cela signifie pour lutter contre la résistance
Pris ensemble, les travaux montrent qu’E. coli peut rapidement assembler une défense hautement spécifique contre la gentamicine en modifiant à la fois le site d’ancrage du médicament sur l’ARN ribosomique et une pièce mobile du moteur protéique qui conduit la traduction. Ces changements ne détruisent pas l’usine à protéines ; ils l’ajustent juste assez pour que l’antibiotique ne puisse plus bloquer le processus. Le système ARGP offre une manière simple et visuelle de générer et d’étudier de telles voies de résistance dans des conditions contrôlées, et pourrait être adapté à d’autres médicaments et agents pathogènes. Pour les non‑spécialistes, le message clé est que la résistance n’est pas une tendance vague et lente — elle peut apparaître rapidement via des modifications moléculaires précises. Comprendre ces modifications en détail est essentiel si l’on veut concevoir de nouveaux antibiotiques et stratégies de traitement qui restent un pas devant les bactéries en évolution.
Citation: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Mots-clés: résistance aux antibiotiques, gentamicine, Escherichia coli, ribosome, évolution expérimentale