Clear Sky Science · es
Explorando mecanismos moleculares de resistencia a aminoglucósidos en Escherichia coli MG1655 usando la placa de crecimiento para resistencia a antibióticos
Por qué los microbios que cambian rápido importan a todos
Los antibióticos han salvado innumerables vidas, pero las bacterias aprenden de forma constante a esquivarlos. Este trabajo explora cómo bacterias comunes del intestino, Escherichia coli, pueden desarrollar resistencia a un antibiótico de uso generalizado, la gentamicina, en apenas un par de días. Al observar la aparición de resistencia en una placa de crecimiento diseñada ad hoc y luego examinar el ADN y las estructuras moleculares de las bacterias, los investigadores descubren detalles nuevos sobre cómo estos microbios burlan el fármaco. Sus resultados ayudan a explicar por qué la resistencia puede surgir tan rápido y señalan herramientas que podrían predecir qué tratamientos probablemente fallarán.
Una nueva placa para ver la evolución en acción
Para hacer visible la resistencia conforme emergía, el equipo construyó lo que llaman la Placa de Crecimiento para Resistencia a Antibióticos (ARGP). Imagínese una placa de Petri dividida en tres bandas circulares: sin fármaco en el centro, una dosis moderada en el anillo intermedio y una dosis muy alta en el borde exterior. Sembraron el centro con una cepa estándar sensible al fármaco de E. coli y dejaron que las bacterias se desplazaran hacia fuera a través de una capa delgada y semisólida. A medida que los microbios se expandían, encontraban concentraciones de gentamicina cada vez mayores. La mayoría quedaba detenida en las fronteras entre zonas, pero de vez en cuando pequeños brotes conseguían atravesar al siguiente anillo y seguir creciendo. En solo dos o tres días, algunas líneas prosperaban en concentraciones de antibiótico diez veces superiores a la mínima necesaria para detener la cepa original. 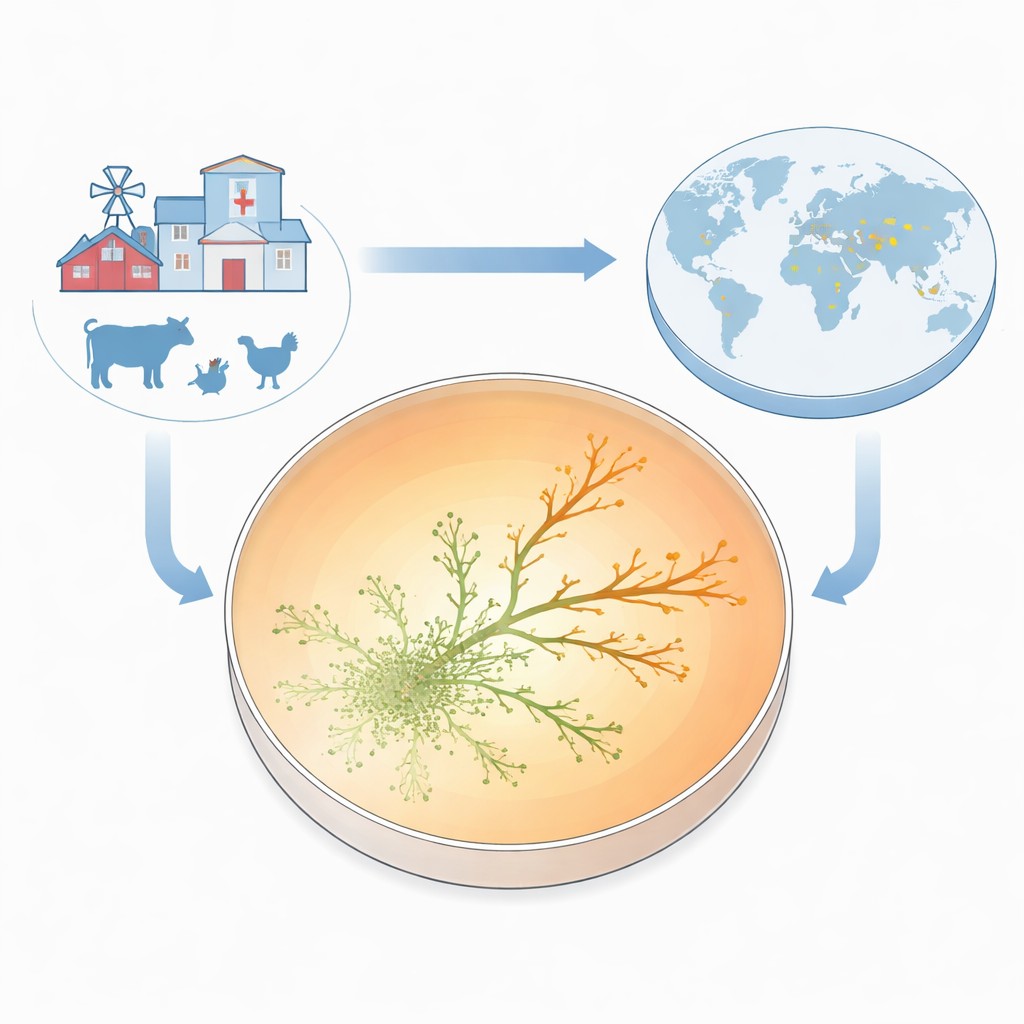
Rastreando los cambios genéticos detrás de la supervivencia
Ver aparecer colonias resistentes fue sólo el principio. Los científicos recopilaron células de esos brotes resistentes y compararon su secuencia de ADN completa con la de la cepa original. Tras filtrar cuidadosamente artefactos y fragmentos contaminantes, se centraron en cambios en genes conocidos por intervenir en la producción de proteínas dentro de la célula. Encontraron mutaciones en partes del código genético que construyen la maquinaria de fabricación de proteínas: varias copias del gen del ARNr 16S y un gen llamado fusA, que codifica una proteína auxiliar clave conocida como EF-G. Ambos objetivos tienen sentido porque la gentamicina actúa uniéndose al ribosoma bacteriano, el complejo que lee las instrucciones genéticas y ensambla nuevas proteínas. Cualquier ajuste que altere esta maquinaria sin destruirla por completo tiene el potencial de atenuar el efecto del fármaco.
Cómo un único cambio en una bisagra debilita el fármaco
La alteración más llamativa fue un cambio de una sola letra en el gen fusA que intercambia un aminoácido —prolina— por otro —treonina— en la posición 610 de la proteína EF-G. EF-G actúa como un brazo móvil que ayuda a desplazar los ARNt y el ARNm a través del ribosoma mientras se ensamblan las proteínas. Usando modelos informáticos de la estructura tridimensional de EF-G, el equipo mostró que esta posición se sitúa en una bisagra entre dos dominios de EF-G, donde la proteína se dobla y gira al empujar el ribosoma. La prolina en esa bisagra parece estar inusualmente conservada entre bacterias relacionadas, lo que sugiere su importancia. Cuando se sustituye, la flexibilidad y la compacidad global de EF-G cambian, remodelando sutilmente cómo la proteína encaja contra el ribosoma. Simulaciones de acoplamiento que colocan virtualmente la gentamicina en complejos ribosoma–EF-G sugieren que este pequeño cambio estructural altera la geometría de la región de unión del fármaco. En la forma mutada, la gentamicina ya no puede atrapar el ribosoma en la etapa vulnerable en la que normalmente bloquea el movimiento.
Pequeños cambios en la estructura del ARN con grandes consecuencias
También surgieron mutaciones en dos de las múltiples copias del gen del ARNr 16S que contribuyen a formar la subunidad pequeña del ribosoma. Al mapear estos cambios sobre estructuras de ARN conocidas, los autores encontraron que todos se agruparon en la región del “cuerpo 5′”, cerca de donde normalmente se acoplan la gentamicina y una proteína ribosomal vecina. Predicciones informáticas detalladas mostraron que el plegamiento global del ARN se conservaba en gran medida, pero que bucles y tallos locales próximos a las bases mutadas se reorganizaban sutilmente. Estos pequeños reajustes estructurales bastan para cambiar cómo el ARN interactúa tanto con proteínas ribosomales como con el fármaco, desplazando potencialmente bases críticas fuera de las posiciones precisas que la gentamicina necesita para unirse con firmeza. Cuando se combinan con la mutación de la bisagra en EF-G, el resultado es un ribosoma que sigue leyendo instrucciones genéticas incluso en presencia de altos niveles del antibiótico. 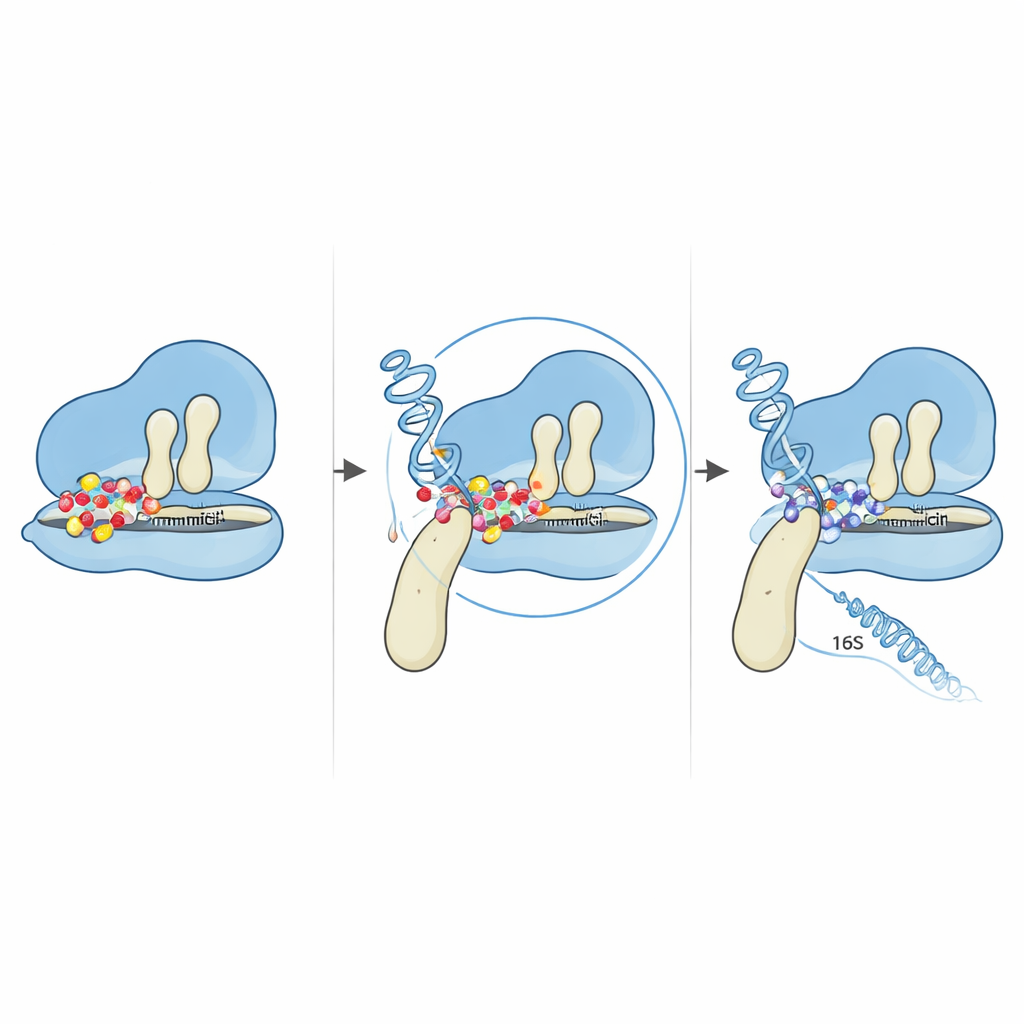
Qué significa esto para combatir la resistencia
En conjunto, el trabajo muestra que E. coli puede ensamblar rápidamente una defensa altamente específica contra la gentamicina modificando tanto el sitio de acoplamiento del fármaco en el ARN ribosomal como una pieza móvil del motor proteico que impulsa la traducción. Estos cambios no destruyen la fábrica de proteínas; la afinan lo justo para que el antibiótico ya no pueda bloquear su funcionamiento. El sistema ARGP ofrece una forma simple y visual de generar y estudiar estas vías de resistencia bajo condiciones controladas, y podría adaptarse a otros fármacos y patógenos. Para el público general, el mensaje clave es que la resistencia no es una tendencia vaga y lenta: puede surgir con rapidez mediante ediciones moleculares precisas. Comprender esas ediciones en detalle es esencial si queremos diseñar nuevos antibióticos y estrategias de tratamiento que se adelanten a las bacterias en evolución.
Cita: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
Palabras clave: resistencia a antibióticos, gentamicina, Escherichia coli, ribosoma, evolución experimental