Clear Sky Science · ja
抗生物質耐性成長プレートを用いた大腸菌MG1655のアミノグリコシド耐性の分子機構の解明
急速に変化する微生物が誰にとっても重要な理由
抗生物質は数え切れない命を救ってきましたが、細菌はそれを回避する方法を着実に学んでいます。本研究は、一般的な腸内細菌である大腸菌が、広く使われる抗生物質ゲンタマイシンにわずか数日で耐性を獲得しうる仕組みを探ります。耐性が現れる様子を専用に設計された成長プレート上で観察し、その後に細菌のDNAや分子構造を解析することで、これらの微生物が薬剤をどのように出し抜くかについて新たな詳細を明らかにしています。結果は、耐性がなぜ迅速に発生し得るかを説明し、どの治療が失敗しやすいかを予測する助けとなる道具を示唆します。
進化を実際に観察する新しいプレート
耐性が現れる過程を目に見えるようにするために、研究チームは「抗生物質耐性成長プレート(ARGP)」と呼ぶ装置を作成しました。ペトリ皿を中心に無薬の領域、中央リングに中等度の薬剤濃度、外周に非常に高い濃度の三つの同心円状の帯に分けたものを想像してください。研究者は薬剤に感受性のある標準株の大腸菌を中心に播き、薄い半固体層を介して外側へ泳がせました。微生物が拡散するにつれて、次第に高まるゲンタマイシン濃度に直面します。ほとんどはゾーンの境界で止まりますが、稀に小さな分岐が次のリングを越えて増殖を続けることがありました。わずか2〜3日間で、いくつかの系統は元の株を止めるのに必要な濃度の十倍もの抗生物質濃度下で繁栄するようになりました。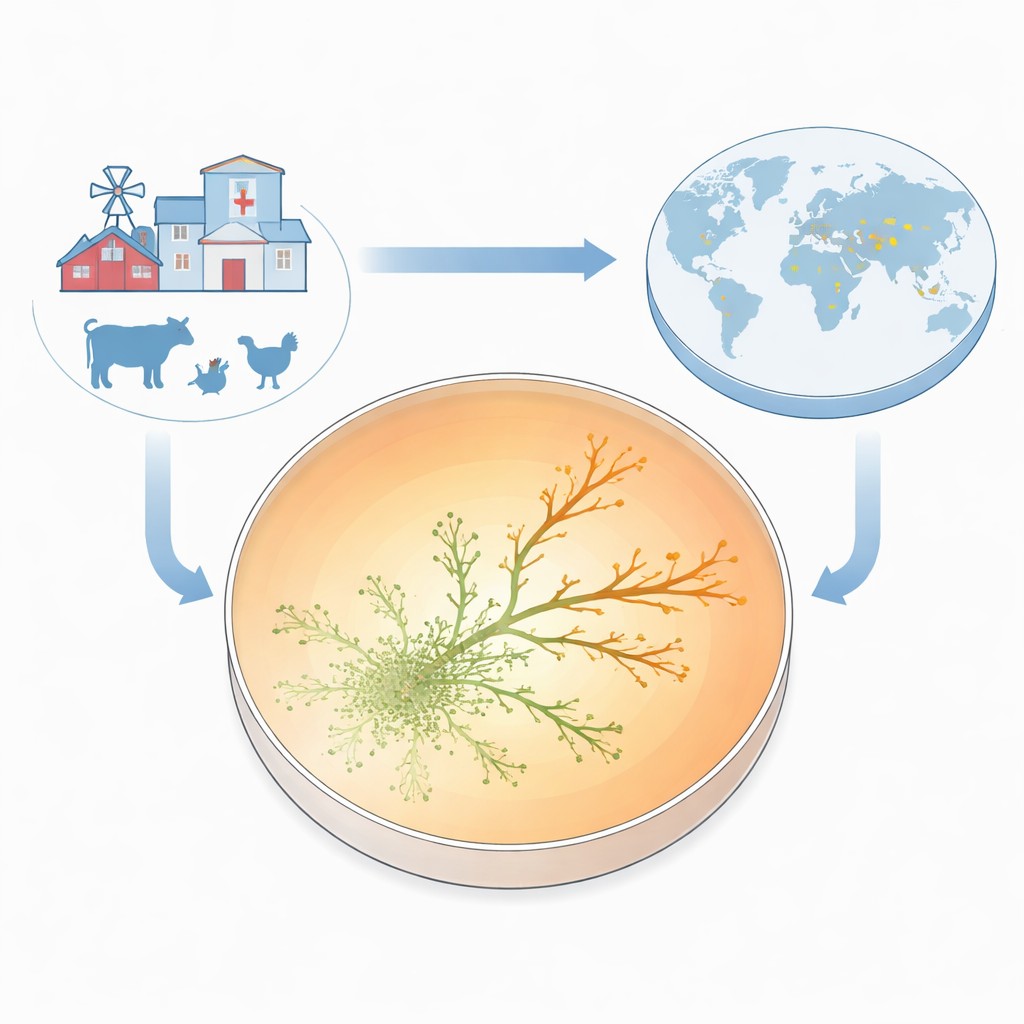
生存の背後にある遺伝的変化を追う
耐性コロニーの出現を観察することは出発点に過ぎませんでした。研究者らはこれらの頑健な外伸び株から細胞を採取し、元の株の全ゲノム配列と比較しました。人工的な変異や汚染断片を慎重に除外した後、細胞内でのタンパク質生産に関与することが知られている遺伝子の変化に焦点を当てました。複数コピー存在する16SリボソームRNA遺伝子と、EF-Gとして知られる重要な補助タンパク質をコードするfusA遺伝子に変異が見つかりました。どちらも妥当な標的で、ゲンタマイシンはタンパク質合成の指令を読み取り新しいタンパク質をつなぎ合わせる複合体である細菌リボソームに結合して作用するからです。装置を完全に壊さずにこの機構を変えるような微細な修正は、薬剤の効果を弱める可能性があります。
一か所のヒンジ変化が薬の効き目を弱める仕組み
最も目立った変化は、fusA遺伝子の一塩基置換によってEF-Gタンパク質の610番目の位置でプロリンがスレオニンに置き換わる一アミノ酸の変化でした。EF-Gは、転移RNAとメッセンジャーRNAをリボソーム内で移動させるのを助ける可動アームのように働きます。EF-Gの三次元構造をコンピュータモデルで解析したところ、この位置はEF-Gのドメイン間のヒンジに位置し、タンパク質がリボソームを押し進める際に曲がってスイングする部分に当たります。このヒンジのプロリンは関連する多くの細菌で非常に保存されているように見え、その重要性を示唆しています。これが置換されると、EF-Gの全体的な柔軟性や緊密さが変化し、タンパク質がリボソームに当たる形が微妙に変わります。リボソーム–EF-G複合体にゲンタマイシンを仮想的に配置するドッキングシミュレーションは、この小さな構造変化が薬剤の結合領域の幾何学を変えることを示唆します。変異型では、ゲンタマイシンは通常リボソームを移動できない脆弱な段階で捕捉できなくなります。
RNA構造の小さな変化が大きな影響を与える
複数コピーの16S rRNA遺伝子のうち二つにも変異が現れ、小さなリボソーム半分を形成するこれらのRNAに影響を与えました。既知のRNA構造にこれらの変化をマッピングすると、すべてが“5′ボディ”領域に集中しており、そこは通常ゲンタマイシンや近傍のリボソームタンパク質が結合する場所の近くにあたります。詳細なコンピュータ予測は、全体的なRNAの折りたたみは大きく保たれているものの、変異した塩基の近くの局所的なループや茎の配置が微妙に再配列されていることを示しました。これらの小さな構造的調整は、RNAがリボソームタンパク質や薬剤と相互作用する仕方を変えるのに十分であり、重要な塩基をゲンタマイシンが堅く結合するために必要な正確な位置からわずかに押しのける可能性があります。EF-Gのヒンジ変異と組み合わさると、その結果として高濃度の薬剤存在下でも遺伝情報を読み続けられるリボソームが生まれます。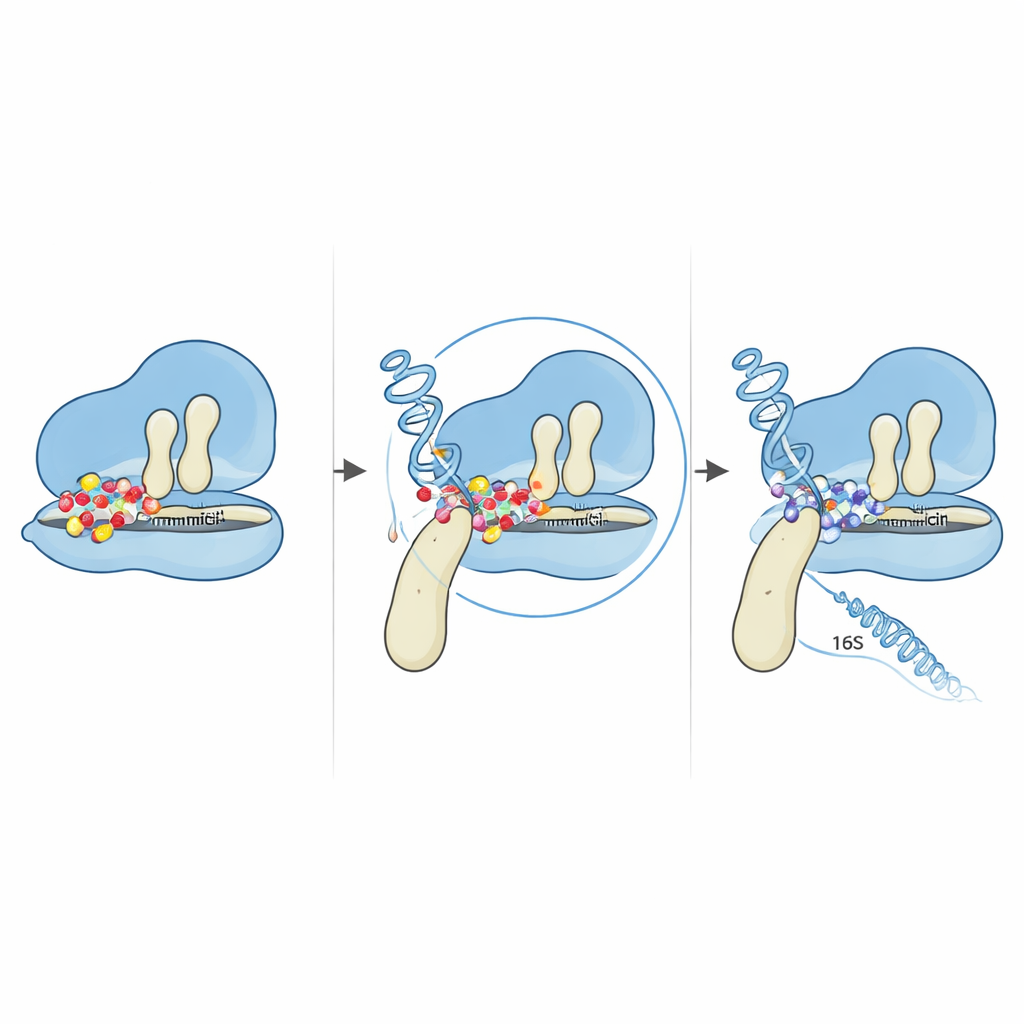
耐性対策にとっての意義
総じて、本研究は大腸菌がリボソームRNA上の薬剤結合部位と翻訳を駆動するタンパク質機構の可動部位の両方を修正することで、ゲンタマイシンに対して極めて特異的な防御を短期間で組み立て得ることを示しています。これらの変化はタンパク質合成装置を破壊するのではなく、それを微調整して抗生物質が機構を詰まらせられないようにします。ARGPシステムは、こうした耐性経路を制御下で視覚的かつ単純に生成して研究する方法を提供し、他の薬剤や病原体へも適用可能です。専門外の読者への要点は、耐性は漠然とした遅い傾向ではなく、精密な分子編集を通じて急速に生じ得るということです。その編集を詳細に理解することが、新たな抗生物質や治療戦略を進化する細菌より一歩先に設計するために不可欠です。
引用: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
キーワード: 抗生物質耐性, ゲンタマイシン, 大腸菌, リボソーム, 実験進化