Clear Sky Science · ar
استكشاف الآليات الجزيئية لمقاومة الأمينوجليكوزيدات في Escherichia coli MG1655 باستخدام صفيحة نمو مقاومة المضادات الحيوية
لماذا تهم الكائنات سريعة التغير الجميع
أنقذت المضادات الحيوية عدداً هائلاً من الأرواح، لكن البكتيريا تتعلّم تدريجياً كيف تتجنبها. تستعرض هذه الورقة كيف يمكن لبكتيريا الأمعاء الشائعة، الإشريكية القولونية، أن تطوّر مقاومة لمضاد شائع الاستخدام، الجنتامايسين، في غضون يومين فقط تقريباً. من خلال ملاحظة بروز المقاومة على صفيحة نمو مصممة خصيصاً ثم فحص حمضها النووي وتركيباتها الجزيئية، يكشف الباحثون تفاصيل جديدة عن كيفية تفوّق هذه الميكروبات على الدواء. تساعد نتائجهم في تفسير سبب ظهور المقاومة بسرعة، وتشير إلى أدوات قد تتنبّأ بالعلاجات التي قد تفشل.
صفيحة جديدة لمراقبة التطور أثناء حدوثه
لإظهار المقاومة أثناء ظهورها، بنى الفريق ما يسمّونه صفيحة نمو مقاومة المضادات الحيوية (ARGP). تخيّل طبق بتري مقسّم إلى ثلاثة أحزمة دائرية: لا دواء في المركز، وجرعة متوسطة في الحلقة الوسطى، وجرعة عالية جداً على الحافة الخارجية. زرعوا المركز بسلالة معيارية حساسة للمضاد وسمحوا للبكتيريا بالتحرك خارجاً عبر طبقة رقيقة شبه صلبة. أثناء انتشار الميكروبات، واجهت مستويات متزايدة من الجنتامايسين. أوقف معظمها عند حدود المناطق، لكن بين الحين والآخر نجح بعض التفرعات الصغيرة في عبور الحلقة التالية والمواظبة على النمو. في غضون يومين إلى ثلاثة، بدا أن بعض السلالات تزدهر في تراكيز من المضاد تفوق عشر مرات الحد الأدنى الذي يوقف السلالة الأصلية. 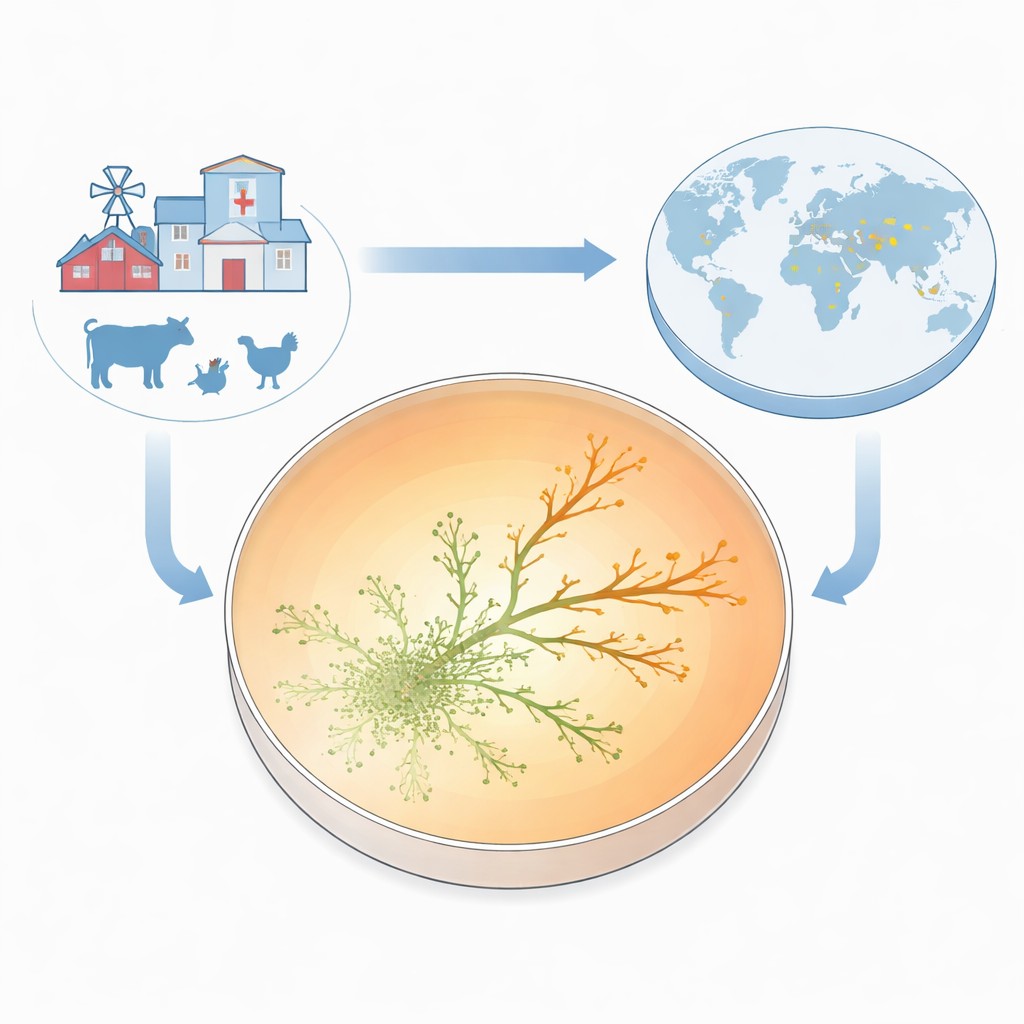
تتبُّع التغيرات الجينية وراء البقاء
كان ملاحظة بروز مجموعات مقاومة مجرد البداية. جمع العلماء خلايا من هذه النتوءات المقاومة وقارنوا تسلسل حمضها النووي الكامل مع ذلك الخاص بالسلالة الأصلية. بعد تصفية دقيقة للعيوب والقطع الملوِّثة، ركَّزوا على تغييرات في جينات معروفة بأنها تشارك في إنتاج البروتين داخل الخلية. وجدوا طفرات في أجزاء من الشفرة الوراثية التي تبني آلية صنع البروتين في الخلية: في عدة نسخ من جين ريبosomal RNA 16S، وجين يدعى fusA الذي يشفر بروتين مساعد رئيسي يعرف بـ EF-G. كلا الهدفين منطقيان لأن الجنتامايسين يعمل بالارتباط بالريبوسوم البكتيري، المركب الذي يقرأ التعليمات الوراثية ويربط الأحماض الأمينية لتكوين البروتينات الجديدة. أي تعديل يغير هذه الآلية دون تدميرها تماماً قد يضعف تأثير الدواء.
كيف يُضعِف تغيير مفصلي واحد الدواء
أبرز التغير كان استبدال حرف واحد في جين fusA يبدل حمضاً أمينياً واحداً—برولين—بآخر—تريونين—عند الموضع 610 في بروتين EF-G. يعمل EF-G كذراع متحركة تساعد في تحريك الـtRNA والـmRNA عبر الريبوسوم أثناء بناء كل بروتين جديد. باستخدام نماذج حاسوبية للتركيب ثلاثي الأبعاد لـ EF-G، بيّن الفريق أن هذا الموضع يقع عند مفصل بين اثنين من نطاقات EF-G، حيث ينحني البروتين ويدور أثناء دفعه للريبوسوم. يبدو أن البرولين في هذا المفصل محفوظ بشكل غير عادي عبر العديد من البكتيريا ذات الصلة، مما يشير إلى أهميته. عندما يُستبدل، تتغير مرونة EF-G ومدى انضغاطه بشكل طفيف، مما يعيد تشكيل كيفية احتكاك البروتين بالريبوسوم. تشير محاكاة ترسيب الجنتامايسين التي تضع الدواء افتراضياً على مجمعات الريبوسوم–EF-G إلى أن هذا التغيير الهيكلي الطفيف يغيّر هندسة موقع ارتباط الدواء. في الشكل المطوّر، لا يستطيع الجنتامايسين بعد ذلك حصر الريبوسوم في الحالة الضعيفة التي كان يعيق فيها الحركة.
تحولات طفيفة في بنية الـRNA ذات عواقب كبيرة
ظهرت طفرات أيضاً في اثنين من نسخ جين 16S rRNA المتعددة التي تشكل النصف الأصغر من الريبوسوم. من خلال رسم هذه التغيرات على هياكل الـRNA المعروفة، وجد المؤلفون أنها كلها تتجمع في منطقة «جسم الطرف 5′»، قرب الموضع الذي يرتبط فيه عادة الجنتامايسين وبروتين ريبوسومي مجاور. أظهرت توقعات حاسوبية مفصلة أن الطي العام للـRNA ظل محفوظاً إلى حد كبير، لكن الحلقات والسلاسل المحلية قرب القواعد المتحولة أعيد ترتيبها بشكل طفيف. هذه التعديلات البنيوية الصغيرة تكفي لتغيير كيفية تفاعُل الـRNA مع كل من بروتينات الريبوسوم والدواء، مما قد يزيح قواعد حاسمة بعيداً عن المواضع الدقيقة التي يحتاجها الجنتامايسين للارتباط المحكم. عند الجمع بين طفرة مفصل EF-G وتلك في الـ16S، تكون النتيجة ريبوسوماً يواصل قراءة التعليمات الوراثية حتى في وجود مستويات عالية من الدواء. 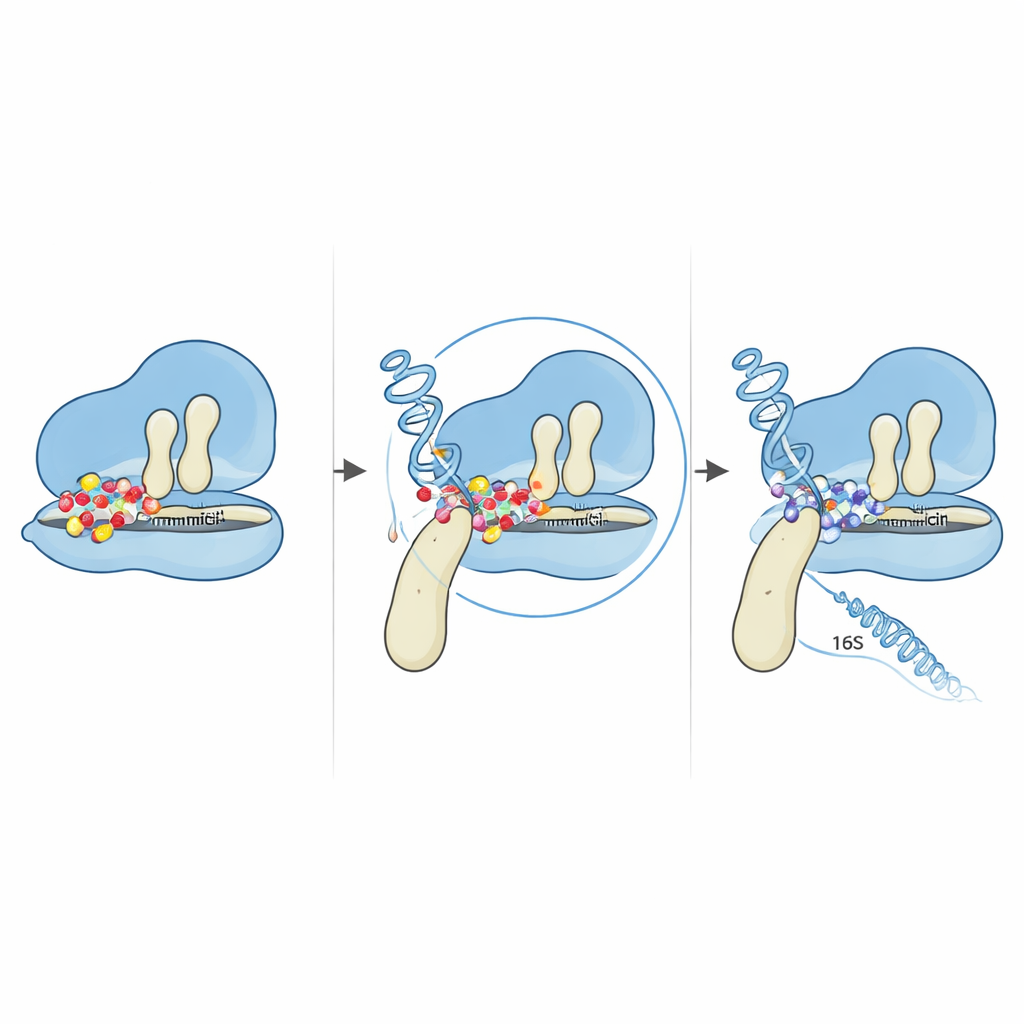
ما يعنيه هذا لمواجهة المقاومة
تُظهر النتائج مجتمعة أن الإشريكية القولونية قادرة سريعاً على بناء دفاع محدد للغاية ضد الجنتامايسين عبر تعديل كل من موقع ارتساء الدواء على ريبosomal RNA وجزء متحرك من المحرك البروتيني الذي يقود الترجمة. لا تدمر هذه التغيرات مصنع البروتين؛ بل تضبطه بدقة كافية بحيث لا يعود المضاد قادراً على تعطيل عمليته. يوفر نظام ARGP وسيلة بصرية بسيطة لتوليد ودراسة مثل هذه مسارات المقاومة تحت ظروف مضبوطة، ويمكن تكييفه لأدوية ومسببات أمراض أخرى. للقراء غير المتخصصين، الرسالة الأساسية هي أن المقاومة ليست ظاهرة غامضة بطيئة—يمكن أن تنشأ بسرعة عبر تعديلات جزيئية دقيقة. وفهم تلك التعديلات تفصيلياً ضروري إذا أردنا تصميم مضادات حيوية واستراتيجيات علاجية تظل خطوة أمام البكتيريا المتطورة.
الاستشهاد: Cullen, L., Eldridge, C., Jones, B. et al. Exploring molecular mechanisms of aminoglycoside resistance in Escherichia coli MG1655 using the antibiotic resistance growth plate. Sci Rep 16, 11958 (2026). https://doi.org/10.1038/s41598-026-41386-6
الكلمات المفتاحية: مقاومة المضادات الحيوية, جنتامايسين, الإشريكية القولونية, الريبوسوم, التطور التجريبي